8.1 在原发肿瘤环境中人树突状细胞产生的干扰素-α减少
8.1.1 pDC可产生I型IFN
浆细胞样树突状细胞(pDCs)是一类独特的骨髓源性免疫细胞,具有连接先天免疫系统和适应性免疫系统的作用。它们有两个主要功能,一是产生I型干扰素(IFN-I),另一个是作为抗原提呈细胞(APC)。pDCs虽然只占外周血单核细胞的0.3%-0.5%,但其分泌的IFN-α/β/ω确占循环淋巴细胞产生的IFN-I的95%以上。pDC 的激活和随后的 IFN-I 产生是通过模式识别受体(例如 toll 样受体 TLR)启动的信号级联反应的结果。
pDCs的激活主要通过TLR7和TLR9的结合,分别由ssRNA或非甲基化的CpG DNA激活,这两种激活物在微生物基因组中较常见,如病毒或其复制中间体。TLR7 和 TLR9 利用通用接头蛋白 MyD88发挥作用,MyD88通过转录因子 IRF7 和炎症转录因子 NF-κB 起作用,从而分别启动IFN-I和IFN-III 或炎性细胞因子和趋化因子的转录。激活后,pDC 也会发生表型变化,导致共刺激分子(CD40、CD86)上调。最终发展分化为“传统”的树突状细胞,具有经典DC(cDC)的形态和呈递抗原激活幼稚和记忆T细胞的能力。当调节失调时,pDC可以驱动自身免疫,因为自身核酸与抗体的复合物也会触发IFN-I的持续产生,从而增强自身免疫反应和促进B细胞增殖 。
在这种生理病理学状态下,HMBG1(核DNA结合蛋白)和LL37(阳离子抗菌肽)由濒死的细胞释放,它们与循环中的抗DNA自身抗体协同将自身核酸传递到pDC内,导致IFN-I以TLR7/9依赖的方式产生。正常情况下,如通过气道或口服传递抗原,pDC也可以通过促进调节性T细胞(Treg)的分化和增殖(Fig8.1)来促进外周耐受。pDC在免疫应答中的双重性可能取决于它们产生的IFN-I和干扰性刺激对它们的激活。
pDCs对于识别自身改变至关重要,因此可能有助于针对转化细胞的免疫反应。从而可以推测:肿瘤组织中pDC的增加可促进肿瘤抗原的识别和抗肿瘤免疫的激活,进而导致肿瘤的消除。
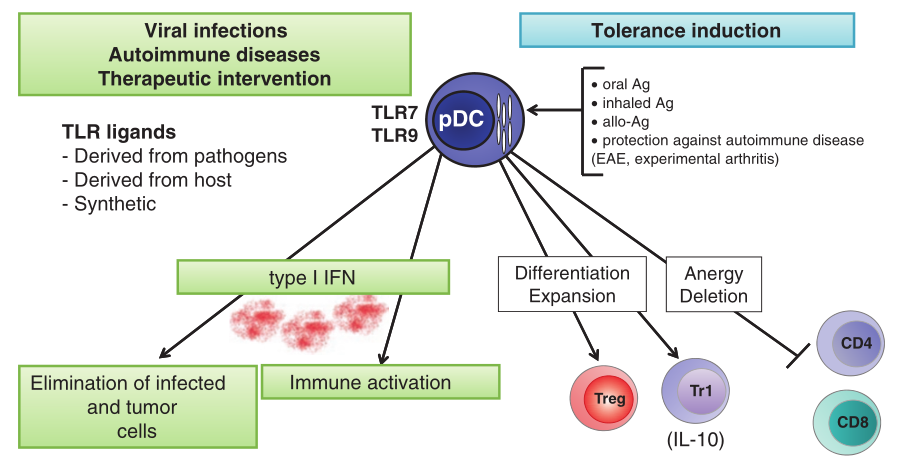
Fig 8.1 pDC可塑性。在病毒感染和发生某些自身免疫性疾病(狼疮、银屑病)期间,pDC通过与病毒或内源性核酸结合TLR-7/9而促进免疫应答,导致其表型的成熟以及产生IFN-I。然而,在其他情况下,如气道或口服抗原递送,在没有TLR-7/9参与的情况下,pDC也可以通过促进Treg的分化和扩增来促进外周耐受。
8.1.2 IFN-I在癌症免疫监视中的作用
虽然IFN-II很早就被认为是肿瘤免疫监视的关键介质,但直到最近才发现 IFN-I 在肿瘤免疫监视的作用。事实上,缺乏I型干扰素受体(IFNAR1)的转基因小鼠与野生型(WT)对照组小鼠相比,其更容易诱导原发肿瘤,并且抗体介导的 WT 宿主中 IFNα/β 受体的阻断可消除免疫原性移植肿瘤的排斥反应。最近的几份报告表明,宿主来源的IFN-I反应在肿瘤免疫监测的早期阶段以及放射治疗或某些化疗中起着关键作用。
此外,在人类中,重组 IFN-α 的外源给药已显示出治疗癌症患者的功效,并且肿瘤内IFNR1基因的高表达对癌症有积极的预后价值。与此一致,最近的研究表明,肿瘤间质中IFNAR1的下调刺激了肿瘤的发生发展,并且与人类结直肠癌患者免疫豁免区的形成以及不良的预后有着密切的相关性 。
从机制上看,IFN-I通过刺激CD8α+DCs将肿瘤来源的抗原交叉呈递给细胞毒性T淋巴细胞(CTL),从而促进抗肿瘤免疫,它还会产生刺激CTL克隆性扩增并提高其活性的信号。此外,cGAS/STING通路(重要异常胞浆DNA监控机制之一)也是细胞转化、化疗或放疗过程中诱导I型干扰素产生的关键途径。STING激动剂目前正在进行临床试验,旨在通过增加肿瘤中IFN-I的产生,限制肿瘤生长并促进特异性的抗肿瘤免疫反应。然而,在大多数癌症模型中,IFN-I分泌细胞的性质仍未确定,其他肿瘤来源的配体和先天感受器可能有助于诱导内源性IFN-I的产生。从这个角度来看,解释了为什么pDCs存在于病变组织中,它们能够通过TLR7/9感知宿主产生的因子,以及能够特异性产生IFN-I。
8.1.3 乳腺肿瘤中的pDCs
乳腺癌是女性中最常见的恶性肿瘤,也是女性癌症死亡的首要原因。其中,三阴性乳腺癌(非扩增的Her2neu,ERneg和PRneg)(TN)是最具侵袭性的。乳腺癌被认为是免疫原性肿瘤,因为(1)CD8+T细胞反应以及对TAA(Her2neu,p53,MUC1)的体液反应已被证实,(2)最近的报道证实CD8+T细胞浸润与较好的预后相关。此外,原发性乳腺肿瘤(BT)主要由先天免疫细胞浸润,即活化后的NK细胞、树突状细胞(DC)和显示活化表型的巨噬细胞(MΦ),表明它们在BT环境中受到刺激。也有报道称在BT中存在强大的CD4+和CD8+T淋巴细胞,表明建立有效抗肿瘤反应的免疫细胞存在于BT环境中。然而,当临床检测到肿瘤时,这种免疫反应大多数无法抑制肿瘤发展,因为已经形成了免疫抑制。
多项研究表明,肿瘤微环境破坏了免疫细胞的功能,有利于免疫抑制,从而逃避抗肿瘤免疫的建立。最近的研究也表明pDC在几种实体癌中积聚,但分析它们在肿瘤微环境中作用的研究非常有限。
在此背景下,我们观察到pDC的BT浸润与不良的临床结果相关,提示它们可能有助于肿瘤的免疫逃逸,并最终导致肿瘤的生长。
在一项对79例新确诊的乳腺癌患者进行的前瞻性研究中,我们观察到侵袭性BT中具有高有丝分裂指数和TN表型的pDC优先积聚。与患者的血液pDC相比,这种肿瘤相关(TA)-pDC部分表型(CD40、CD83、CD86和HLA-DR中间水平)被激活。这可能与GM-CSF对TA-pDC的局部作用有关,也可能与TLR7/9配体等内源性核酸有关。值得注意的是,GM-CSF和pDC的伴随增加与相对更具侵袭性的乳腺癌亚型显著相关。此外,与扁桃体pDC相似,TLR7/9激动剂体外激活的TA-pDC仍能成熟并具有诱导幼稚CD4+T细胞增殖以及分泌IL-10和IFN-γ的能力。相反,TA-pDC在体外TLR7/9刺激下分泌IFN-α的能力明显受损,并且特定发生在肿瘤部位。而TA-pDC中CXCL10等炎症分子的产生以及患者血液中IFN-α的产生没有受到影响。
8.1.4 卵巢肿瘤中的pDCs
卵巢癌(OC)是妇科最常见、最具侵袭性的恶性肿瘤。通过对血液、肿瘤和腹水中pDC的数量、表型和功能进行系统的比较,研究了肿瘤和恶性腹水中pDC存在的临床相关性。结果表明pDC在大多数恶性腹水中积聚,并且在36%的原发肿瘤中出现的频率很高。重要的是,与乳腺肿瘤一样,肿瘤中pDC的积聚是与早期肿瘤复发相关的独立预后因素。
这些结果在33例OC患者中得到证实,其中pDC经流式细胞仪鉴定为CD4+BDCA2+CD123+细胞,并通过免疫组织化学(IHC)在更大范围的OC患者(n=97)中得到证实。在本研究中,经福尔马林固定后的TApDC被鉴定为BDCA2+细胞。使用组织微阵列(TMA)对石蜡包埋(FFPE)组织进行分析,可以分析pDC对癌症上皮和癌症间质中存在的淋巴细胞聚集体的影响。在单变量分析中,癌上皮内TApDC的存在与早期复发和较短的中位生存期相关。在多变量分析中,除了临床预后因素(晚期、去瘤手术和肿瘤残留)外,TApDC的存在仍然是与较短的无进展生存期(PFS)相关的独立预后因素。
因此,在两个独立的队列中使用两种不同且互补的方法(流式细胞术和免疫组化),观察到OC肿瘤中TApDC的存在对患者预后的不良影响。这些数据证实了乳腺癌和其他肿瘤如黑色素瘤中的发现,表明TApDC的积聚与不良预后相关。总之,这些结果提示TApDC可能有助于免疫耐受和肿瘤发展。
与乳腺肿瘤不同,我们发现来自卵巢癌的TApDC与腹水pDC不同,(1) 卵巢癌的TApDC表达半成熟的表型,高表达CD40和CD86 ;(2) 由于CpG-A(TLR9配体)可以诱导产生大量I型IFN,因此抑制了TApDC 产生IFN-α,它对肿瘤微环境传递的内源性信号的应答是分化成熟而不是产生IFN-α,说明优先激活NFκB信号通路而不是IRF7途径。
8.1.5 导致TApDC功能缺陷的机制
乳腺和卵巢肿瘤在TApDC生物学上的相似性表明相同的抑制机制可能发生在不同部位的上皮癌症之间。
在乳腺癌和卵巢癌中,除IFN-α外,肿瘤环境还影响TLR激活的pDC产生IFN-β和TNF-α(肿瘤坏死因子α),但不影响CXCL10和MIP1-α/CCL3的产生。研究证实TGF-β(转化生长因子β)和TNF-α是改变TA-pDC功能的主要可溶性因子(Fig. 8.2),重组的TGF-β和TNF-α协同阻断了pDC产生IFN-α,并且中和肿瘤上清液中的TGF-β和TNF-α能够恢复pDC产生IFN-α的功能。通过检测乳腺肿瘤组织中TA-pDC细胞核中磷酸化的Smad2(信号转导子),进一步证实了肿瘤来源的TGF-β的参与。I型干扰素的作用机制不涉及TLR下调,而是肿瘤上清液或重组TGF-β1和TNF-α作用于DC后抑制其IRF-7的表达和核转位。
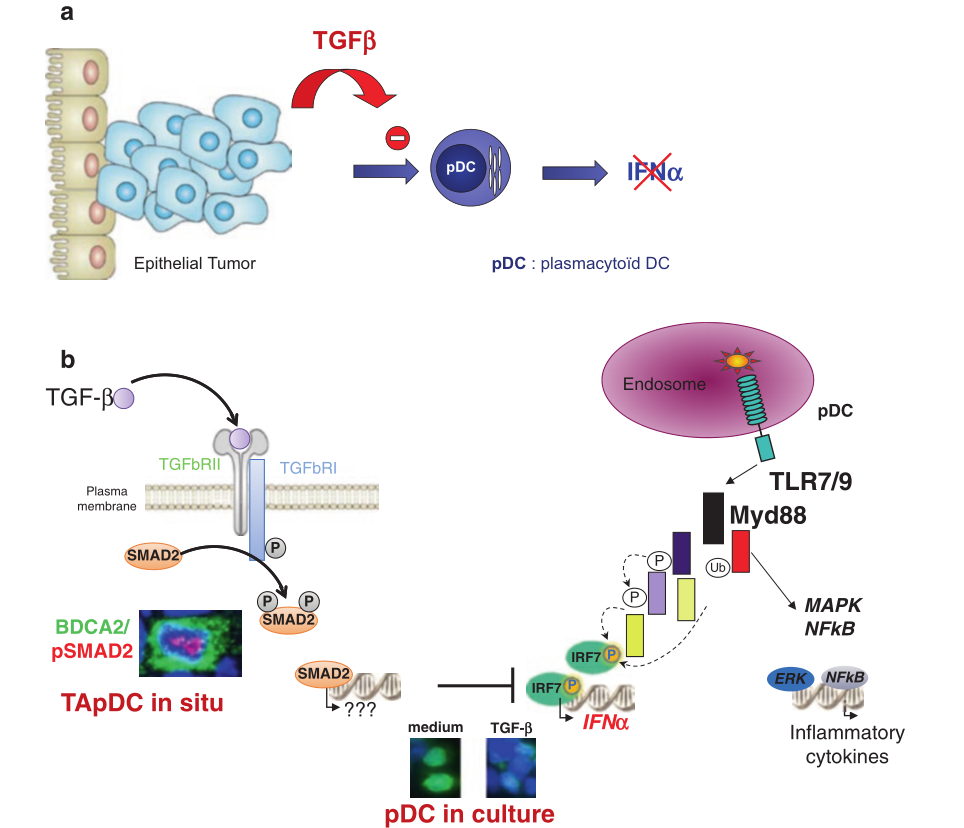
Fig 8.2 TApDC通过TGF-β抑制IFN-Ⅰ的产生。(A)乳腺和卵巢肿瘤环境中产生的TGF-β能有效抑制pDC产生I型IFN。(B)原位TApDC表达核磷酸化的Smad2,证实其表达TGF-β,并导致阻断irf7的核转位。
最近,E.Gatti和他的合作者发现,在造血细胞中,只有未激活的人pDCs表达BAD-LAMP(LAMP5)分子。BAD-LAMP(LAMP5)—树突状细胞(BAD)相关溶酶体相关膜蛋白(LAMP)样分子,控制TLR9向LAMP1+晚期内体转运,减少CpG DNA(非甲基化CpG寡核苷酸)激活的pDC产生IFN-1,并有利于 pDC 中产生TNF-α。相反,BAD-LAMP沉默后允许TLR9在没有外源性TLR激动剂的情况下激活。进一步研究证明,乳腺TA-pDC表达更多的BAD-LAMP,这导致它们无法产生 IFN-I。因此,BAD-LAMP的表达通过促进TLR9向晚期内体的分选,限制了pDC中IFN-I的表达。
由于IFN-I直接或间接通过免疫监视激活发挥重要的抗肿瘤功能,研究表明,BT抑制TApDC产生IFN-I可能为肿瘤细胞提供了一种选择性优势,代表了一种新的逃逸机制。
先前在慢性病毒感染(如艾滋病毒和丙型肝炎病毒)中已经描述过,pDC对TLR配体的反应影响了IFN -α的产生,从而阻碍有效免疫反应。之前也报道了乳腺癌、肺癌、头颈癌和慢性髓系白血病中的这种改变。
我们的研究结果表明,以TLR7/9为基础的免疫治疗联合TGF-β拮抗剂,靶向TApDC以恢复其IFN-α的产生,可能是诱导乳腺癌抗肿瘤免疫的一种可行策略。
8.2 乳腺肿瘤中的Treg
调节性T细胞(Treg)存在于许多实体肿瘤中。然而,它们对肿瘤进展的影响因肿瘤类型不同而不同。最近在乳腺癌中获得的证据表明,Treg定位于淋巴结中,而不是肿瘤中,并对患者的生存有负面影响。Tregs在浸润性乳腺癌中的不良影响已被证实,新辅助化疗中Tregs的减少与改善预后相关。此外,我们还发现,当与成熟DC接触时,Treg通过CCR4/CCL22被选择性地募集到淋巴结中,然后选择性地被激活(HLA-DRhigh,高诱导性共刺激分子(ICOS) high),从而阻断常规T细胞反应。
8.2.1 Treg招募
研究发现,参与免疫耐受的免疫亚群如pDC和CD4+CD25HighCD127negFoxP3+Treg和2型MΦ对BT的浸润与原发BT患者总生存期(OS)的不良预后密切相关。
一项深入的体外分析表明,肿瘤相关的Treg(TA Treg)(1)在表达ICOS、HLA-DR、GITR和CTLA-4时被激活,(2)它们具有抑制CD4+T细胞增殖和干扰素γ分泌的功能,(3) 是原位增殖的,与BT中检测到的静止的非调节性CD4+记忆T细胞和CD8+T细胞形成对比。
与相关患者的血液Treg不同,肿瘤相关Treg(TA Treg)表现出选择性的膜CCR4丢失,随后通过 BT 环境中分泌的 CCL22 进行主动募集。与此相一致的是,(1)CCL22(而不是CCL17)诱导的CCR4下调和(2)缺乏CCL22表达的BT不会被不依赖于CCR4另一配体CCL17产生的TA Treg浸润。
在原发性 BT 环境中,与肿瘤周围的乳腺组织相比,CCL22 表达强烈增加,这不仅通过 IHC 评估,而且通过 BT 上清液的 ELISA 检测。
有趣的是,在系统水平上观察到健康受试者、原发性BT患者、首次转移复发患者或更晚期BT患者的CCL22血浆水平逐渐升高,这可以反映肿瘤负荷。
研究使用BT上皮细胞株和原代BT标本,证明了免疫浸润在肿瘤上皮细胞选择性诱导CCL22而不是CCL17中的主要作用。使用(1)细胞因子受体和/或细胞因子的抑制性抗体或(2)外源重组细胞因子的体外实验表明,上皮肿瘤细胞与肿瘤浸润的NK细胞和M-Φ之间的通讯对CCL22的产生具有重要作用。通过这些研究,我们推测出如下事件的顺序(Fig8.3):(1) 检测到肿瘤细胞的 NK 细胞分泌 IFNγ;(2)IFNγ 激活 MΦ,有利于它们分泌 IL-1β 和 TNFα;(3) 3种细胞因子共同作用促进上皮性肿瘤细胞产生CCL22。使用BT原代标本的体外实验进一步证实了这一点,该实验证明了M-Φ和NK细胞的协同作用有利于肿瘤细胞产生CCL22。
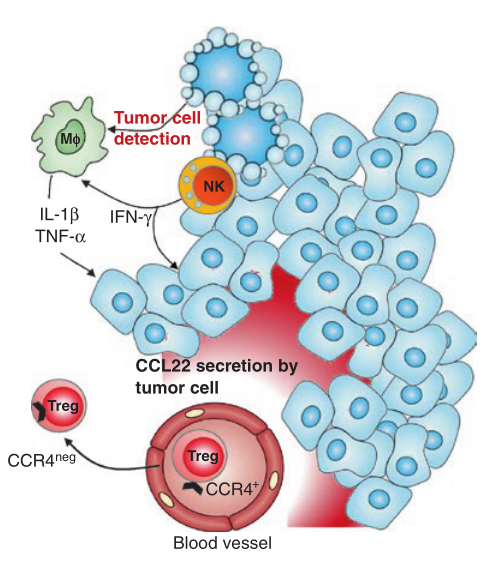
Fig 8.3 IFN-γ、TNF-α和IL-1β由NK和MΦ分泌,转化细胞分泌CCL22,在乳腺肿瘤中吸引CCR4+Treg。健康乳腺上皮细胞在腺泡内以极化的方式分泌低水平的CCL22,它们的转化通过浸润NK细胞导致干扰素γ的分泌而有利于它们的识别。IFN-γ可促进MΦ活化,与乳腺上皮肿瘤细胞相互作用后可分泌TNF-α和IL-1β。IFN-γ、IL-1β和TNF-α的联合作用将诱导肿瘤细胞CCL22的非极化分泌,从而诱导CCR4+Treg从外周募集,导致CCR4内化。
这说明了一种机制,允许转化的乳腺上皮细胞消除涉及NK和M-Φ的局部炎症,从而支持由CCL22分泌介导的Treg募集,正如先前在慢性结肠炎症中所描述的那样。反过来,TA Treg还可能通过以下途径促进肿瘤进展:(1)抑制NK细胞杀伤功能 ;(2)将1型MΦ转化为2型MΦ,产生促进血管生成、肿瘤细胞增殖和有利于免疫抑制的因子。
综上所述,这些数据有力地表明CCL22参与了BT的免疫抑制,并促进了疾病的进展。在此背景下,CCR4拮抗剂(小分子(AF-399))已被证实能在体外和体内阻断CCL22介导的人Treg和Th2细胞的募集。
— THE END —
V. Sisirak, I. Labidi-Galy, I. Le Mercier, N. Goutagny,
I. Puisieux, C. Ménétrier-Caux, and C. Caux
▉ 往期文章目录
基础免疫学系列
肿瘤免疫学系列
肿瘤免疫学-第6章:调节性T细胞的作用、作用机制以及对癌症的影响(下)
肿瘤免疫学-第6章:调节性T细胞的作用、作用机制以及对癌症的影响(上)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(下)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(上)
文献分享系列
年度巨献:神刊CA发布最新癌症数据:全球1000万人死于癌症,中国占比超3成
HLA-I分子加工和递呈抗原功能受损是免疫检查点抑制剂耐药的重要原因
生信入门学习笔记系列
基础实验技术系列
Annexin V/PI染色检测细胞凋亡-OncoLab实验室
仪器操作系列
蔡司LSM800激光共聚焦显微镜操作视频-中西医结合基础研究中心
IN Cell Analyzer2200高内涵细胞成像分析系统操作教程-中西医结合基础研究中心
作图投稿选刊系列
GraphPad+AI制作可发表级别的柱状图-OncoLab实验室
PubMed中如何按影响因子筛选检索结果并显示影响因子及分区?
如何使用EndNote软件插入参考文献(附6813种杂志参考文献格式文件)
中医中药系列

关注本号~

加入读者交流群~
本篇文章来源于微信公众号:OncoLab