肿瘤免疫学-第8章:免疫抑制网络中浆细胞样DC和调节性T细胞的作用(上)的内容可点击链接查看。
8.2.2 pDC介导的Treg增殖
高TATreg水平是影响BT(原发性乳腺肿瘤)患者生存预后不良的独立因素。此外,BT浸润的CD4+FoxP3neg T细胞(TATconv)具有记忆性表型(CD45RO+),与高度活化的TATreg(ICOShigh、CTLA-4+、GITR+、HLA-DR+)相比,很少被激活(Ki67+) 并在体外显示抑制活性。
此外,在黑色素瘤和卵巢肿瘤中,属于CD28家族的ICOS在TATreg中高表达,尽管TATreg原位表达Ki67,但TATreg在经典的抗CD3/抗CD28激动剂Ab包被的微球刺激下以及在外源性IL-2存在的情况下,不能在体外增殖,这与BT或血液中强烈增殖的血液Treg或Tconv形成了鲜明的对比。
重要的是,pDC对BT的浸润也与Treg浸润以及肿瘤内、尤其是TNBT内共同定位的两个细胞亚群相关,患者的生存预后也很差。因此,我们想知道TApDC是否可能有助于TATreg在BT微环境中的扩增。
我们观察到,TApDC和经BT培养上清预处理的健康供者的pDC在诱导Foxp3+Treg选择性扩增以及诱导分泌IL-10的CD4+T细胞的分化方面非常有效。有趣的是,外源性 IFN-α 逆转了由 TApDC 和 BT 环境诱导的免疫抑制性 CD4+ T 细胞反应,这表明在肿瘤中 IFN-α 的产生受损可导致TApDC 的促肿瘤能力增强。
为了了解TApDC的负面影响,我们建立了一个与人类病理非常接近的原位小鼠乳腺肿瘤模型,包括pDC和Treg浸润。我们发现TApDC大多是未成熟的,在体内保持其内化抗原的能力,并在体外保持其激活CD4+T细胞的能力。
更重要的是,TApDC在体外对作为TLR9配体的细胞因子可产生有特异性的改变,而对TLR7配体的反应保持不变。在体内,pDC的缺失延缓了肿瘤的生长,降低了肿瘤内Treg的比例,这表明TApDC提供了一个免疫抑制的环境,很可能是通过激活Treg促进了肿瘤的生长。
pDC先前被证明可调节多发性骨髓瘤(MM)细胞的生长,最近被证明有利于乳腺癌细胞的骨转移。
健康供者的pDC在TLR7或TLR9激动剂体外激活后高表达ICOS-L,而尽管TApDC其表型为CD40+HLA-DR+CD86+,但在乳腺和卵巢肿瘤扩增中缺乏ICOS-L的表达。
有趣的是,在体外,ICOS+CD4+T细胞与ICOS-L的结合会导致其在pDC膜上的表达下调,而在阻断性抗ICOS单抗存在的情况下,肿瘤细胞扩增悬液培养24小时后,TApDC上ICOS-L的表达恢复。
这些数据表明,在Treg/pDC接触过程中,BT中发生了ICOS/ICOS-L的相互作用。
有趣的是,[pDC+TA-CD4+T细胞]共培养的同种异体反应导致了FoxP3+Treg的强烈富集和增殖,并促进了IL-10的分泌。这种免疫抑制T细胞对pDC刺激的反应高度依赖于ICOS,因为加入中和的抗ICOS单抗可以选择性地抑制Treg增殖和IL-10的分泌。
此外,髓系DC (mDC, LinnegHLA-DR+ CD11c+ BDCA2neg)在激活后不过度表达ICOS-L,与Treg富集或强烈分泌IL-10无关。与我们对TATreg的观察一致的是卵巢肿瘤腹水中的ICOS+Treg或胸腺中表达ICOS的自然Treg(nTreg)对pDC的反应也依赖于ICOS/ICOS-L的相互作用。
此外,pDC还被报道通过ICOS/ICOSL相互作用增加CD4 T细胞对IL-10的产生。此外,我们最近与D Olive团队合作,证实了在体内ICOS-L对滤泡性淋巴瘤B细胞的下调,以及ICOS/ICOS-L依赖性的Treg在这种肿瘤环境中的扩张。
重要的是,与IL-10相反,在BT中既没有检测到IL-2、IL-17,也没有检测到IFN-γ。ICOS的中和仅轻微降低了TFN-α的分泌和Tconv的增殖,并不影响T细胞对mDC的应答。这表明ICOS有利于TATreg的扩增和IL-10的产生,但不参与原发BT免疫效应的诱导。最重要的是,在一组BT患者的回顾性队列中,IHC检测到ICOS主要在Treg上表达,在单变量分析中,ICOS+细胞浸润与PFS和OS减少相关,这与卵巢肿瘤的结果一致。
ICOS构成体液免疫反应的关键调节因子,主要是因为它刺激滤泡辅助T细胞(Tfh)激活,如ICOS缺陷小鼠和患者所表现的那样。一些报告也表明ICOS可能有助于抗肿瘤细胞免疫。事实上,在黑色素瘤患者中,已经在对抗CTLA-4(Ipilimumab)治疗有反应的患者中观察到产生IFN-γ的CD4+ICOS+T细胞的比例增加,而ICOS缺陷小鼠对携带B16肿瘤的抗CTLA-4治疗没有达到预期治疗效果。
ICOS+Treg已在几种人和小鼠肿瘤中被报道,我们的体外实验表明ICOS+TATreg的扩增强烈依赖ICOS,而不是来自外周血的Treg。ICOS依赖性可以反映这种Treg的特定亚群,或者与胸腺ICOS+nTreg类似的特定来源相关联,或者与其微环境或激活状态相关联。在这种情况下,目前还不清楚TATreg是nTreg还是由外周幼稚的T细胞诱导的。从逆转乳腺癌患者TACD4+T细胞免疫抑制反应的角度来看,了解ICOS阻断是否在nTreg、iTreg和TATreg之间显示出不同的影响可能是至关重要的。
综上所述,我们的数据表明,ICOS阻断可能是一种很有前景的治疗策略,可以根除原发性BT中产生TATreg和IL-10的CD4+T细胞。ICOS的中和可能需要是暂时的,以便在不干扰可能表达ICOS的效应细胞恢复的同时来消除Treg的扩增。
8.2.2.1 结论
总之,我们的结果显示BT微环境通过TGF-β和TNF-α抑制TApDC产生I型干扰素,从而增强了它们在体内通过ICOS-ICOSL相互作用促进FoxP3高表达TATreg扩增和IL-10分泌的T细胞的能力。
这有利于免疫抑制性的CD4+T细胞在肿瘤部位的聚集,阻止抗肿瘤免疫反应(Fig.8.4)。我们的观察结果为乳腺癌患者的新治疗策略的开发铺平了道路,(1)通过将TLR7/9配体与TNF-α和TGF-β拮抗剂结合使用,恢复TApDC的IFN-α的产生,从而诱导有效的抗病毒样抗肿瘤免疫,或(2)中和pDC和Treg之间的ICOS/ICOS-L相互作用。
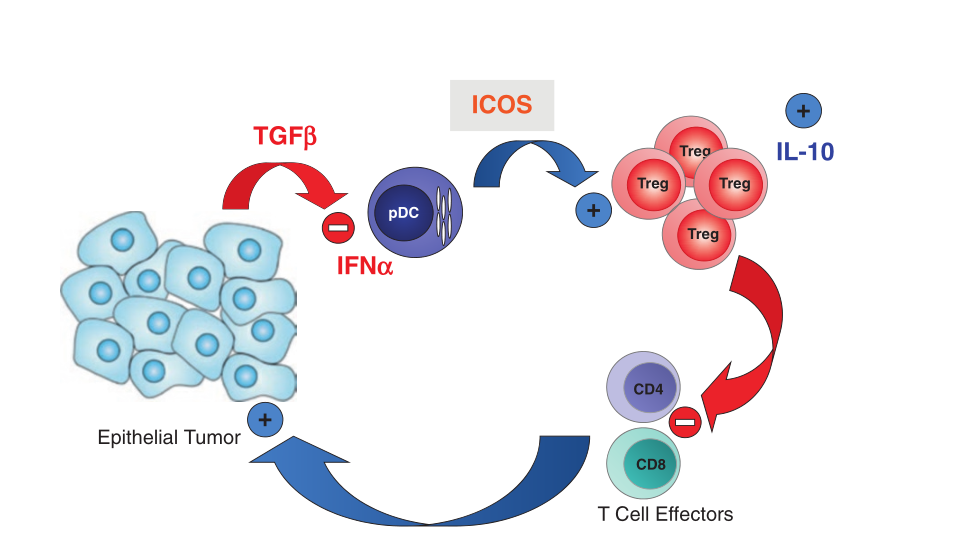
Fig 8.4 位于乳腺肿瘤免疫抑制网络中心的pDC/Treg,ICOS/ICOSL的作用。BT和ICOS+细胞通过TApDC表达ICOS-L参与Treg的增殖和IL-10的分泌,与患者的不良预后有关。这表明ICOS参与了T细胞介导的免疫抑制,提示中和Treg上的ICOS是一种新的肿瘤免疫治疗策略。
8.2.3 Treg介导的抑制作用
Treg能抑制大多数免疫细胞,包括CD4+和CD8+T细胞、DC、B细胞、MΦ和NK细胞。体内和体外研究表明,Treg介导的抑制可以通过多种机制发挥作用,并且不同的分子可以在细胞表面分泌或表达,并同时协同地积极参与它们对这些不同细胞亚群的抑制功能(Fig.8.5)。
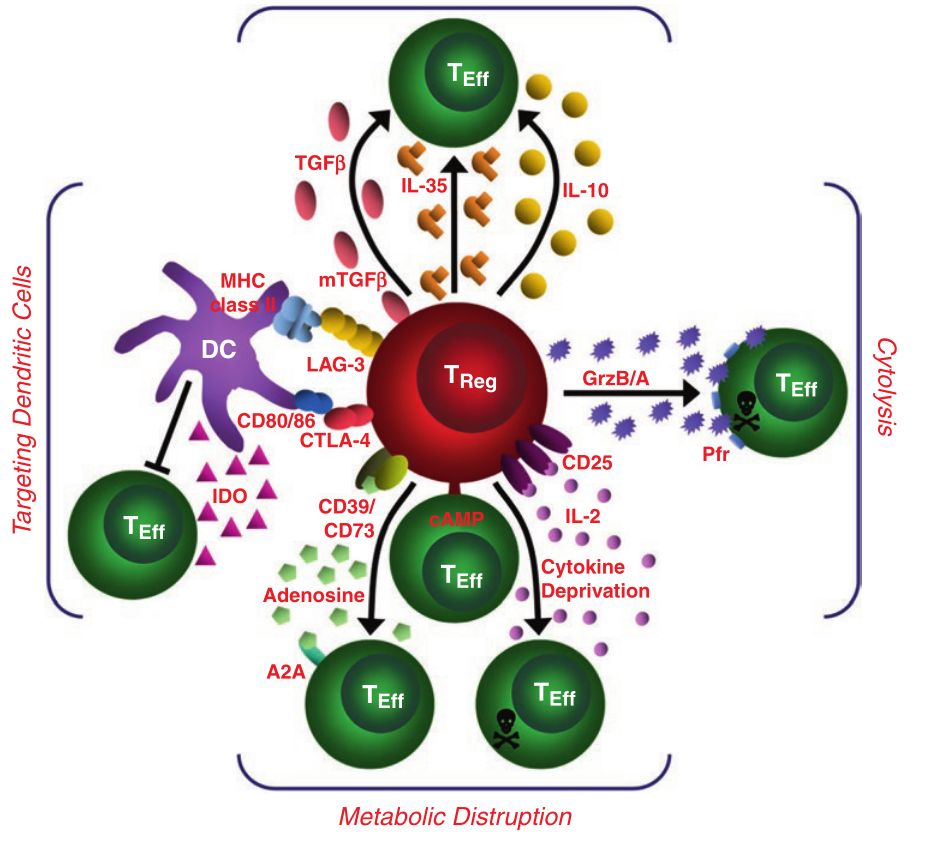
Fig8.5 Treg抑制机制。该示意图描述了四种不同模式的Treg抑制机制。
“抑制性细胞因子”包括IL-10、IL-35和TGF-β。
“细胞溶解”包括颗粒酶A和颗粒酶B依赖的杀伤机制和穿孔素依赖的杀伤机制。
“代谢紊乱”包括高亲和力IL-2受体α(CD25)依赖的细胞因子剥夺介导的细胞凋亡,环磷酸腺苷(cAMP)介导的抑制,以及CD39和/或CD73产生的腺嘌呤能腺苷受体(A2A)介导的免疫抑制。
“靶向树突状细胞”包括调节DC成熟或功能的机制,如LAG3(也称为CD223)-MHC-II介导的抑制DC成熟的机制,以及CTLA4-CD80/CD86介导的诱导DC吲哚胺2,3-双加氧酶(IDO)产生的机制,IDO是一种免疫抑制酶。
IL2:IL-2可能通过STAT5上调FOXP3的表达,增强Treg抑制功能。此外,Treg还可以通过其高亲和力的IL-2Rα受体(CD25R)通过消耗来剥夺局部的IL-2。
细胞因子分泌:IL-10和TGF-β参与nTreg和iTreg介导的抑制。
颗粒酶依赖性细胞溶解:人类Treg表达穿孔素和激活颗粒酶A后,可以杀死CD4+和CD8+T细胞和其他独立于Fas和FasL的细胞类型。
CD39和CD73介导的细胞外核苷酸代谢:CD73与CD39协同作用,从ATP产生腺苷(ADO)。CD39主要催化ATP转化为AMP,AMP被CD73降解生成腺苷。为了介导抑制,ADO与四个不同的ADAR之一(A1、A2A、A2B、A3)结合。A2A和A2B受体偶联到Gs亚基上,激活腺苷酸环化酶和蛋白激酶A(PKA),从而提高cAMP水平。先天免疫细胞和获得性免疫细胞与A2B和A2A的结合抑制了它们功能。
事实上,腺苷通过A2B受体影响APC(单核细胞和DC)的成熟及其促炎细胞因子的分泌,并通过诱导单核细胞分泌IL-10而促进免疫抑制环境的形成。
此外,腺苷可通过A2A受体降低NK细胞的细胞毒力,减少IFN-γ的分泌,促进免疫抑制细胞因子(IL-4和TGF-β)的分泌,抑制BCR诱导的NF-κB活化,降低效应T细胞的主要功能,如IL-2和IFN-γ的分泌、增殖和细胞溶解功能,并改变其存活率。腺苷通过这些途径共同影响了抗肿瘤免疫反应的效果。
CD39和CD73共同将ATP降解为腺苷,是Treg诱导细胞周围腺苷产生的一种机制。然而,虽然大多数研究报道CD39和CD73在小鼠Treg上共表达,但我们的工作表明,在人的外周血液、淋巴组织或乳腺肿瘤组织中,Treg从未在膜上或细胞质表达CD73。
与小鼠相似,在人类乳腺肿瘤中,Treg表达高水平的CD39。此外,TLR-7激活的pDC选择性地诱导Treg上CD39水平的上调(未发表的数据)。
然而,CD73可以在非Treg CD4+T细胞亚群上观察到,这些细胞能够在激活时增殖并分泌高水平的IFN-γ。
我们最近的数据显示CD39+TATreg与CD73+CD4+T细胞效应器协同介导腺苷的产生及其局部抑制功能,表明CD39/CD73轴是重要的Treg介导的抑制机制。
靶向DC:Treg表面组成性表达的CTLA-4,与其在DC上的配体CD80/CD86的相互作用是Treg介导其抑制功能的重要途径。
事实上,Treg在体外可下调或抑制DC上CD80和CD86的上调,阻断它们的共刺激功能和随后的T细胞激活。Treg上表达的Lag-3可能也会在Treg诱导的DC功能抑制中发挥作用,通过与未成熟DC表达的MHC-II类分子结合,诱导ITAM介导的抑制信号,阻止它们的成熟,损害它们的功能。
8.3 治疗策略
8.3.1 基于pDC/Treg相互作用的Treg中和策略
我们开发了一个临床相关的小鼠肿瘤模型,在该模型中,生长在WT宿主中的HER2/neu+NEU-15细胞系通过pDC和Treg介导的免疫替代逃避免疫监视,这与我们在人类乳腺癌中的观察结果非常相似(Fig.8.6)。
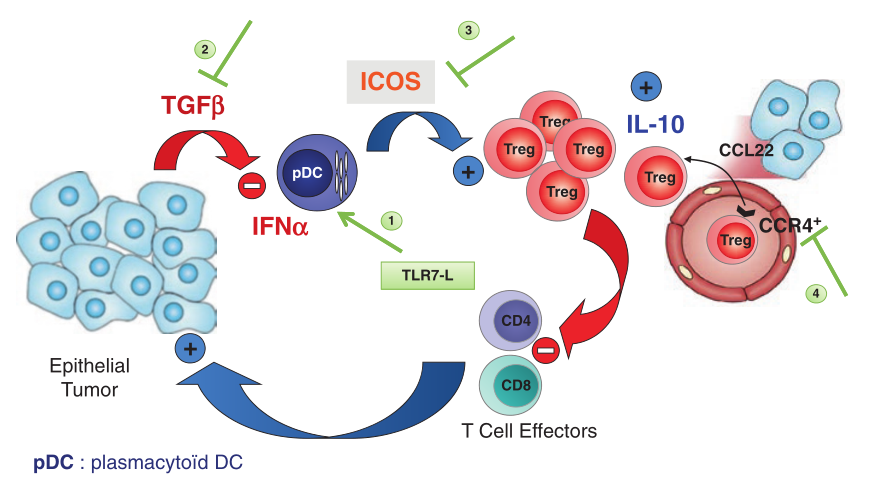
Fig 8.6 针对pDC/Treg相互作用的治疗策略。基于对PDC介导的Treg扩增的观察,我们提出了几种互补的方法来重新激活抗肿瘤免疫。(1)通过 TLR-7 配体对 pDC 进行再激活,促进其产生I 型 IFN ,目前有一项临床试验正在进行中;(2)TGF-β中和以恢复pDC功能,几种抗TGF-β受体或TGF-β的抗体,或TGF-β受体激酶结构域抑制剂目前也在临床试验中;(3)通过ICOS/ICOSL中和抗体阻断ICOS从而抑制Treg增殖;(4)中和CCL22/CCR4以阻断肿瘤内 Treg 募集,中和CCR4或小分子抑制剂目前正在临床试验和/或开发中。
8.3.1.1 TApDC的重新激活
通过TLR激动剂来重新激活TApDC并诱导其产生IFN-I的治疗策略可以减少Treg的扩增。
尽管它们对肿瘤进展有负面影响,但 TApDC 可以通过肿瘤内注射 TLR-7L 在体内重新激活,从而介导 Th1 特征反应和随后的肿瘤消除。TLR-7L 诱导长期保护性记忆反应,结果显示100% 治愈的小鼠受到保护免受随后的肿瘤攻击。
体内耗尽pDC会抑制TLR-7L的治疗活性,表明TApDC在TLR-7L介导的抗肿瘤反应中起关键作用。重要的是,我们证明了这种治疗活性是由局部诱导的,而不是全身性的I型干扰素介导的。这表明了肿瘤内TApDC重新激活的重要性,这将导致I型干扰素的产生,以及随后的附加功能,如抗原交叉提呈和Treg中和。
我们确实观察到I型干扰素中和导致了肿瘤内Th1信号的抑制。在此背景下,咪喹莫特(TLR7L)治疗皮肤癌导致TApDC募集和IFN-α的产生,这与局部免疫反应和肿瘤细胞的破坏相关。咪喹莫特的这种抗肿瘤活性依赖于颗粒酶B和/或TRAIL介导的TLR7激活的TApDC的直接肿瘤杀伤活性,从而导致随后的抗原捕获和交叉呈递。
基于文献结果,正在进行的I/II期临床试验目前正在评估TLR激动剂治疗各种类型癌症的治疗潜力。鉴于我们观察到TApDC对TLR-7L有反应,而对CpG ODN(TLR-9L)无反应,TLR-7激动剂对人乳腺肿瘤的治疗潜力是值得考虑的。
8.3.1.2 TGF-β中和
用免疫荧光法(IF)检测BDCA2 TApDC细胞核中磷酸化的Smad2蛋白在BDCA2 TApDC细胞核中的表达。这些观察结果表明,TApDC暴露于BT环境中时释放TGF-β,并提示Smad信号在TGF-β介导的TApDC抑制中发挥重要作用,就像已经在小鼠身上证明了的Smad3一样。
我们的研究确定TGF-β是恢复IFN-I生成的新靶点。因为(1)针对人pDC的TLR-9(CpG ODN)和TLR-7(咪喹莫特)配体目前正在肿瘤患者的免疫刺激临床试验中进行评估;(2)针对TGF-β或其受体信号转导的药物目前正在开发中,(3)pDC对于咪喹莫特通过产生干扰素-α和获得细胞毒特性而介导的黑色素瘤小鼠模型的抗肿瘤反应是必要的。
我们的结果表明,使用TGF-β拮抗剂结合TLR7/9激活来恢复TApDC产生的干扰素-I是一种有前景的局部BT治疗新策略。
此外,由于TGF-β也是推动FoxP3+iTreg由外周原始CD4+T细胞发展分化而来的因素之一,那么靶向TGF-β通路也将有助于减少Treg的产生。
8.3.1.3 Treg上的ICOS中和
ICOS是CD28分子超家族的成员,包括CTLA-4、PD-1或BTLA,它们都在免疫调节中发挥关键作用。基于我们的观察显示BT和滤泡性淋巴瘤中通过ICOS/ICOS-L相互作用扩增Treg,并在卵巢肿瘤中得到证实,我们正在将ICOS作为中和Treg的治疗靶点。然而,已有研究表明,抗CTLA-4拮抗剂抗体的某些作用直接归因于ICOS-ICOS-L相互作用的干扰。
此外,ICOS还表达在其他T细胞亚群上,如TFH细胞,这表明ICOS在它们的生物学中起着核心作用。Tfh 细胞通过在 B 细胞滤泡内为生发中心 B 细胞提供存活和分化信号,构成专门调节体液免疫的辅助 T 细胞亚群。ICOS在Treg和Tfh生物学和病理生理学中的重要性需要进一步探讨,以便考虑将ICOS作为使用中和抗体进行免疫治疗的潜在靶点。
此外,不同的抗ICOS激动剂单抗(JTX2011(#nct-02904226),GSK-3359609(#NXT-02723955))目前正在晚期实体肿瘤的I-IIa期临床试验中进行评估,单独或与抗PD-1联合治疗,以重新激活效应T细胞反应。
8.3.1.4 CD39/CD73轴
CD73 与 CD39 协同促使 ATP 转变为 Ado。几个团队已经使用小鼠肿瘤模型揭示了 Ado/CD73 在抑制抗肿瘤免疫和促进肿瘤发展中的关键作用 。
特别是通过三种不同的技术抑制CD73:(1)shRNAs,(2)小分子化学抑制剂(APCP),或(3)抗CD73单抗(Ty-23)通过诱导适应性免疫反应而阻断乳腺(T-3)和卵巢(ID8)小鼠肿瘤模型的生长。反应包括提高肿瘤特异性T细胞免疫力,改善抗肿瘤T细胞向肿瘤微环境的运输。
在小鼠肿瘤模型中也证明了Treg介导的部分免疫抑制功能依赖于CD73酶活性。在这一点上相一致的是,CD73缺陷的Treg在卵巢癌和淋巴瘤的小鼠模型中较少能够阻碍肿瘤特异性免疫和促进肿瘤生长。
此外,腺苷通过A2A受体能够有效地抑制内源性肿瘤免疫监视,A2A受体缺陷小鼠自发的抗肿瘤T细胞反应能够诱导T细胞依赖性的肿瘤排斥反应。
最后,结果还显示CD73的结构性中和(在CD73 APCP小鼠中)或瞬时中和(shRNA,抗体,APCP)与任何明显的免疫疾病无关。
总之,这些研究表明,干扰CD39/CD73/ADAR是逆转Treg介导的抑制的一种潜在策略。在这方面,两家公司(BMS,MedImmune)目前正在进行一期临床试验,用抗hCD73 mAb (BMS-986179 #NCT02754141, MEDI-9447# NCT02503774)与抗PD-1抗体联合进行治疗。
8.3.2 基于Treg靶向/耗尽的其他策略
8.3.2.1 阻断Treg细胞的诱导和募集
我们的研究表明,CCL22介导Treg向人卵巢和乳腺肿瘤的迁移,在免疫缺陷的小鼠异种移植模型中,阻断CCL22显著减少了Treg向卵巢肿瘤的迁移,导致在抗肿瘤效应T细胞存在的情况下发生抗肿瘤免疫反应。
趋化因子受体小分子拮抗剂(AF-399)或单抗(Mogalizumab)能够在体外阻断CCL22介导的人Treg和Th2细胞的募集,并已进入I期临床试验,用于晚期实体癌患者(肺癌、胃癌、食管癌和肾癌)单独或联合抗PD-1(#NCT02946671)的治疗。
8.3.2.2 Treg耗尽
化疗方案:节律剂量的环磷酰胺或紫杉醇可选择性降低Treg数量。
CD25表达细胞的耗竭:CD25仍然是Treg耗竭策略的主要靶点。在小鼠模型中,抗 CD25 mAb (PC61) 的消耗性给药可引起外周淋巴组织中的 Treg 强烈减少并诱导已形成的肿瘤的消退。
几种针对CD25的药物正在进行临床试验:
(1) 德尼罗金地塞米松(Denileukin Diftitox)(Ontak®,DAB389IL-2)是一种将白喉毒素活性区域与人IL-2融合的重组蛋白;
(2)Daclizumab(zentex®)和巴利昔单抗(Simect®)是抗人CD25单抗。
然而,由于CD25的非特异性表达,这种策略的主要风险是可能会清除肿瘤内存在的活化T细胞,这些T细胞有助于T细胞抗肿瘤免疫的启动。
抗CTLA-4耗竭性抗体:其他Treg受体也可以实现Treg靶向,其中,抗CTLA-4单抗的研究较多。BMS(MDX-100:易普利姆玛(药名)®/yervov®)和辉瑞/阿斯利康(CP675206:tremlimumab®)开发的两种完全人源化单抗已经在不同肿瘤类型的癌症患者中进行了临床试验。基于小鼠研究,提出IgG1同型(ADCC活性)的易普利姆玛(药名)的部分治疗活性是通过耗尽细胞表面CTLA4易位激活的Treg。这已经在黑色素瘤患者中的体外实验得到证实。
8.3.2.3 阻断Treg功能
TNFR家族:TNFR家族有几个成员(OX40、GITR、CD137等)。目前尚不清楚如何在不损害T效应功能的情况下阻断Treg功能。与抗CTLA-4类似,ADCC活性激动剂抗GITR单抗可诱导Treg耗竭,同时通过其激动剂活性诱导T效应器的激活。
通过TLR激动剂阻断Treg抑制功能:TLR-2信号(PAM2CSK4、PAM3CSK4、FSL-1)在体外和体内肿瘤模型中可降低Treg抑制功能。Treg介导的抑制在体外可以被TLR-8衍生信号抑制,而用CpG(TLR-9激动剂)在体内治疗黑色素瘤患者会导致Treg的数量降低。
结论
我们的工作强调了Treg/pDC相互作用在乳腺和卵巢肿瘤微环境中的重要性。肿瘤细胞在NK和巨噬细胞活化后分泌炎性细胞因子,通过CCR4和CCL22募集Treg。招募的 TATreg 随后被 TApDC 扩增,由于 TGF-β暴露和 smad2 在肿瘤环境中磷酸化,它们产生 IFN 的能力有缺陷。扩增的Treg表达上调的CD39,CD73在效应器细胞上的表达将通过腺苷的产生介导免疫抑制。这种抑制通路可能在导致肿瘤细胞死亡和ATP释放的化疗过程中特别相关。
这种pDC/Treg相互作用的途径确定了几个恢复抗肿瘤免疫的潜在靶点:(1)mAb中和CCL22/CCR4以阻断Treg在肿瘤内的重新募集;(2)pDC通过TLR-7配体重新激活以产生I型干扰素;(3)TGF-β中和以恢复pDC功能;以及(4)通过ICOS/ICOSL中和mAb中和ICOS以阻断Treg增殖。
— THE END —
V. Sisirak, I. Labidi-Galy, I. Le Mercier, N. Goutagny,
I. Puisieux, C. Ménétrier-Caux, and C. Caux
▉ 往期文章
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,主要是为了方便团队成员使用,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,大家需要的话也可以收藏使用~
20220501更新:整合了百度、谷歌、必应三大搜索引擎到检索工具中,方便作为主页使用~
网址是:dh.oncolab.cn

关注本号~

加入读者交流群~
本篇文章来源于微信公众号:OncoLab