9.1 引言
T细胞能识别体内主要组织相容性复合体(MHC)分子上的抗原,并且产生针对肿瘤的特异性反应,因此T细胞在癌症免疫治疗中具有重要作用。事实上,肿瘤浸润的细胞毒性CD8+T细胞和Th1极化的CD4+T细胞通常与较好的预后有关,但常规的T细胞并不是抗癌免疫的唯一介质。
尽管一些免疫细胞缺乏抗原肽的特异性受体,但仍能检测到肿瘤恶性转化的最早迹象。其中激活机体先天免疫细胞可即时提供保护,因此先天免疫细胞很可能在肿瘤的早期阶段发挥着关键作用。癌症的先天免疫监测涉及骨髓细胞,如巨噬细胞和中性粒细胞;携带T细胞受体(TCR)的非常规T细胞,如自然杀伤T(NKT)细胞和γδT细胞;以及一个不断增长的淋巴细胞家族,称为先天淋巴细胞(ILC)。
先天淋巴样细胞的特点是淋巴样形态、缺乏 RAG 重排的抗原特异性受体以及缺乏树突或髓系谱系的表面标志物。ILC包括具有共同来源的异质细胞群体。它们被分为杀伤(破坏)型和辅助型ILC(Fig. 9.1)。
自然杀伤(NK)细胞是ILC家族中最典型的细胞毒性细胞。杀伤型ILC具有与CD8+细胞毒性T细胞相似的细胞毒性颗粒和内容物。而辅助型ILC可以反映CD4+辅助T细胞的活性。
此外,根据ILC细胞因子的表达谱以及对特异性转录因子的需求,ILC可被分为3类。
第1类 ILC依赖于Th1细胞相关的转录因子T-bet,可以释放干扰素γ。这类细胞包括NK细胞和辅助型1型ILC1(ILC1),虽然NK细胞和ILC1在发育上是截然不同的,但它们有许多共同的表面标记,所以这两种先天细胞群体通常不易区分。除唾液腺ILC1外,NK细胞区别于ILC1的标志是转录因子Eomes的表达。
第2类ILC的发育和功能依赖于转录因子GATA3和RoRα,并可以释放2型细胞因子(主要是IL-5和IL-13)。
最后,第3类 ILC的发育和功能是根据它们产生IL-17和IL-22的能力以及它们对转录因子RoRγt的依赖性来判断的。
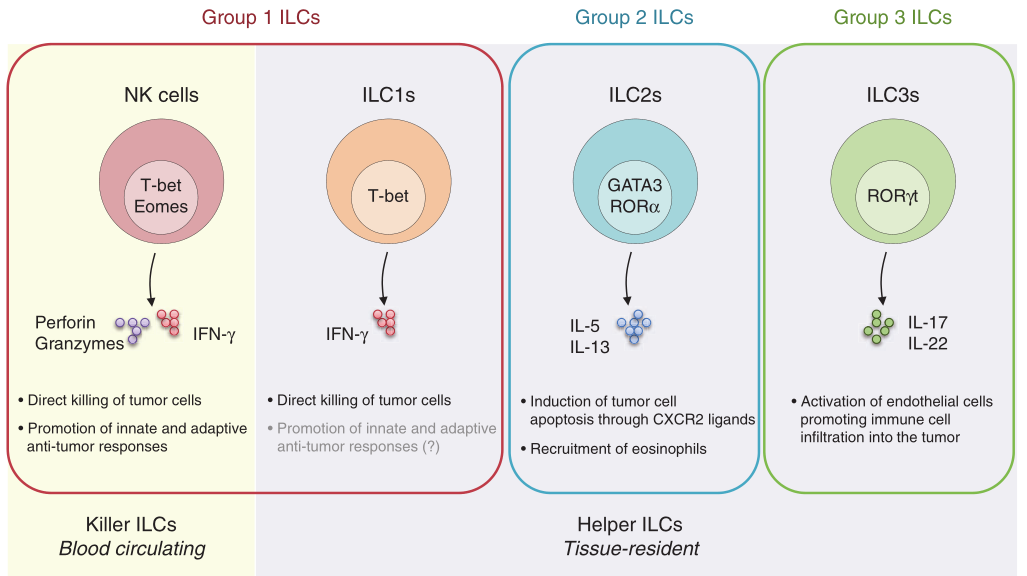
Fig. 9.1 ILC家族成员及其在癌症中的作用。ILC家族包括杀伤型ILC和辅助型ILC。ILC根据其标志性细胞因子和转录因子的依赖性被进一步分为三类。本文介绍了这三类ILC的主要特性以及它们的抗肿瘤活性。问号(?)指尚未表现出的可能的作用。NK 细胞直接杀死肿瘤细胞已得到充分证实,但只有少数研究通过裂解颗粒途径或在肝脏 ILC1 的情况下通过 TRAIL 描述了 ILC1 介导的细胞毒性。
NK细胞是第一个被发现的ILC亚群,最初被鉴定为具有自发的细胞毒活性。NK细胞通常被称为CD3阴性细胞,在人类中表达CD56,在小鼠中表达NK1.1,在两种物种中都表达NKp46。这种对NK细胞的表型定义同样适用于一些其他的ILC亚群。
此外,NK细胞还可以分为不同的亚型。在人类中,两个主要的NK细胞亚型是CD56brightCD16−NK细胞和CD56dimCD16+NK细胞,CD56brightCD16−NK细胞是重要的细胞因子生产者,在淋巴结中含量丰富;CD56dimCD16+NK细胞是血液中主要的NK细胞群,具有高细胞毒性。NK细胞耗竭抗体以及NK细胞缺陷的小鼠模型是证明NK细胞抗癌活性的基础(Table 9.1)。
NK细胞中许多表面受体能够区分癌变的细胞和正常细胞。此外,NK细胞不仅具有强大的细胞毒性功能,而且还是抗肿瘤细胞因子干扰素-γ的主要来源。这些特性使NK细胞在机体对癌症的先天免疫检测中起着至关重要的作用。然而,与大量关于癌症中 NK 细胞的报道完全相反,辅助型 ILC 可能的促肿瘤或抗肿瘤功能在很大程度上仍未得到探索。最近仍有研究表明组织中的1类ILC参与了自发性肿瘤的免疫监测。此外,其他各种报道也阐述了ILC2s和ILC3s的抑瘤活性。

Table 9.1 用于研究NK细胞功能的小鼠模型和耗竭抗体
在本章中,我们将回顾ILC检测恶性(肿瘤)细胞和预防癌症发展的不同机制。我们目前的认识大多局限于构成了典型的辅助型抗癌ILC亚群的NK细胞。因此本章我们将主要关注NK细胞,同时也会介绍有关ILC的最新研究。虽然目前已有相关研究证明辅助型ILC的促肿瘤和抗肿瘤活性,但在这里我们只讨论它们潜在的宿主保护功能。
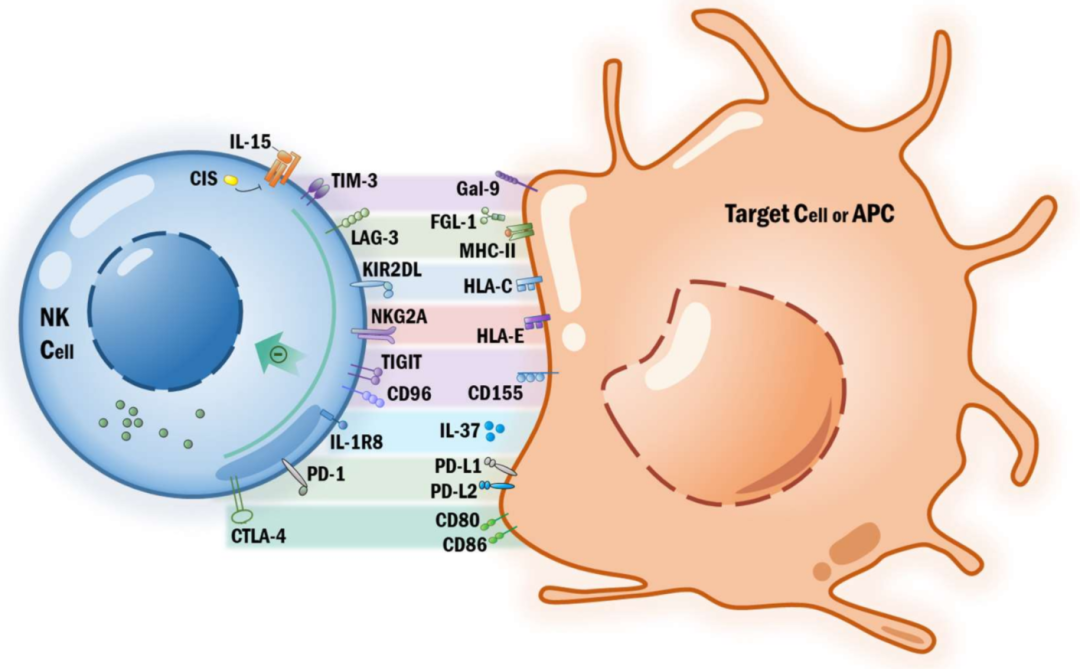
固有细胞表达一组固定的种系编码受体,这组受体可以识别外来、老化和受损的细胞,所以激活和抑制表面受体对于调节NK细胞的功能至关重要,其中一些受体也会在辅助型ILC亚群上表达(Fig. 9.2)。
此外,与辅助细胞(通常是单核细胞或树突状细胞(DC))的相互作用也能刺激NK细胞产生促炎因子并增强其杀伤功能。研究证明,NK细胞能够杀死下调MHC-I类分子(MHC-I)的肿瘤细胞,这一作用机制被称为“丢失自我”识别。
大多数细胞类型表面会表达自身多肽-MHC-I复合物,但大部分癌细胞的MHC-I表达会出现部分或全部丧失,这种MHC-I表达的部分或全部丧失现象通常是由CD8+T细胞介导的免疫反应引起的,它同时会使肿瘤细胞对NK细胞介导的细胞毒性作用变得更加敏感。而正常细胞不会引起NK细胞的自身反应,是因为在正常细胞表面表达的MHC-I分子会与抑制性NK细胞受体结合并传递负信号,从而避免NK细胞的自身反应。
除了“丢失自我”的识别外,检测受损细胞表面表达的自身配体也能提高NK细胞的杀伤能力。事实上,NK细胞与靶细胞相互作用的结果取决于NK细胞受体与靶细胞自身MHC-I结合传递的抑制信号和其识别靶细胞表面应激配体时传递的激活信号之间的平衡。
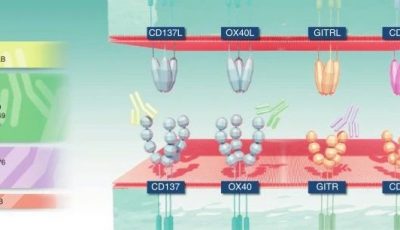
激活参与肿瘤免疫监视的NK细胞的受体包括固有细胞毒性受体(NCRs)、NKG2D(也称为CD314和KLRK1)和DNAM-1(也称为CD226);以及其他受体如低亲和力的激活受体FcγRIIIa(CD16)/共刺激分子CD137, OX40和GITR都具有强大的介导NK细胞激活的能力,因此很有希望将其运用于临床治疗的靶点。但现在仍没有任何相关报道能证明这些受体在新生肿瘤的早期检测中的作用,因此这里不再讨论。
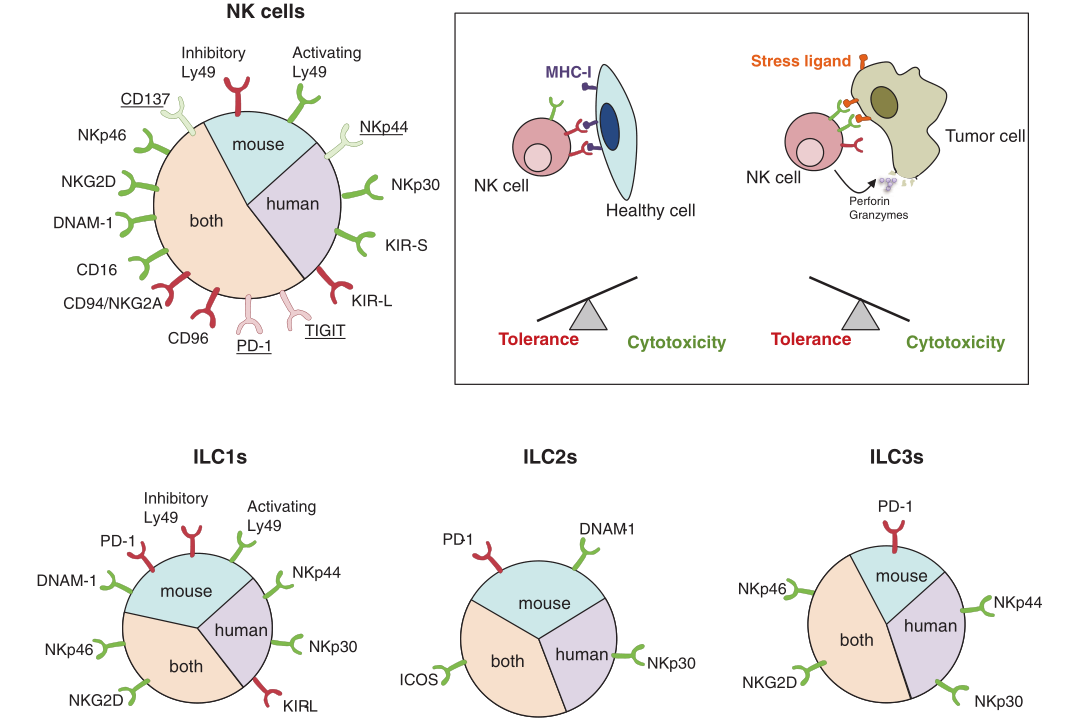
Fig. 9.2 细胞表面受体参与ILC识别肿瘤细胞。NK细胞表达一系列激活(绿色)或抑制(红色)细胞表面受体。有些受体只在激活的NK细胞上表达(下划线)。NK细胞与靶细胞相互作用的结果取决于激活和抑制信号之间的平衡。正常细胞可以表达与NK细胞抑制受体结合的MHC-I分子,而癌细胞可下调MHC-I分子和/或表达NK细胞激活受体识别的应激配体。激活信号超过抑制信号会导致NK细胞的激活和靶细胞的细胞毒性作用。最近研究发现DNAM-1和PD-1在小鼠ILCs上的表达,但尚未研究其在人ILC上的表达情况。
NCR家族有三个成员:NKp46(NCR1;CD335)在小鼠和人中都有表达,而NKp44(NCR2,CD336)和NKp30(NCR3;CD337)仅表达于人的NK细胞。与NKp46和NKp30不同的是,NKp44在静息NK细胞上检测不到,但在激活后的NK细胞上表达上调。
NCR参与触发NK细胞介导的细胞毒性和干扰素γ的分泌。重要的是,NCR的表达不仅仅限于NK细胞,在辅助型ILC1s、人类ILC2s以及名为NCR+ILC3s的ILC3s中也有表达,肿瘤细胞和肿瘤相关成纤维细胞结合NKp44可以刺激NCR+ILC3释放IL-8和TNF。同样,NKp30介导的人类肿瘤细胞的识别诱导ILC2中NF-κB信号通路的激活,从而促进IL-13和其他2型细胞因子的产生。但是,NCR对恶性细胞的辅助型ILC1识别的调控作用还有待证实。
目前仅有部分研究明确报道了肿瘤细胞上的NCR配体,其中包括NKp44L、HLA-B相关转录本3(BAT3)、B7-H6、硫酸乙酰肝素和增殖细胞核抗原(PCNA)。奇怪的是,PCNA不同于其他NCR配体,它通过抑制NK细胞功能来发挥作用。此外,NCR基因编码不同的剪接变体,其中一些是起免疫抑制作用的。
最近的研究表明,细胞因子定义的微环境可能会影响NK细胞中NKp30和NKp44亚型的表达谱,而基因编码的选择性剪接会导致抑制亚型的产生,从而抑制NK细胞的功能。
此外,在胃肠道间质瘤中,免疫抑制的NKp30c亚型的表达明显高于免疫刺激的NKp30a和NKp30b亚型的表达,并且与生存率降低相关。缺乏NKp46的小鼠可用于确定NKp46在体内控制肿瘤初始生长和在预防肿瘤转移中的作用。但由于缺乏NKp30和NKp44的小鼠同源物,其他NCR在肿瘤免疫监测中的体内研究受到限制。
NKG2D是主要NK细胞激活受体之一,某些T细胞亚群也表达NKG2D。NKG2D可识别几种与MHC相关的配体,这些配体在正常细胞表面表达很低,但在恶变细胞中表达较高。例如,在未转化的小鼠或人类细胞中,DNA损伤反应的激活会诱导NKG2D配体的上调,并增强细胞对NK细胞杀伤的敏感性。
小鼠中NKG2D配体是RAE-1α-ɛ、MULT1和H60a-c,在人类中则是MICA-B和ULBP1-6。NKG2D 参与刺激信号级联反应,导致细胞活化、杀伤和细胞因子产生。
一项开创性的研究表明,经过工程改造以表达高水平 NKG2D 配体并皮下注射到同系小鼠中的小鼠肿瘤细胞系被常规 NK 细胞迅速排斥,而无需 T 细胞和 B 细胞。将表达高水平NKG2D配体的小鼠肿瘤细胞系,皮下注射到同基因小鼠后,不需要T细胞和B细胞,NK细胞就能迅速排斥该肿瘤细胞系。
此外,在发生肿瘤和癌变的小鼠模型中都证实了NKG2D在肿瘤免疫监控中的关键作用。在小鼠B细胞中表达Epstein-Barr病毒转化蛋白LPM1导致B细胞淋巴瘤的模型中,淋巴瘤细胞表达NKG2D的配体,并在体外能被NK细胞杀伤。在这个模型中,T细胞是免疫监视的主要效应者。
在体内,淋巴瘤的发生可能涉及逃避NK细胞抗肿瘤活性作用的逃逸机制。事实上,肿瘤进展通常与免疫编辑过程有关,会出现对NK细胞活性有抵抗力的恶性克隆。多发性骨髓瘤从癌前阶段到恶性阶段的转变与肿瘤细胞表面的MICA脱落有关。该脱落过程除了降低肿瘤细胞上NKG2D配体的表面密度外,还会产生可溶性配体,下调免疫细胞上NKG2D的表达,进而促进肿瘤免疫逃逸。
事实上,长期暴露于表面的低亲和力NKG2D配体也会导致NK细胞对NKG2D依赖和非依赖途径的脱敏。令人惊讶的是,高亲和力的NKG2D配体和MULT1的脱落并没有阻止肿瘤细胞的识别,而是通过增强NK细胞效应器功能来促进肿瘤排斥反应。这提示MULT1可阻止NK细胞与肿瘤微环境中表达的低亲和力配体(如RAE-1)的免疫抑制作用,并恢复NK细胞的反应性。
DNAM-1是一种可与整合素LFA-1结合且表达在NK细胞和T细胞上的黏附分子,其参与维持溶细胞性突触的稳定。最初发现DNAM-1在细胞间黏附中起作用,可识别一类凝集素和凝集素样分子家族。
Nextin和Nextin样分子参与了广泛的生物学过程,它们显著调节T细胞、NK细胞和抗原提呈细胞的免疫功能。除了增强NK细胞黏附和细胞毒作用外,DNAM-1还能促进干扰素-γ的分泌。
此外,可以通过DNAM-1的表达区分小鼠体内的两个功能NK细胞亚群。与DNAM-1−NK细胞相比,DNAM-1+NK细胞能增强IL-15信号,产生更高水平的促炎细胞因子。
有趣的是,DNAM-1在小鼠肝脏ILC1上高水平表达,在早期ILC前体和小鼠骨髓中ILC2前体上也能检测到DNAM-1。然而,DNAM-1调节辅助型ILC功能的作用仍有待研究。
DNAM-1配体CD155(也称为PVR)和CD112(也称为Nectin-2、PRR2或PVRL2)通常在实体肿瘤和血液系统恶性肿瘤中过度表达。与上述介绍过的NKG2D配体类似,肿瘤细胞表达DNAM-1配体CD155似乎是由于复制压力导致的DNA损伤,这一途径依赖一种检测双链DNA断裂的酶ATM。
在Eμ-Myc小鼠淋巴瘤模型中进行的一项有趣的研究证实,DNA损伤反应诱导早期转化的B细胞上CD155的表达,从而导致部分依赖于DNAM-1的自发肿瘤消退。
DNAM-1在免疫监测中的作用在于可以诱导纤维肉瘤的发展,以及促进DNAM-1缺陷小鼠自发和可移植肿瘤的生长。
NK细胞表达的激活受体和抑制受体种类繁多,抑制受体可以防止NK细胞杀死正常的组织和抑制NK细胞对下调MHC-I类分子(MHC-I)的肿瘤细胞的杀伤作用(抑制了“丢失自我识别”)。
人类KIR家族的NK细胞受体和小鼠Ly49家族的NK细胞受体可直接识别MHC-Ia分子。此外,人类和鼠都可表达CD94/NKG2A异二聚体受体,CD94/NKG2A异二聚体与人的非典型MHC分子HLA-E和小鼠的Qa-1递呈的肽结合。
这些受体与MHC-I成功结合后会传递一种抑制信号,从而扰乱NK细胞的激活途径。例如,抑制性受体KIR2DL2参与阻止激活受体聚集和诱导肌动蛋白重塑,同时参与靶细胞回缩。
在关于小鼠肉瘤中LY49抑制受体水平降低和自发性B细胞淋巴瘤发病加速的相关报道中,体现了“丢失自我”识别在NK细胞介导的免疫监控中的重要性。到目前为止,NK细胞被认为是“丢失自我”识别中唯一的ILC亚群介体。虽然在其他ILC亚群的表面已经检测到Ly49受体,但是它们的功能还需要进一步评估。
在肿瘤微环境中,其他受体也可能参与调节ILC功能。免疫检查点分子CTLA-4和PD-1可以抑制NK细胞的活性并构成重要的临床靶点,但对于它们在癌症固有免疫检测中的作用仍知之甚少。
有趣的是,小鼠的辅助型ILC前体的特征是高表达的PD-1。此外,很少有成熟的ILC表达PD-1,但它们在激活时会上调PD-1,因此仍需要更多的研究来评估PD-1在肿瘤内ILC上的作用。
TIGIT和CD96与Nextin和Nectin样分子家族相互作用的受体能有效抑制NK细胞和T细胞功能,它们可以与CD155结合并抵消DNAM-1介导的NK细胞活化。TIGIT可抑制小鼠和人NK细胞介导的细胞毒性作用,CD96可减少小鼠NK细胞产生干扰素-γ。CD96基因缺陷的小鼠对实验性肺转移和癌变表现出很强的抵抗力,而TIGIT在NK细胞介导的癌症监测中的作用仍有待研究证明。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。
关注本号~

加入读者交流群~

加入知识星球~
用于OncoLab读者交流互助永久免费
本篇文章来源于微信公众号:OncoLab