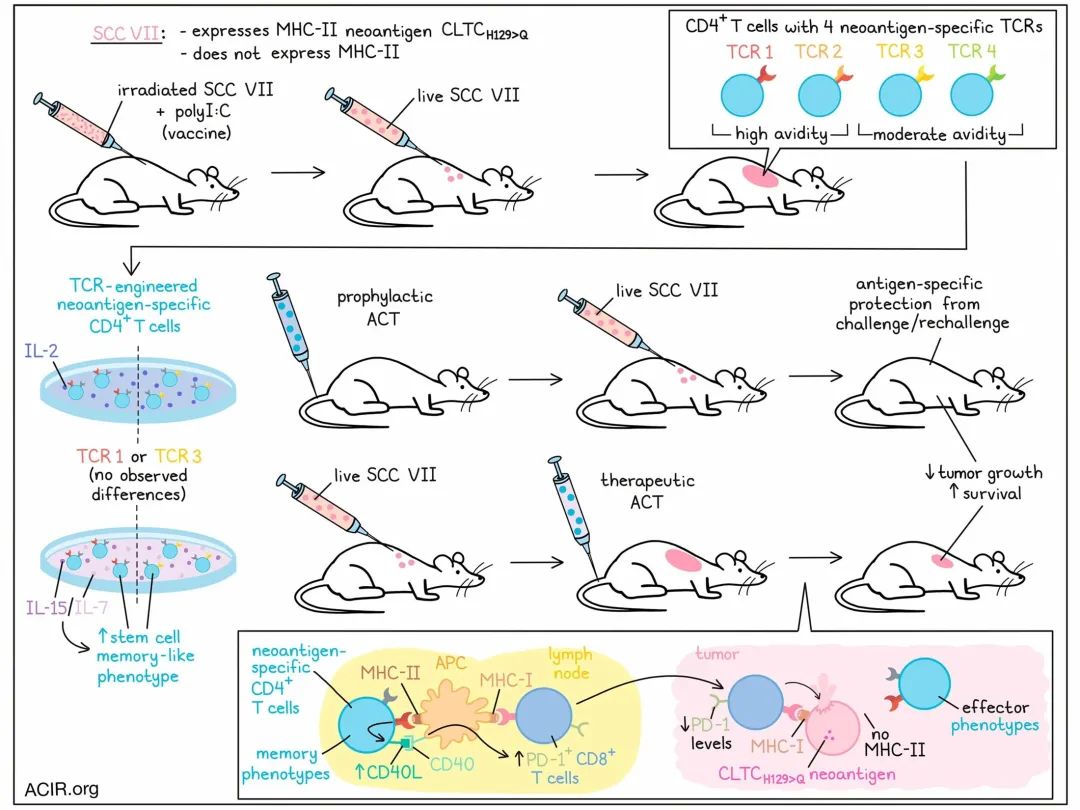
CD4+ T 细胞在抗癌免疫反应中的角色已得到广泛确认,然而其具体的作用机制以及影响其功能的因素仍待明确。在之前对小鼠的研究中,科学家们已经确认了特异性 CD4+ T 细胞对于 MHC-II 缺陷型鳞状细胞癌肿瘤模型(SCC VII)中表达的新抗原靶标 CLTCH129 > Q 的反应。为了深化这一研究,Brightman 等人近期识别出四种不同的 TCR 克隆型,这些克隆型可以以不同的亲和力识别该抗原靶标,并对 CLTCH129 > Q 特异性 CD4+ T 细胞在增强抗癌免疫反应中的潜力进行了评估和优化。这一研究成果已在《Nature Immunology》期刊中发表。
首先,Brightman等人使用小鼠接种辐照的SCC VII细胞和佐剂polyI:C,并保护其免受SCC VII活肿瘤攻击,以分离扩大的CLTCH129> Q特异性CD4+ T细胞池。接下来,他们从这些细胞中识别和验证了四种不同的 TCR 克隆型,由三种 TCR β 克隆型和四种 α 链克隆型组成。值得注意的是,TCR 1 和 TCR 2 共享相同的 TCR β 链,并且他们的 α 链也几乎相同,只有一个氨基酸的差异。另外,尽管与先前在 CD8+ T 细胞中的观察结果不同,TCR 1 和 TCR 2 的活性明显高于 TCR 3 和 TCR 4(约高出10倍),并且这一现象并未与 TCR 的近端信号传导差异相关。
为了研究 CLTCH129 > Q 特异性 CD4+ T 细胞在体内的扩增和活化,研究人员将相同数量的逆转录病毒转染标记表达 的TCR 1或 TCR 3的 CD4+ T 细胞转移到幼稚小鼠中。当随后用 SCC VII 攻击小鼠时,两个亚群都对抗原识别作出反应,两个亚群均发生扩增,表达相似水平的急性激活标志物 CD69,并以相似的程度上调 PD-1。
即使在炎症条件下,SCC VII也不表达MHC-II,表达TCR 1的活化CD4+ T细胞过继转移在1天后保护小鼠免受肿瘤攻击。这种保护是抗原特异性的,因为当小鼠被激活的多克隆非特异性CD4+ T细胞处理时,没有观察到同样的保护。在第一次攻击中被保护的小鼠在第30天也被保护免受再次攻击,这表明CLTCH129>Q特异性CD4+ T细胞介导持久的免疫记忆。这些结果取决于转移的细胞数量,因为与接受较高细胞剂量的小鼠相比,接受较低细胞剂量的小鼠的生存益处降低。
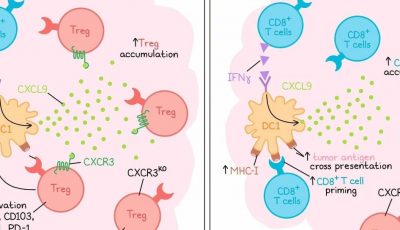
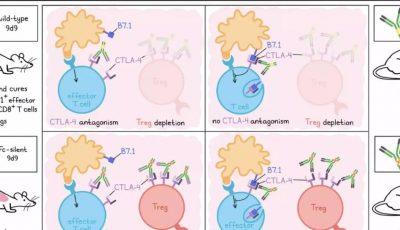
鉴于CLTCH129>Q特异性CD4+ T细胞由于SCC – VII肿瘤细胞缺乏MHC-II而不能直接识别肿瘤细胞上的新抗原,研究人员假设观察到的抗肿瘤作用可能是通过CD8+ T细胞的帮助介导的。事实上,在新抗原特异性CD4+ T细胞过继转移之前,CD8+ T细胞的清除使其保护作用失效。基于最近的证据,CD4+ T细胞通过CD40L依赖的cDC1s许可提供帮助,研究人员评估了表达TCR 1的CD4+ T细胞对CD40L表达的影响,发现在体外脾细胞识别肽段时上调。在体内,在肿瘤植入当天和2天后再次给予cd40l阻断抗体,消除了新抗原特异性CD4+ T细胞诱导的抗肿瘤免疫。同样,TCR1和TCR3之间没有差异。
接下来,Brightman等人研究了CLTCH129>Q特异性CD4+ T细胞对已经形成的较大肿瘤的潜在疗效。在这种情况下,新抗原特异性的CD4+ T细胞在tdLNs中增殖并浸润肿瘤,但未能提高生存率。为了提高它们的效力,研究人员尝试在转移前在IL-15和IL-7中培养细胞,而不是在标准的IL-2中培养细胞,因为在CD8+ T细胞的研究中,这种策略已被证明可以诱导分化程度较低的干细胞记忆样状态,并增强ACT。与IL-2培养的细胞相比,IL-15/IL-7培养的CLTCH129>Q -特异性CD4+ T细胞在外周血中有更大的扩增,在肿瘤和tdLNs中积累,并有效地延缓肿瘤生长和提高生存率。表达TCR 1和TCR 3的CD4+ T细胞之间的结果相似。
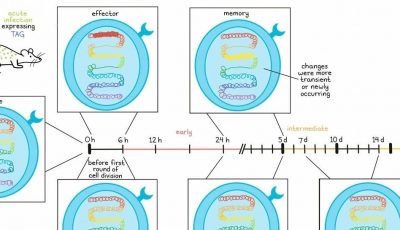
通过对不同位置CLTCH129>Q特异性CD4+ T细胞的基因表达分析,研究人员发现tdLNs中的细胞差异表达了记忆T细胞标记物,而肿瘤中的细胞差异表达了与效应功能相关的基因,包括TH1细胞因子、TCR信号通路成分和细胞毒性基因。与此相一致的是,流式细胞术显示,肿瘤细胞群主要包含效应记忆T细胞,而tdLNs包含各种记忆亚群,包括效应记忆、中央记忆和干细胞记忆样细胞群。值得注意的是,当细胞在IL-15/IL-7中培养时,观察到独特的记忆群体,而当细胞在IL-2中培养时则没有观察到。这些结果表明,淋巴结作为转移的TSCM细胞的储存库,产生更多分化的亚群,运输到肿瘤。
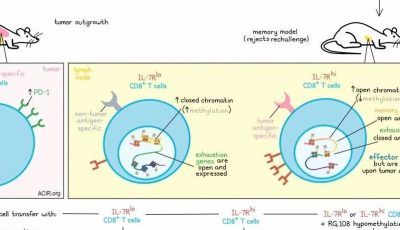
为了评估治疗性转移的CLTCH129>Q特异性CD4+ T细胞(在IL-15/IL-7中培养)对CD8+ T细胞免疫的影响,研究人员检测了PD-1的表达。虽然肿瘤中表达PD-1的宿主CD8+ T细胞的百分比没有变化,但PD-1的水平较低,表明终末衰竭减少。在tdLNs中,研究人员发现PD-1+CD8+ T细胞显著增加,这与转移的细胞数量相关,表明激活增加。当将CLTCH129>Q特异性CD4+ T细胞转移到CD8+ T细胞清除了的荷瘤小鼠体内时,观察到一些初步的抗肿瘤作用,但失去了较长期的肿瘤生长延迟。总之,这些结果表明,新抗原特异性的TSCM样CD4+ T细胞积极参与了tdLNs中肿瘤特异性CD8+ T细胞的启动。
总之,这些发现表明CLTCH129>Q特异性CD4+ T细胞通过CD40L诱导对SCC VII的抗肿瘤免疫,从而增强CD8+ T细胞的启动。无论TCR的密度如何,抗肿瘤作用都是明显的,并且可以通过在IL-15/IL-7混合物中培养工程化的新抗原特异性T细胞来增强,从而诱导干细胞记忆样表型,从而增强体内T细胞的扩增并诱导持久的肿瘤控制。
作者面对面
这周,第一作者Spencer Brightman和主要作者Stephen Schoenberger回答了我们的问题。
对你来说,这项研究最令人惊讶的发现是什么?
SB: 我们惊讶地发现,表达具有适度亲和力的T细胞受体的CD4+ T细胞,其功能与表达高亲和力受体的细胞在体内的扩展、抗肿瘤效能和表面标记表型方面相似。我们还惊讶地发现,治疗性转移的T细胞在转移后几天内在肿瘤引流淋巴结中保持了其干细胞样表型。
SS: 我已经研究了多年CD4+ T细胞对CD8+ T细胞的帮助机制,所以我对它也能调节新抗原特异性应答感到满足,而不是惊讶。然而,我确实感到惊讶的是,高亲和力和适度亲和力的CD4+ T细胞在效能上似乎没有太大区别,而且他们的治疗能力涉及到依赖CD8和独立于CD8的活动。
前景如何?
SB: 我们希望这些发现将通过增加对免疫治疗的兴趣来影响这个领域,这些免疫治疗除了集中在细胞毒性的CD8+ T细胞外,还关注CD4+ T细胞,而到目前为止,免疫治疗的主要焦点一直是CD8+ T细胞。进一步的研究应该确定通过采用类似干细胞的新抗原特异性CD4+ T细胞进行转移,对肿瘤微环境产生的广泛细胞和转录组改变。
SS: 啊,这就是有趣的地方!目前的细胞移植疗法涉及到针对肿瘤表达的单一靶标抗原的工程化T细胞,人们在患者中观察到,如果肿瘤丧失或修改其对那个抗原的表达,这种方法可能会变得无效。我们的工作显示,通过针对交叉呈递肿瘤抗原的抗原呈递细胞,可以实现有效的免疫治疗,这增强了激活而非杀伤。然后这些被激活的APC可以发动一支针对许多肿瘤抗原的细胞毒性CD8+ T细胞军队,而不仅仅是一个。我们现在已经准备好将这种方法应用到临床实践中,如果成功,这种方法可能会为免疫治疗提供新的方法。
你最近在工作之外学到的最酷的事情是什么?
SS:我最近成了一个“空巢老人”,一直在享受变化带来的所有机会:更多的旅行,更少的购物,更安静的生活。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab