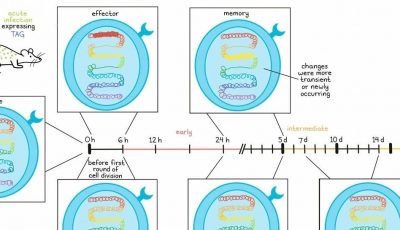
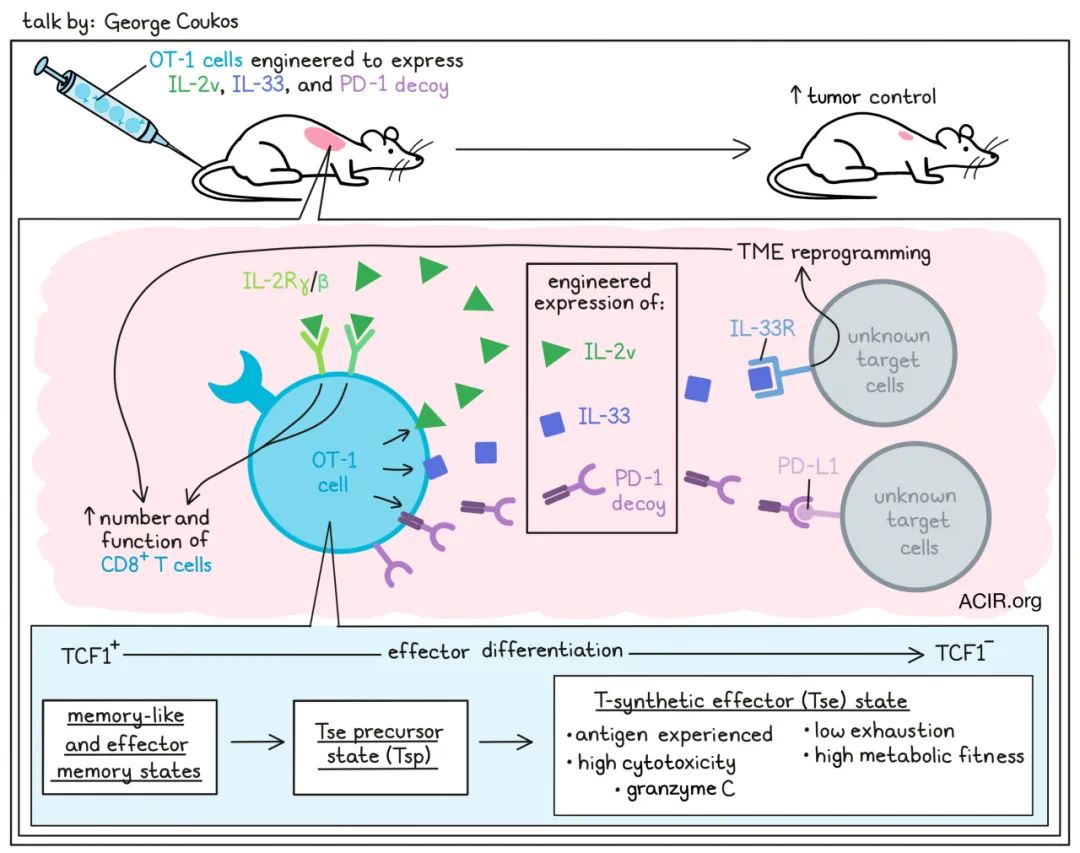
1. 借鉴自然免疫以创建合成免疫
George Coukos – 洛桑大学医院(CHUV)/联合国际癌症研究所(UNIL-Ludwig Institute for Cancer Research),瑞士洛桑
2. 肿瘤微环境驱动的GD2 CAR T细胞预防了非肿瘤靶向的细胞毒性
Kristen Vogt-纽约美国纪念斯隆·凯特琳癌症中心
3. Tebentafusp – 一种用于治疗转移性葡萄膜黑色素瘤的gp100定向TCR-CD3双特异性药物
Koustubh Ranade-美国洛克维尔Immunocore公司
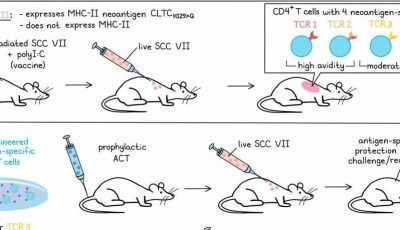
4. 探索T细胞受体以获取新的癌症免疫治疗靶点
Johanna Olweus – 奥斯陆大学医院,挪威奥斯陆

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab