杂志名称:Cell
发表日期:2024.03.11
DOI:10.1016/j.cell.2024.02.022.
PubMed:https://pubmed.ncbi.nlm.nih.gov/38490195/
影响因子:64.5
内容简介
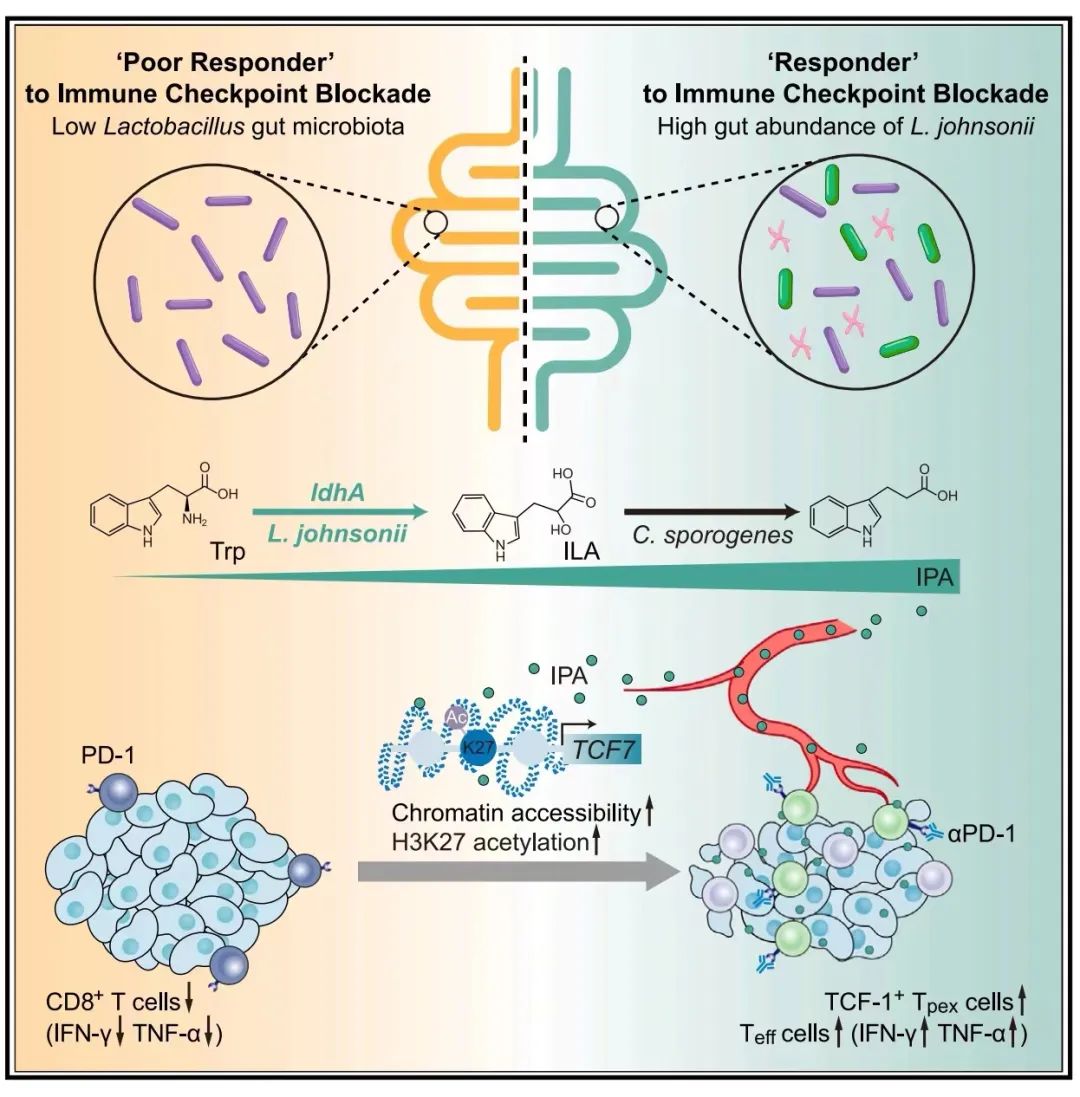
人类癌症中的免疫检查点阻断(ICB)反应与肠道菌群密切相关。我们的研究发现,共生乳杆菌Lactobacillus johnsonii的丰度与ICB的响应性正相关。补充Lactobacillus johnsonii或色氨酸衍生的代谢产物吲哚-3-丙酸(IPA)可以增强CD8+ T细胞介导的αPD-1免疫治疗的效果。从机制上讲,Lactobacillus johnsonii与Clostridium sporogenes协同作用产生IPA。IPA调节CD8+ T细胞的干性程序,并通过增加Tcf7超增强子区域的H3K27乙酰化,促进前体耗竭CD8+ T细胞(Tpex)的生成。IPA在泛癌症水平上改善ICB的响应性,包括黑色素瘤、乳腺癌和结直肠癌。总的来说,我们的发现识别了一条微生物代谢产物-免疫调节途径,并提出了一种潜在的基于微生物的辅助方法来提高免疫治疗的响应性。
创新性及研究意义
本研究提出了一种全新的免疫治疗策略,即通过调节T细胞干性来增强泛癌免疫治疗的效果。研究显示,肠道常住菌乳杆菌Lactobacillus johnsonii的丰富度与免疫检查点阻断(ICB)治疗的响应性正相关,且乳杆菌能与梭菌Clostridium sporogenes共同作用,生成色氨酸衍生的代谢产物吲哚-3-丙酸(IPA)。IPA能够调节CD8+ T细胞的干性编程,并通过增加Tcf7基因超级增强子区域的H3K27乙酰化,促进前体耗竭CD8+ T细胞(Tpex)的形成,从而在包括黑色素瘤、乳腺癌和结直肠癌在内的多种癌症中提高ICB的反应性。
这项研究的创新性在于揭示了微生物代谢产物在调控免疫反应中的关键角色,特别是在通过调节特定基因的表观遗传修饰来影响T细胞的功能。此外,研究还展示了微生物代谢产物IPA作为一种潜在的免疫疗法佐剂,可以在不同类型的癌症中增强ICB治疗的效果。这一发现不仅为肠道微生物与宿主免疫系统的相互作用提供了新的机制理解,也为临床上改善免疫治疗效果开辟了新的策略,具有重要的研究意义和应用前景。
数据图
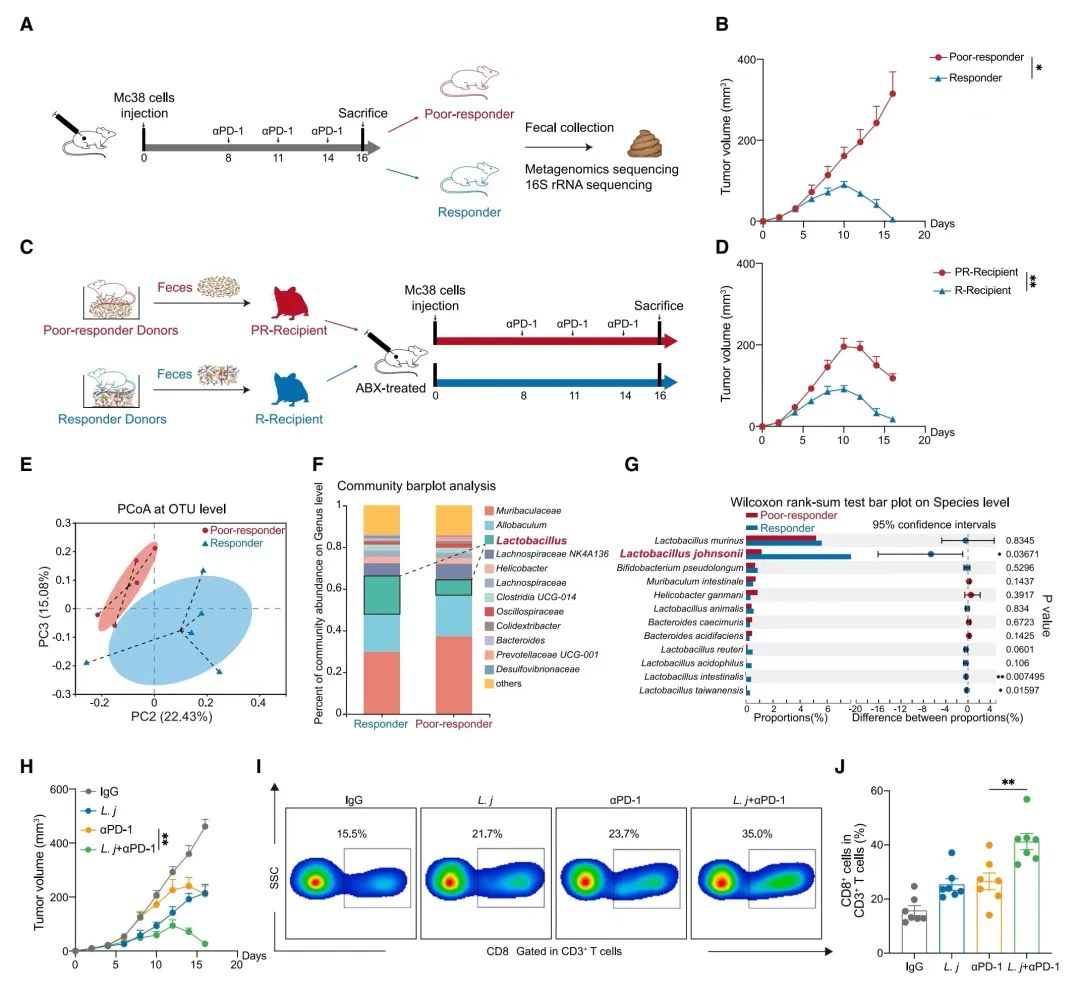
图 1. L. johnsonii 通过激活肿瘤浸润的CD8+ T细胞,增强抗PD-1免疫疗法的效果
(A)示意图展示了在皮下Mc38异种移植瘤模型中抗PD-1免疫疗法的过程。
(B)皮下Mc38肿瘤体积变化(单位:立方毫米),对比了对抗PD-1免疫疗法反应良好(响应者)和反应较差(低响应者)的小鼠。每组5只小鼠。
(C)示意图展示了粪便菌群移植的过程。
(D)接受了抗生素处理并移植了响应者菌群(R-接受者)或低响应者菌群(PR-接受者)的小鼠,其皮下Mc38肿瘤体积变化(单位:立方毫米)。每组6只小鼠。
(E)主坐标分析(PCoA)图表展示了在操作分类单元(OTU)水平上,响应者和低响应者小鼠的粪便样本的16S rRNA测序结果。每组5只小鼠。
(F)在属水平上,通过16S rRNA序列分析对响应者和低响应者小鼠的粪便样本进行的群落条形图分析。每组5只小鼠。
(G)在种水平上,对响应者和低响应者小鼠的粪便样本进行Wilcoxon秩和测试的条形图分析。每组5只小鼠。
(H)在接受了IgG同型对照抗体、抗PD-1抗体、L. johnsonii单独使用或与抗PD-1抗体联合使用的处理后,小鼠皮下Mc38肿瘤体积变化(单位:立方毫米)。每组7只小鼠。
(I 和 J)皮下Mc38肿瘤中CD8+ T细胞的频率。(I)展示了代表性的流式细胞术图,(J)展示了综合数据。每组7只小鼠。
(B)、(D)和(H)表示的是通过两因素方差分析并用Sidak的多重比较校正得出的均值 ± 标准误差。(G)表示的是通过Wilcoxon秩和测试得出的均值 ± 标准差,没有进行多重测试。(J)表示的是通过单因素方差分析并用Sidak的多重比较校正得出的均值 ± 标准误差。这些数据代表了三次独立实验的结果。16S rRNA是指16S核糖体RNA;L. j代表L. johnsonii。*p < 0.05, **p < 0.01。另见补充图1。
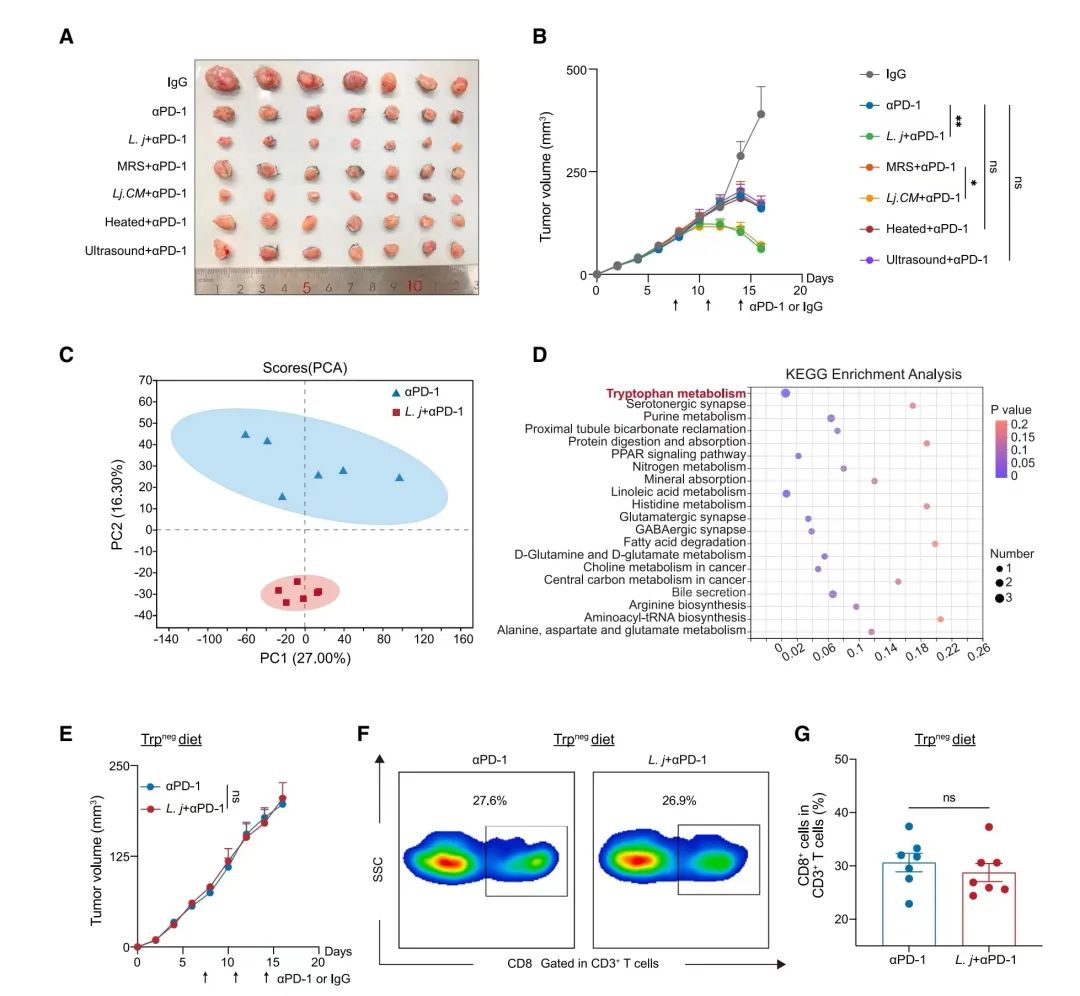
图 2. L. johnsonii 通过色氨酸代谢提升免疫检查点阻断(ICB)疗法的反应性
(A 和 B)(A)展示了处理不同条件下的小鼠皮下Mc38肿瘤的代表性图片,(B)则显示了这些肿瘤的体积变化(单位:立方毫米)。处理条件包括使用IgG对照抗体、抗PD-1抗体(aPD-1)、联合活L. johnsonii的抗PD-1抗体(L. j + aPD-1)、MRS培养基(MRS + aPD-1)、L. johnsonii条件培养基(Lj.CM + aPD-1)、热灭活L. johnsonii(加热 + aPD-1)以及超声波处理的L. johnsonii(超声 + aPD-1)。每组7只小鼠。
(C)主成分分析(PCA)显示了接受抗PD-1与同时接受L. johnsonii和抗PD-1处理的小鼠的血浆代谢物,这些代谢物由液相色谱-串联质谱(LC-MS/MS)鉴定。每组6只小鼠。
(D)通过京都基因与基因组百科全书(KEGG)途径分析对比了接受抗PD-1与同时接受L. johnsonii和抗PD-1处理的小鼠中不同富集的血浆代谢物。每组6只小鼠。
(E)在接受色氨酸缺乏(Trpneg)饮食的条件下,研究了小鼠接受抗PD-1抗体单独使用与联合L. johnsonii使用时皮下Mc38肿瘤的体积变化(单位:立方毫米)。每组7只小鼠。
(F 和 G)皮下Mc38肿瘤中CD8+ T细胞的频率。(F)展示了代表性的流式细胞术图,(G)则显示了综合数据。每组7只小鼠。
(B)和(E)的数据表示通过两因素方差分析并用Sidak的多重比较校正的均值 ± 标准误差。(G)的数据则通过未配对t检验分析的均值 ± 标准误差。这些数据代表了三次独立实验的结果。L. j代表L. johnsonii;MRS代表de Man, Rogosa和Sharpe培养基;CM代表条件培养基;Trpneg diet代表色氨酸缺乏饮食。ns表示无显著性,*p < 0.05, **p < 0.01。
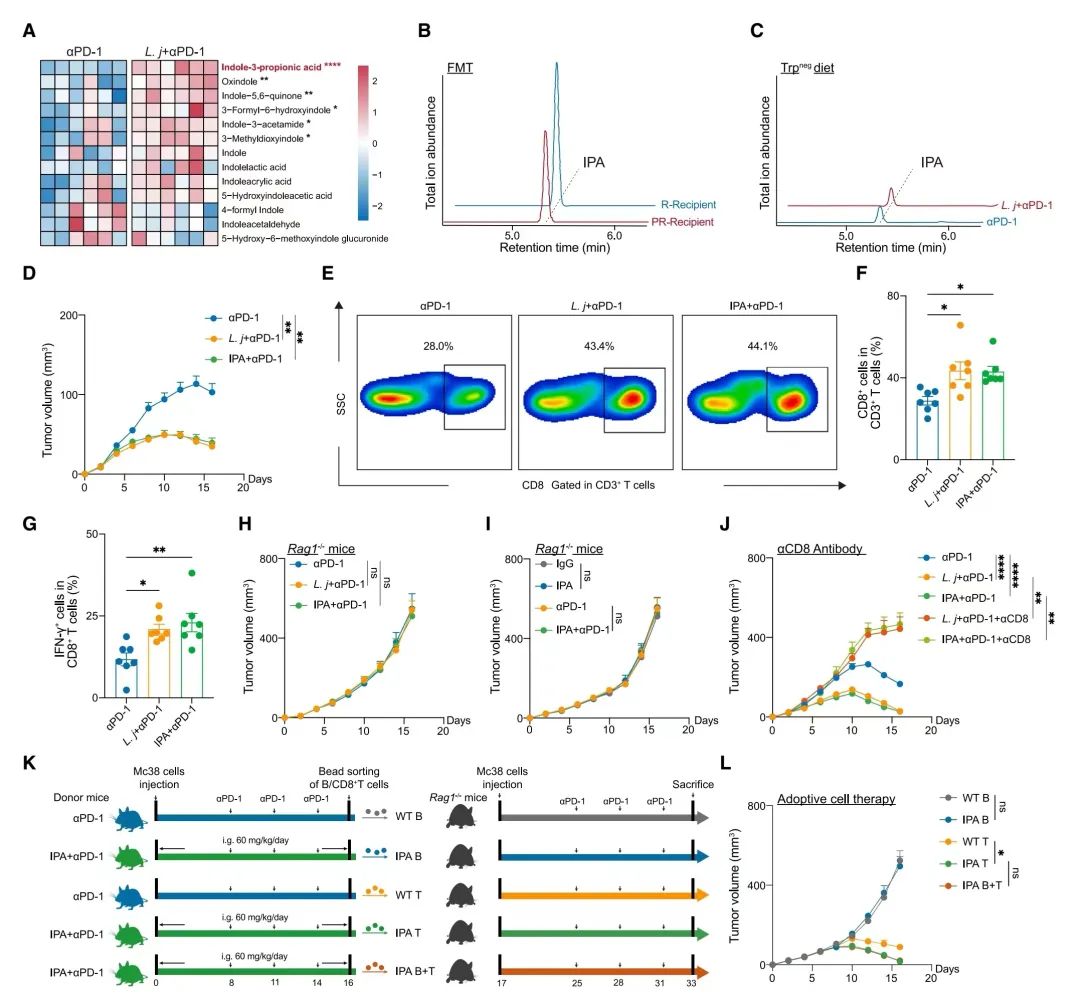
图 3. 来自L. johnsonii的IPA通过CD8+ T细胞提升ICB疗法的反应性
(A)热图显示了接受抗PD-1疗法单独或结合L. johnsonii治疗的小鼠中,与色氨酸相关的血浆代谢物的富集情况。每组6只小鼠。
(B)液相色谱-串联质谱(LC-MS/MS)用于确定接受响应者和低响应者菌群移植的小鼠血浆中IPA的含量。每组6只小鼠。
(C)液相色谱-串联质谱(LC-MS/MS)用于确定在接受色氨酸缺乏(Trpneg)饮食和抗PD-1疗法单独或结合L. johnsonii治疗的小鼠血浆中IPA的含量。每组7只小鼠。
(D)在接受抗PD-1疗法单独、结合L. johnsonii(L. j + aPD-1)或结合IPA(IPA + aPD-1)的治疗后,小鼠皮下Mc38肿瘤的体积变化(单位:立方毫米)。每组7只小鼠。
(E 和 F)皮下Mc38肿瘤中CD8+ T细胞的频率。(E)展示了代表性的流式细胞术图,(F)展示了综合数据。每组7只小鼠。
(G)通过流式细胞术分析皮下Mc38肿瘤中IFN-γ+ CD8+ T细胞的频率。每组7只小鼠。
(H)在Rag1−/−小鼠中,接受抗PD-1疗法单独或结合L. johnsonii或IPA的治疗后,皮下Mc38肿瘤的体积变化(单位:立方毫米)。每组6只小鼠。
(I)在Rag1−/−小鼠中,接受IgG同型对照抗体、抗PD-1、IPA单独或IPA和抗PD-1联合治疗后,皮下Mc38肿瘤的体积变化(单位:立方毫米)。每组5只小鼠。
(J)接受抗PD-1疗法单独或结合L. johnsonii或IPA的治疗,以及同时接受抗CD8和抗PD-1抗体以及L. johnsonii或IPA的治疗的小鼠,皮下Mc38肿瘤的体积变化(单位:立方毫米)。每组7只小鼠。
(K)示意图显示了异体细胞转移(ACT)的过程。供体小鼠接受抗PD-1疗法单独或结合IPA的治疗。来自供体小鼠的B细胞或(及)CD8+ T细胞根据显示转移到接受者小鼠(Rag1−/−)中。
(L)在接受者小鼠中,皮下Mc38肿瘤的体积变化(单位:立方毫米)。每组5只小鼠。
(D)、(H)-(J)和(L)的数据表示通过两因素方差分析并用Sidak的多重比较校正的均值 ± 标准误差。(F)和(G)的数据通过单因素方差分析并用Sidak的多重比较校正得出的均值 ± 标准误差。这些数据代表了三次独立实验的结果。L. j代表L. johnsonii;IPA代表吲哚-3-丙酸;FMT代表粪便菌群移植;Trpneg diet代表色氨酸缺乏饮食;ACT代表异体细胞转移;WT代表野生型。ns表示无显著性,*p < 0.05, **p < 0.01, ****p < 0.0001。另见补充图S2。
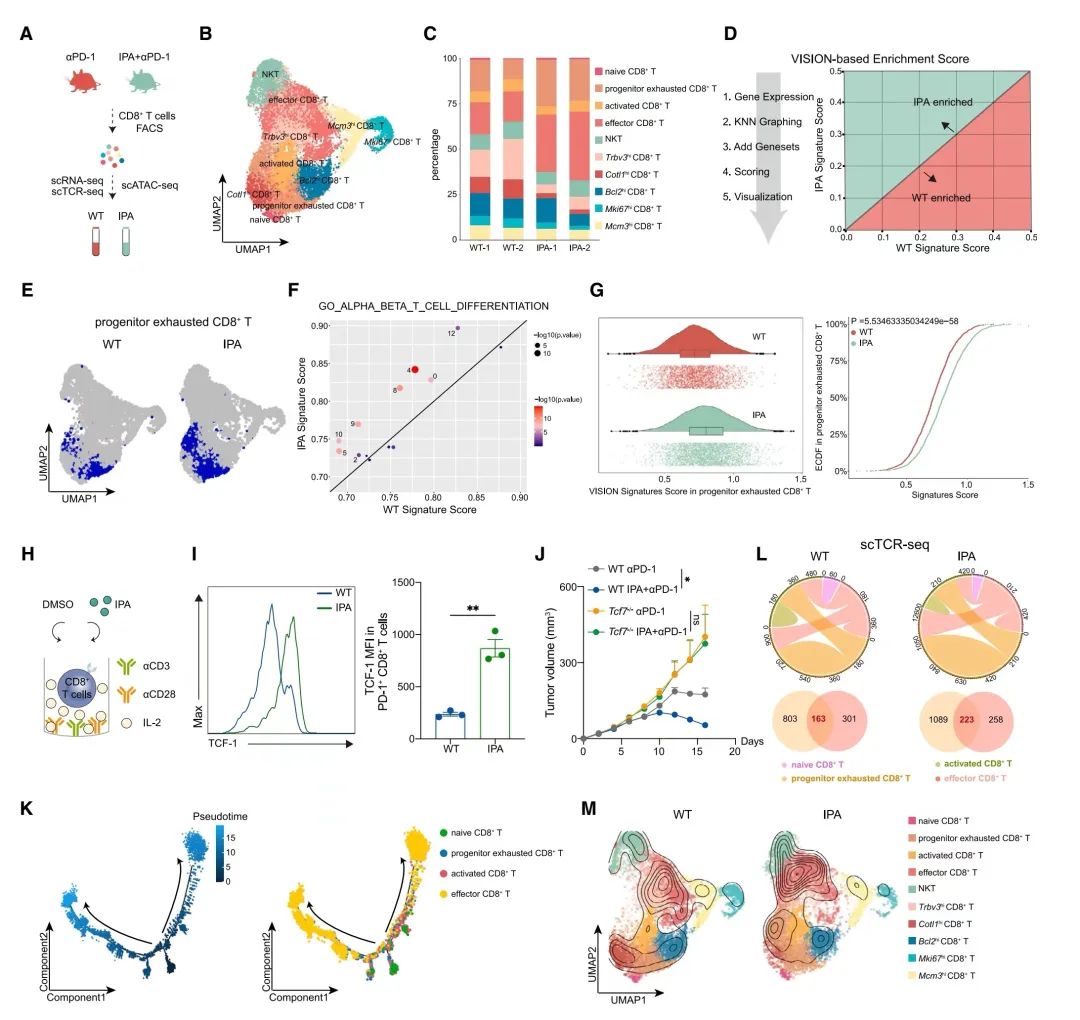
图 4. IPA通过促进Tpex细胞的活性来维持CD8+ T细胞的反应
(A)示意图展示了单细胞RNA测序(scRNA-seq)、单细胞TCR测序(scTCR-seq)和高通量测序用于靶向开放染色质的单细胞分析(scATAC-seq)的流程。
(B)单细胞RNA测序和UMAP聚类分析,用于从接受抗PD-1和同时接受抗PD-1及IPA处理的小鼠中分类后的CD8+ T细胞。
(C)堆叠条形图显示了在接受抗PD-1(WT, n = 2)和同时接受抗PD-1及IPA(IPA, n = 2)处理的小鼠中,每种识别出的细胞类型在CD8+ T细胞中的百分比。
(D)示意图展示了基于VISION的分析流程。
(E)代表性的UMAP图显示了在WT和IPA小鼠中,前体耗竭CD8+ T细胞(以蓝色突出显示)的分布。
(F)散点图显示了在WT(n = 2)和IPA(n = 2)小鼠中,每个细胞群集的GO_ALPHA_BETA_T_CELL_DIFFERENTIATION基因集的平均签名得分。
(G)小提琴图(左)和ECDF图(右)展示了WT和IPA小鼠中前体耗竭CD8+ T细胞群集的VISION富集得分,针对GO_ALPHA_BETA_T_CELL_DIFFERENTIATION基因集。
(H)示意图展示了CD8+ T细胞的体外培养过程。
(I)代表性直方图(左)和结合的平均荧光强度(MFI)(右)展示了用流式细胞术测量的经DMSO或IPA处理的PD-1+ CD8+ T细胞中TCF-1的表达。CD8+ T细胞从小鼠的淋巴结或脾脏中纯化。
(J)Tcf7−/−小鼠及其WT同窝控制小鼠的肿瘤体积变化(单位:立方毫米),两种小鼠均接受了抗PD-1单独或与IPA结合的处理。每组5只小鼠。
(K)通过monocle 2在二维状态空间定义的CD8+ T细胞的假时间轨迹,颜色深浅表示假时间(左),颜色代表不同的识别出的T细胞亚群(右)。
(L)互连和弦图显示了在WT和经IPA处理的样本中CD8+ T细胞亚群共享的TCRs(顶部),以及在WT和经IPA处理的样本中前体耗竭CD8+ T细胞亚群与效应CD8+ T细胞亚群之间共享相同的CDR3(配对的TCRα和TCRβ链)氨基酸序列的数量的韦恩图(底部)。
(M)WT和经IPA处理的样本中,跨CD8+ T细胞亚群的克隆密度图。UMAPs为标记的T细胞亚群簇进行了颜色编码。
(G)的数据通过Wilcoxon秩和测试分析VISION富集得分。(I)的数据表示通过未配对t检验分析的均值 ± 标准误差。(J)的数据通过两因素方差分析并
用Sidak的多重比较校正得出的均值 ± 标准误差。这些数据代表了三次独立实验或生物重复。ECDF代表经验累积分布函数;IPA代表吲哚-3-丙酸;UMAP代表均匀流形逼近和投影;WT代表野生型。ns表示无显著性差异,*p < 0.05, **p < 0.01。另见图S3和S4。
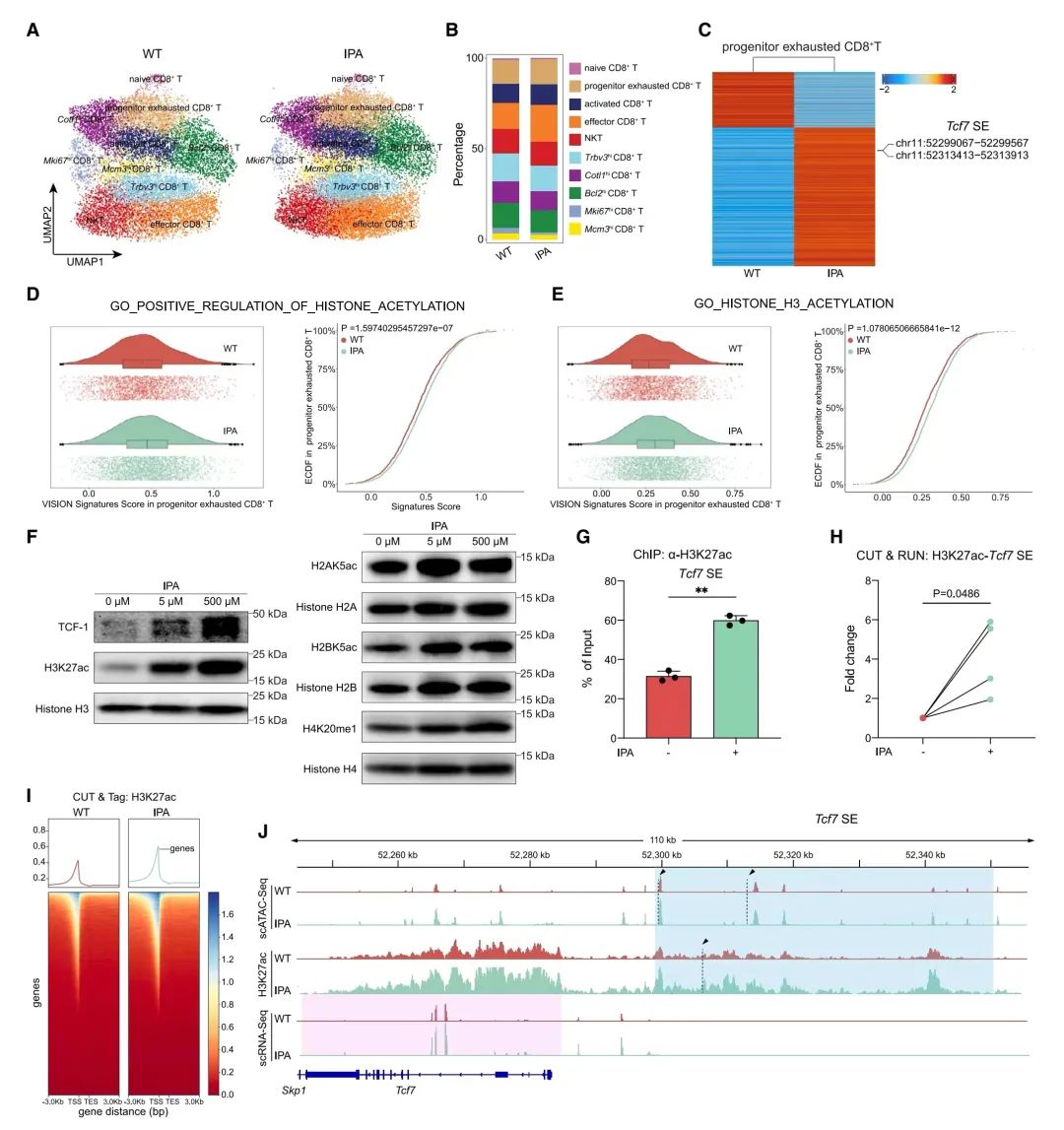
图 5. IPA通过调整Tcf7基因超级增强子区域的H3K27乙酰化激活Tpex细胞
(A)单细胞ATAC测序(scATAC-seq)和UMAP聚类分析,用于从接受抗PD-1(WT)和同时接受抗PD-1及IPA(IPA)处理的小鼠中分类后的CD8+ T细胞。
(B)堆叠条形图显示了在WT(n = 2)和IPA(n = 2)处理的小鼠中,每种识别出的细胞类型在CD8+ T细胞中的百分比。
(C)热图显示了在WT(n = 2)和IPA(n = 2)小鼠中,前体耗竭CD8+ T细胞群集的不同染色质可访问性峰位置。
(D)小提琴图(左)和ECDF图(右)展示了WT和IPA小鼠中前体耗竭CD8+ T细胞群集的“GO_POSITIVE_REGULATION_OF_HISTONE_ACETYLATION”基因集的VISION富集得分。
(E)小提琴图(左)和ECDF图(右)展示了WT和IPA小鼠中前体耗竭CD8+ T细胞群集的“GO_HISTONE_H3_ACETYLATION”基因集的VISION富集得分。
(F)通过Western blot分析,检测了与IPA共培养或未共培养的CD8+ T细胞中TCF-1、H2AK5ac、H2BK5ac、H3K27ac、H4K20me1、组蛋白H2A、H2B、H3和H4的表达(浓度分别为0, 5, 500 mM)。
(G)ChIP-qPCR方法检测了与IPA共培养或未共培养的CD8+ T细胞中Tcf7基因超级增强子位点的H3K27乙酰化情况。每组3个生物重复。
(H)CUT&RUN-qPCR方法检测了与IPA共培养或未共培养的CD8+ T细胞中Tcf7基因超级增强子位点的H3K27乙酰化情况。每组4个生物重复。
(I)CUT&Tag测序分析了与IPA共培养或未共培养的CD8+ T细胞中的H3K27乙酰化情况,乙酰化峰值在上层面板显示。每组6个生物重复。
(J)通过单细胞ATAC测序(scATAC-seq,每组2个重复)、H3K27ac测序(每组6个重复)或单细胞RNA测序(scRNA-seq,每组2个重复)分析,在指定条件下Tcf7基因位点的基因组结合模式的代表性插图。黑色虚线表示强度有差异的峰。Tcf7基因区域以粉色突出显示,超级增强子区域以蓝色突出显示。
(D)和(E)的数据通过Wilcoxon秩和测试分析VISION富集得分。(G)的数据表示通过双尾比率配对t检验分析的均值 ± 标准差。(H)的数据通过双尾比率配对t检验分析CUT&RUN-qPCR。这些数据代表了3至6次独立实验或生物重复。IPA代表吲哚-3-丙酸;SE代表超级增强子。***p < 0.001。另见图S5。
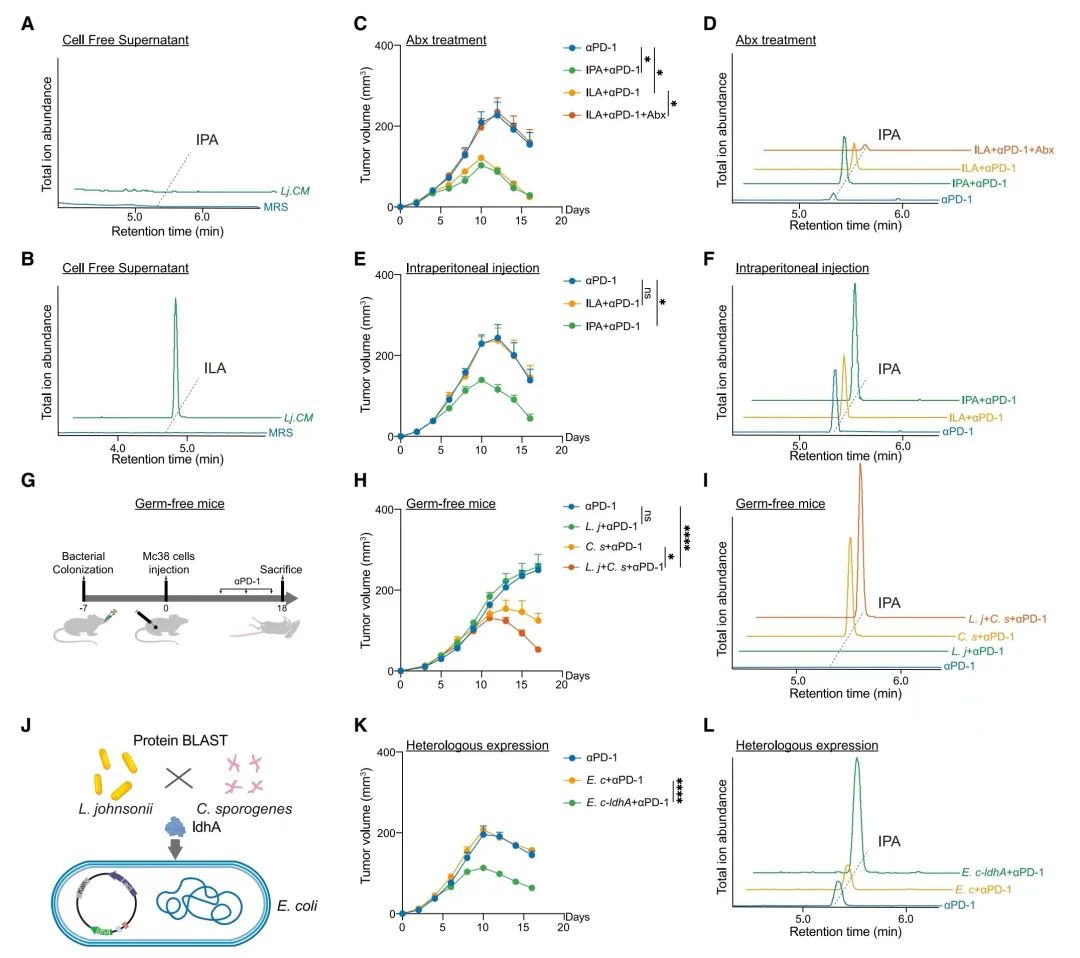
图 6. L. johnsonii 与 C. sporogenes 共同作用产生IPA
(A)通过液相色谱-串联质谱(LC-MS/MS)检测MRS培养基和L. johnsonii条件培养基(Lj. CM)上清液中的IPA。n = 6次独立实验。
(B)通过LC-MS/MS检测MRS培养基和Lj.CM上清液中的吲哚-3-乳酸(ILA)。n = 6次独立实验。
(C)皮下Mc38肿瘤体积变化(单位:立方毫米),小鼠接受抗PD-1治疗,抗PD-1联合IPA或ILA治疗,或抗PD-1联合ILA和抗生素(Abx)治疗。n = 6只小鼠每组。
(D)通过LC-MS/MS检测接受上述指定治疗的小鼠血浆中的IPA。n = 6只小鼠每组。
(E)通过腹腔注射,小鼠接受抗PD-1或抗PD-1联合ILA或IPA治疗后的皮下Mc38肿瘤体积变化(单位:立方毫米)。n = 6只小鼠每组。
(F)通过LC-MS/MS检测接受上述指定治疗的小鼠血浆中的IPA。n = 6只小鼠每组。
(G)示意图展示了在无菌小鼠上进行抗PD-1免疫治疗的过程。
(H)在单独定植L. johnsonii或(和)C. sporogenes的无菌小鼠中,接受抗PD-1治疗后的皮下Mc38肿瘤体积变化(单位:立方毫米)。n = 7只小鼠每组。
(I)通过LC-MS/MS检测接受上述指定治疗的无菌小鼠血浆中的IPA。n = 7只小鼠每组。
(J)示意图展示了蛋白质BLAST分析和在大肠杆菌中过表达ldhA基因的过程。
(K)小鼠接受抗PD-1,或抗PD-1联合大肠杆菌或工程大肠杆菌(E. c-ldhA)治疗后的皮下Mc38肿瘤体积变化(单位:立方毫米)。n = 7只小鼠每组。
(L)通过LC-MS/MS检测接受上述指定治疗的小鼠血浆中的IPA。n = 7只小鼠每组。
(C)、(E)、(H)和(K)的数据表示通过两因素方差分析并用Sidak的多重比较校正得出的均值 ± 标准误差。这些数据代表了三次独立实验。ILA代表吲哚-3-乳酸;IPA代表吲哚-3-丙酸;Abx代表抗生素;L. j代表L. johnsonii;C. s代表C. sporogenes。ns表示无显著性,*p < 0.05, ****p < 0.0001。另见图S6。
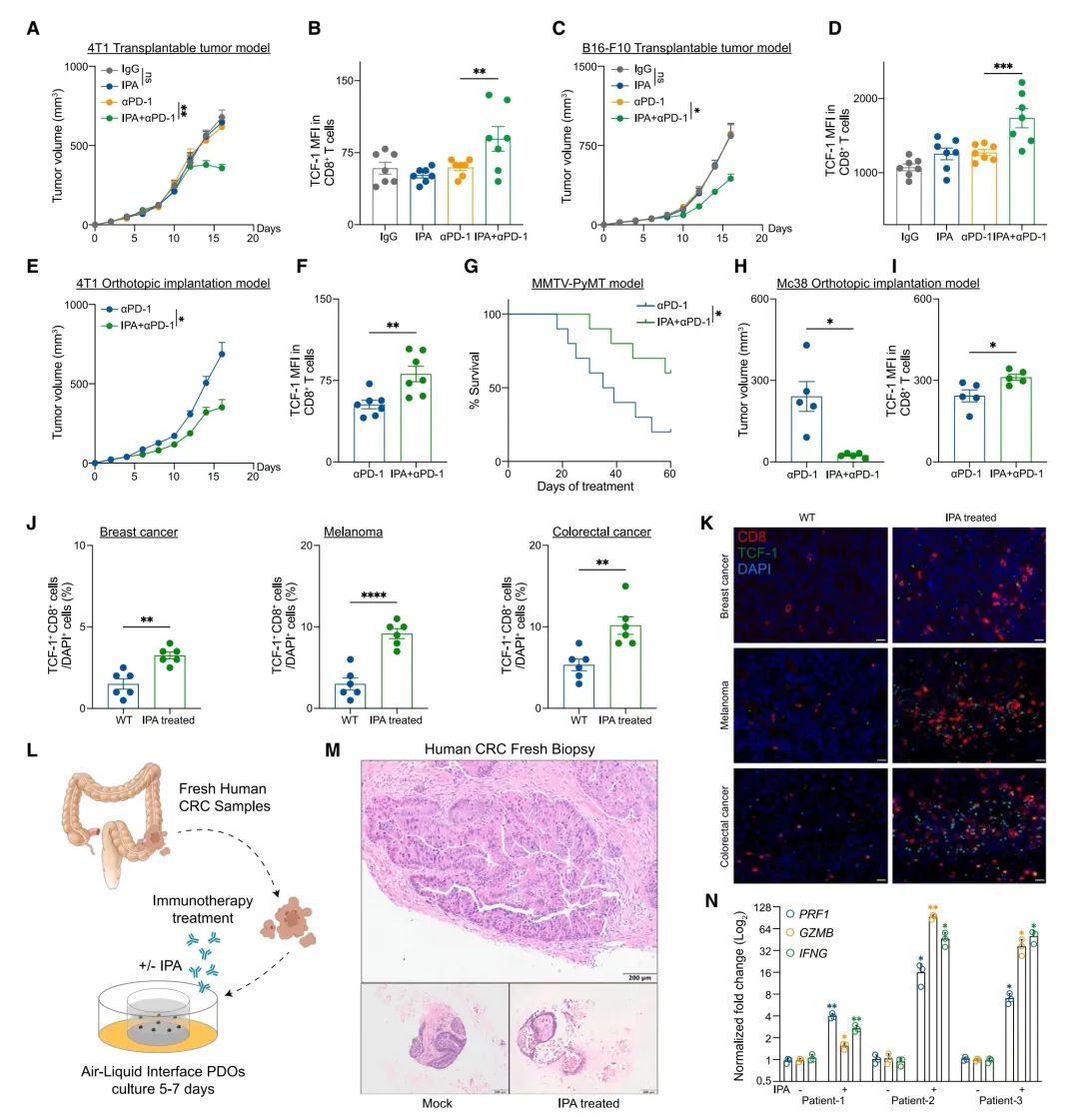
图 7. IPA在多种癌症和结直肠癌来源的类器官体中提高ICB疗法的反应性
(A)接受IgG同型对照、IPA、抗PD-1或同时接受IPA和抗PD-1治疗的小鼠,其可移植4T1乳腺肿瘤的体积变化(单位:立方毫米)。n = 7只小鼠每组。
(B)流式细胞术分析从4T1乳腺肿瘤中分离的CD8+ T细胞中TCF-1的平均荧光强度(MFI)。n = 7只小鼠每组。
(C)接受IgG同型对照、IPA、抗PD-1或同时接受IPA和抗PD-1治疗的小鼠,其可移植B16-F10黑色素瘤的体积变化(单位:立方毫米)。n = 7只小鼠每组。
(D)流式细胞术分析从B16-F10黑色素瘤中分离的CD8+ T细胞中TCF-1的平均荧光强度(MFI)。n = 7只小鼠每组。
(E)接受抗PD-1或与IPA联合治疗的小鼠,其4T1原位乳腺肿瘤的体积变化(单位:立方毫米)。n = 7只小鼠每组。
(F)流式细胞术分析从4T1原位乳腺肿瘤中分离的CD8+ T细胞中TCF-1的平均荧光强度(MFI)。n = 7只小鼠每组。
(G)接受抗PD-1或与IPA联合治疗的MMTV-PyMT小鼠的生存曲线。n = 10只小鼠每组。
(H)接受抗PD-1或与IPA联合治疗的小鼠,其Mc38原位肿瘤的体积变化(单位:立方毫米)。n = 5只小鼠每组。
(I)流式细胞术分析从Mc38原位肿瘤中分离的CD8+ T细胞中TCF-1的平均荧光强度(MFI)。n = 5只小鼠每组。
(J)两组小鼠中,乳腺癌、黑色素瘤和结直肠癌中TCF-1+ CD8+细胞与DAPI+细胞的频率。n = 6只小鼠每组。
(K)代表性图像显示接受IPA治疗与否的小鼠中乳腺癌、黑色素瘤和结直肠癌样本的免疫荧光染色,CD8(红色)、TCF-1(绿色)和DAPI(蓝色)(标尺,20毫米)。n = 6只小鼠每组。
(L)示意图展示空气-液体界面结直肠癌PDO(患者衍生的类器官体)的制备过程。
(M)新鲜人类结直肠癌活检的H&E染色(上图,标尺,200毫米)以及治疗后PDO的H&E染色(下图,标尺,200毫米)。n = 5位患者。
(N)空气-液体界面PDO在接受IPA治疗与否的条件下,PRF1、GZMB和IFNG表达的qPCR分析。n = 3位患者。
(A)、(C)和(E)的数据表示通过两因素方差分析并用Sidak的多重比较校正的均值 ± 标准误差。(B)和(D)的数据通过单因素方差分析并用Sidak的多重比较校正得出的均值 ± 标准误差。(F)、(I)和(J)的数据通过未配对t检验得出的均值 ± 标准误差。(G)的生存曲线通过对数秩检验分析。(H)的数据通过未配对t检验并应用Welch的校正得出的均值 ± 标准误差。(N)的数据表示通过双尾比率配对t检验的均值 ± 标准差。这些数据代表了三次独立实验。IPA代表吲哚-3-丙酸;CRC代表结直肠癌。ns表示无显著性差异,*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S7。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab