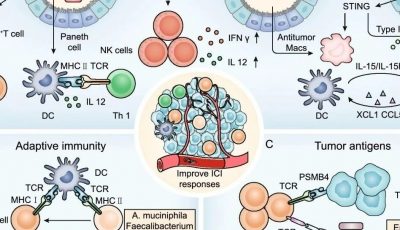
26.1 免疫突触与共刺激信号共同影响抗肿瘤 T 细胞免疫反应
T细胞和NK细胞介导的免疫受到严格控制,因为它们的功能涉及清除那些显示感染迹象、遗传压力和/或促进组织炎症的细胞。T细胞在胸腺的选择过程可确保 T 细胞库的受体(TCR)对自身抗原耐受,并偏向于识别与自身 MHC 分子结合的外来肽。
当T细胞进入人体外围组织后,它们会在抗原呈递细胞表面上搜索抗原。在非炎症状态下遇到相应抗原时,常见的反应是抗原特异性的淋巴细胞发生凋亡或被诱导进入无效状态,而相关的淋巴细胞出现功能障碍。但是,在组织遭受严重损伤、感染或炎症时,环境条件不同,专业的抗原提呈细胞会呈现激活信号,这些信号与处理过的抗原表位一同作用于T细胞受体(TCR),从而引导T细胞快速增殖(克隆扩张)并获得促炎和细胞毒性功能。
辅助信号的传递由可溶性因子(如细胞因子和白细胞介素)以及膜结合的受体-配体对(即共刺激分子)介导。
目前普遍接受的工作模型认为,T细胞的激活依赖于三个不同的信号:第一个信号源自TCR-CD3复合物,第二个信号具有潜在的致病作用,并可抑制细胞凋亡,而第三个信号会增强促炎反应和细胞毒性功能。
在概念上,信号2和信号3很难区分,因为许多共刺激途径同时影响这两种功能。更为复杂的是,表面受体的活性常常调节细胞因子的释放,而这些细胞因子又可以通过自分泌或旁分泌的方式发挥作用,从而使功能效果的归属变得模糊。
总的来说,当TCR识别扫描细胞的抗原性时,是共刺激分子在特定的环境中决定了免疫应答的免疫原性。
值得注意的是,存在另一类表面受体及其配体,它们可以中和共刺激分子的作用,这些在概念上被称为共抑制分子。
共刺激分子如CD28和CD27在未激活的、静息状态的T细胞上常常固有地表达。而像ICOS、CD137、OX40和GITR这样的共刺激受体,则通常只在淋巴细胞经过抗原激活后,或当它们的表达水平从极低的基线状态显著上调时,才在细胞膜上显现。这一区分对于免疫疗法具有重要意义,因为据此可以推断,某些共刺激受体可能在T细胞激活的阶段发挥作用,而其他共刺激机制则可能专门在激活后的T细胞上表现出来。
关键在于,这些受体与配体间的互动通常是在一种特定的细胞对细胞接触环境中进行的,这种环境被称为免疫突触。免疫突触结构主要由黏附分子(例如整合素及其配体)精密地组织而成。胆固醇富集的膜微区域,以及细胞内的微管和肌动蛋白网络,也在这一复杂的结构中扮演重要角色。囊泡和分泌颗粒则利用中心体和微管网络朝向细胞接触区域进行有序的定向移动。TCR和共刺激分子都在这一亚细胞环境中相互作用并发出信号。免疫突触层面的其他激活机制则是由定向分泌的细胞因子所介导的。最著名的五种可溶性蛋白包括IL-2、IL-12、IFNα/β、IFNγ和IL-15。特别是IL-15,在功能上更类似于膜结合型的共刺激分子,因为它通过IL-15Rα附着在细胞膜上,从而呈现给接触的淋巴细胞。
共抑制系统包含的受体-配体对同样在免疫突触层面发挥功能,但它们的角色是缓和或抑制激活信号。这些共抑制受体的作用在于抑制自身免疫反应和保护健康细胞不受病原体感染所引起的组织损伤。这些共抑制配体和受体通常被称为免疫检查点,对此本书的相关章节提供了详细阐述。要深入理解共刺激与共抑制受体之间的平衡,关键在于认识到这些受体对维持整合素依赖的细胞间接触的稳定性和持久性起着控制作用,这直接影响免疫突触中进行的抗原呈递过程。
共刺激分子本身不具备酶活性,其功能依赖于对信号适配蛋白的动态招募。分析共刺激受体发出的细胞内信号是一项挑战,因为这些信号往往在强大的TCR-CD3刺激背景下产生。研究通常表明,共刺激受体的总体作用主要是对TCR依赖的信号进行放大或增强,并很少有证据显示它们能够独立触发生化的第二信号传递。这类共刺激受体的下游直接生化事件主要包括酪氨酸和丝氨酸/苏氨酸残基的磷酸化,或是蛋白质发生泛素化。这两种改变都能引发瞬态蛋白质相互作用位点的产生和多蛋白复合体的形成,这通常会导致转录因子的激活。
共刺激分子的信号传递通常由其天然配体激活,不过也可以通过二价抗体或配体、单克隆抗体(mAbs),或其他分子如核苷酸适配体的交联作用来增强。这些信号传递过程一般在免疫突触的特定区域内发生,并且在受体与配体结合后,受体往往会被内化。
肿瘤坏死因子受体(TNFR)家族由具备不同结构和功能的分子组成,分为包含胞浆内死亡结构域的成员以及不含此结构域的成员。这个家族在免疫系统中负责调控多种机能,包括诱导细胞凋亡、参与炎症反应以及激活淋巴细胞。在肿瘤免疫疗法中,特别关注的是那些不含死亡结构域的靶向受体,因为含有死亡结构域的受体会引入caspase激活机制。TNFR自身不具有任何内在酶活性,它们的信号传导作用依赖于肿瘤坏死因子受体相关因子(TRAF)家族以及其他适配蛋白的协助。图26.1通过示意图展示了TNFR家族成员及其配体在免疫突触中的作用,并且介绍了正在临床开发中的激动剂单克隆抗体。
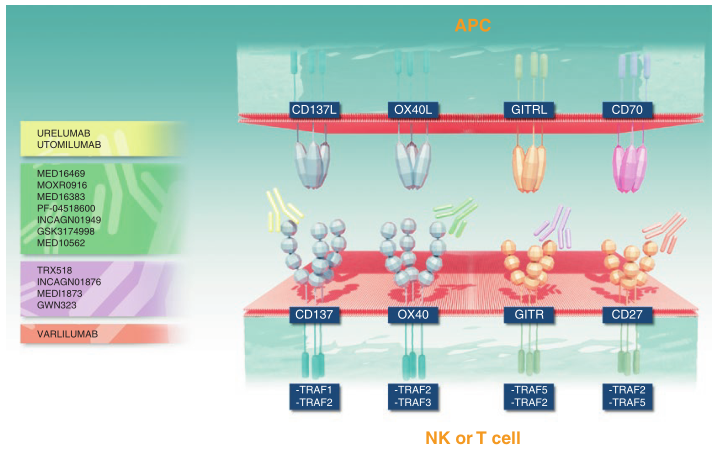
Fig 26.1 在T细胞、NK细胞和抗原呈递细胞(apc)上表达的TNF和TNFR家族的组成型和激活诱导的共刺激成员。效应T细胞(Teff)、调节性T细胞(Treg)和具有APC功能的NK细胞之间的免疫突触示意图。为每个TNFR共刺激分子提供了TRAF接头的使用和临床开发中的激动剂单克隆抗体的参考
26.2 TNFR家族共刺激受体抗体激动剂的临床前和临床经验
在药理学领域,有意识地以抗原特异性的方式启动或增强免疫反应一直是一个长期追求但难以达成的目标。虽然疫苗接种在预防领域取得了成功——即在接触传染性病原体或毒素之前诱导出中和抗体——但是在诱导保护性细胞免疫反应方面,疫苗的效果通常是有限的。在癌症治疗中,常见的现象是已经存在一定程度的免疫反应,虽然这些反应强度不足以消除恶性肿瘤,但从多项小鼠和人类研究中我们得知,这些免疫反应实际上在积极地限制肿瘤的进展。在一定程度上,免疫系统与癌症之间维持着一种动态平衡,主要在肿瘤的微环境及可能在肿瘤引流的淋巴结中发挥作用。基于这些观点,可以设想通过对这种微环境中的免疫细胞受体施以药理影响,决定性地增强潜在的基线免疫反应,从而使其具备对抗恶性肿瘤的能力。20世纪90年代末的免疫学研究意外发现,通过刺激TNFR家族成员可以在小鼠模型中实现肿瘤的根除。目前,关于靶向该家族关键受体的知识和其临床研究效果正在不断积累之中。
26.3 TNF家族成员CD137 (4-1BB)
CD137(亦称为4-1BB或TNFRSF9)最初在活化的T淋巴细胞上被识别到,并已被证实能促进T细胞的增殖和IL-2的产生。实际上,在抗原诱导的激活之后,CD137的表达在活化的CD8+和CD4+T细胞(包括调节性T细胞,Treg)上容易被检测到。研究还发现它在活化的NK细胞、B细胞和髓系细胞上也有表达。在基因敲除小鼠的实验中,CD137被证明对于产生理想的抗病毒和同种异体反应的CTL(细胞毒性T淋巴细胞)反应以及病毒感染后长效记忆T细胞的诱导至关重要。
目前,已确认CD137的唯一跨膜配体是CD137L,属于TNF家族,也称为4-1BBL或TNFSF9。这一配体与受体的相互作用在小鼠和人类中显示出显著的保守性。配体的结合激发CD137通过与TRAF2和TRAF1结合作为主要适配分子,发出强有力的信号。已发现CD137配体的胞外区能够通过与其糖基化状态相关的Galectin 9发生一定程度的预交联作用。这种由凝集素预交联的CD137复合体的构象可能对于信号传导至关重要。
CD137的初始信号传导涉及TRAF2依赖的K-63链型泛素化作用,最终触发NF-κB和MAP激酶途径的活化。早期证据显示,这些途径受到特定去泛素化酶的积极调控。虽然TRAF1在这些复合体中的确切生化功能尚不明确,但最近的研究表明,TRAF1可能参与调节其他TNF家族受体的线性泛素化。有研究表明,存在CD137激动剂时,活化的CD8+ T细胞更易于与抗原发生相遇,这可能与miRNA表达模式的变化和表观遗传层面的染色质结构调整有关。
抗CD137单克隆抗体激动剂和三聚体形式的天然配体已在小鼠模型中显示出抗肿瘤作用。这些单克隆抗体激动剂通过诱发强效的CTL反应来提高针对恶性组织的破坏效率。一些研究指出,这种治疗效果在某些模型中需要NK细胞的参与。CD137与Treg细胞功能的相互作用还存在一些争议,这需要进一步研究以明确。
确实,多种小鼠肿瘤模型已证明对激动型抗CD137单克隆抗体(mAb)治疗响应良好。在难治性肿瘤中,与其他疗法联用时抗CD137 mAb能产生协同效应,这可能导致治愈。这些联合疗法包括与疫苗、细胞因子以及其他免疫激活单克隆抗体的结合使用。此外,放射治疗和化学治疗同样被报道能与抗CD137 mAb产生协同作用。肿瘤细胞膜上表达的抗CD137单链mAb激动剂能够激发强烈的局部细胞毒性T细胞(CTL)和自然杀伤(NK)细胞介导的抗肿瘤免疫反应。最新的研究揭示转录因子eomesodermin在形成这种强力CTL反应中起着关键作用。
对于诸如CD40这样的其他肿瘤坏死因子受体(TNFR)家族成员,激动剂抗体与受体的交联通常依赖于相邻细胞表面的CD32 Fc受体。但是,在我们的研究中发现CD137并非如此,因为缺乏CD32(FcRγII)的小鼠展现出不受影响的抗肿瘤效果,这可能与galectin-9介导的基线预交联作用有关。
二价4-1BB激动型适配体已经在荷瘤小鼠中显现出抗肿瘤活性。这种策略还与一种新型增强肿瘤抗原性的方法结合使用,即通过针对肿瘤细胞的适配体-siRNA融合体来抑制肿瘤细胞无义mRNA介导的降解(NMD)。当4-1BB激动性适配体与针对NMD的抑制策略联合应用时,展现出了协同的抗肿瘤效果。
CD137的胞内区已用于设计含有单链抗体、CD3ζ和CD137胞内区的嵌合抗原受体(CAR)。这些CAR结构中的CD137部分对于支持T细胞的持续生存和扩增至关重要。事实上,包含CD137的抗CD19 CARs在临床上对治疗白血病表现出色,使得T细胞能够在体内长期存活。
CD137共刺激的另一方面,值得关注的是其与T细胞上TCR信号通路的相互作用,以及它在免疫突触中的行为。近期的研究提示CD137能在与其配体结合后迅速被内化,尽管如此,它似乎能持续从内体中传递信号。
在小鼠模型中,针对CD137的抗体不仅成功地治疗了癌症,而且还改善了由CD4 T细胞介导的自身免疫性疾病,例如实验性自身免疫性脑脊髓炎(EAE)、系统性红斑狼疮以及胶原诱导的关节炎。这种看似矛盾的现象尚未得到充分解释,但其作用似乎依赖于CD4淋巴细胞的过度激活,导致这些细胞的最终死亡。与此相反,使用这些抗体治疗小鼠时,通常会引起轻微的肝脏炎症,该炎症由门脉周围区域CD8 T淋巴细胞的多克隆浸润所特征。这种肝脏炎症的发生依赖于CD137的存在(在CD137敲除小鼠中不存在),以及干扰素γ (INFγ) 和肿瘤坏死因子α (TNFα)。值得注意的是,抗CD137单克隆抗体抑制了小鼠的体液性(抗体介导的)免疫反应,这一作用是通过滤泡辅助性T细胞实现的,在人类中,滤泡辅助性T细胞则是健康志愿者血液中CD137基线表达最高的淋巴细胞亚群。在小鼠模型中,通过减少或减弱中和抗体的反应,已经成功地实现了肿瘤病毒治疗与反复给予抗CD137单克隆抗体的配合使用。
在人类和小鼠的自然杀伤(NK)细胞上,CD137的表达是在接触到被IgG包覆的靶细胞并经历抗体依赖性细胞介导的细胞毒性(ADCC)后触发的,这一过程是由CD16的Fcγ受体介导的。CD137一旦表达,激动剂抗CD137单克隆抗体就能显著提升ADCC的功能,从而增强对后续遭遇的响应。实际上,这种强化作用与用于癌症治疗的其他单克隆抗体,如抗CD20的利妥昔单抗或抗EGFR的西妥昔单抗,产生了协同的细胞毒性效应。在接受西妥昔单抗治疗的患者中,已观察到头颈癌浸润性NK细胞中CD137的上调。
目前正在进行两种抗CD137单克隆抗体的临床试验。由BMS公司开发的乌瑞卢单抗(Urelumab),一种IgG4类型的抗体,在临床前的安全性评估中表现出色,包括在犬科猕猴模型中的研究成果。乌瑞卢单抗的初始人体临床试验结果显示,当剂量增至15毫克/千克时,其安全性仍在可接受的范围内。不过,在随后的第二阶段临床试验中,由于一些患者出现肝脏炎症,这一研究项目被迫暂停,且不幸导致两位参与者去世。在研究重新启动后,确认了每两周或四周一次,以0.1 mg/kg的剂量或8 mg/kg的固定剂量为安全用量。目前,乌瑞卢单抗正在与利妥昔单抗(NCT01775631)、西妥昔单抗(NCT02110082)、艾洛妥珠单抗(NCT02252263)和尼伐单抗(2016年SITC会议)等药物的联合治疗方案中进行更进一步的临床评估。乌瑞卢单抗作为单药治疗显示出了一定的临床活性迹象,包括在黑色素瘤(2014年ASCO)、肾细胞癌和淋巴瘤(2016年SITC会议)中观察到的客观应答,虽然其最大的潜力似乎在于联合疗法中。
PFZ-05082566(Utomilumab)是一种IgG2类型的抗CD137单克隆抗体,它在体外试验中展示了生物活性,在非人类灵长类动物安全性研究中也表现良好。该抗体目前正在进行一项I期临床试验及随后的扩展研究,其中包含了与利妥昔单抗(NCT01307267)和彭博利单抗(NCT02179918)联合使用的剂量递增试验。在I期试验中,一些梅克尔细胞癌患者正在接受治疗,初步结果显示该抗体具有客观的临床活性,而在迄今为止的剂量水平上并未观察到肝毒性的迹象。临床缓解数据表明,与pembrolizumab联合使用时,Utomilumab至少在一定程度上增强了治疗效果(ASCO 2016)。因此,扩大研究范围以探索联合免疫治疗策略的必要性变得日益明显。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
作者 | Ignacio Melero, Elisabeth Pérez-Ruiz, Alfonso R. Sanchez-Paulete, Alvaro Teijeira, Angela Aznar, and Miguel F. Sanmamed
初稿翻译 | 冼金欢
编辑排版 | 杜轻松
审核修改 | 王坤 胡珊
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab