导 读
经过多年的研究,我们对免疫系统在晚期癌症中的作用有了新的认识。免疫疗法的种类和多样性也都有了惊人的进展。各种类型的免疫细胞、化学分子和细胞工程单克隆抗体都是有效的治疗资源。在适用于过继性转移前处理或体内药物靶向的免疫效应器中,自然杀伤细胞(NK)表现较为突出。NK细胞是一个先天性淋巴细胞(ILC)群体,他们可以诱导经历了恶性转化和微生物感染的同种异体细胞和自体细胞死亡。它们占人类外周血单核细胞(PBMC)总数的5% -15%,由于它们能够在外周器官之间再循环,所以有助于肿瘤细胞的免疫监视,早期研究也证明了NK细胞在小鼠抗肿瘤反应中的重要性。而在人体中,缺乏NK细胞的病例是很少见的,因此很难评估NK细胞在癌症中的作用。但是几项研究表明,外周血中NK细胞活性的降低与癌症风险的升高之间存在关联。此外,已证明NK细胞的肿瘤浸润是非小细胞性肺癌(NSCLC)、透明细胞肾细胞癌和结直肠癌的有利预后因素。
NK细胞通过表达一系列激活和抑制受体来使其能够检测目标细胞的同时,不伤害正常细胞。所有信号的整合将决定NK细胞的激活状态。NK可以通过人体表达的KIRs(杀伤细胞免疫球蛋白样受体)和小鼠体内表达的Ly49受体,来检测主要组织相容性复合体(MHC)I类是否缺乏 (“missing self假说”)。目前已较全面地了解了KIR家族的特征,揭示了其存在不同的基因和等位基因,以及产生了不同的单倍型。每个KIR受体都能识别一组经典HLA I类同种异型体的α1 域的共有特定特征。KIR抑制性受体通过其胞质结构域中的免疫受体酪氨酸基抑制基序(ITIM)发出信号。当抑制性KIR受体与配体结合时,它们的ITIM发生酪氨酸磷酸化,SHP-1蛋白酪氨酸磷酸酶被激活,从而抑制NK细胞的激活。在NK细胞成熟过程中,需要MHC-I分子与NK细胞受体结合,以产生适应宿主特定MHC-I环境的功能性效应细胞。可在NK细胞亚群上检测到的识别MHC I类分子的相关受体家族被称为Ig样转录物(ILT)或白细胞Ig样受体(LIR)。特别是ILT2(LIR-1)和ILT4(LIR-2),其含有招募SHP-1的细胞质ITIM,也有助于控制NK细胞活化。NK细胞还拥有另一种抑制性受体CD94/NKG2A,它在人类和小鼠中以异二聚体的形式表达。它通过识别与人类HLA-E和小鼠Qa-1b相对应的非经典MHC I类分子。与结合并呈现自身肽的经典HLA-A、HLA-B和HLA-C分子不同,HLA-E结合源自特定HLA-A、HLA-B、HLA-C和HLA-G分子信号序列的先导肽。因此,CD94/NKG2A复合物与HLA-E分子之间的相互作用允许NK细胞间接监测其他MHC-I分子的表达。
在肿瘤转化过程中,细胞通常会降低MHC-I分子的表达,这使它们成为NK细胞的潜在靶点。但NK细胞也需要来自能识别肿瘤细胞膜上配体的激活受体的刺激。在人类和小鼠中,这些激活受体包括NKp46、NKG2D和DNAM-1,而NKp30和NKp44仅在人类NK细胞上表达。NKp30和NKG2D可检测出在基础状态下不存在,但在应激或病原体感染下表达增加的分子,包括2B4和NKp80在内的其他触发性表面分子似乎起着共受体的作用。事实上,激活受体只有在与共受体共同作用时才能诱导自然细胞毒性。大多数成熟NK细胞也表达CD16(Fc-RIIIA),它是G型免疫球蛋白(IgG)Fc区的一种低亲和力受体,这与抗体依赖的细胞介导的细胞毒性作用(ADCC)的产生相关。
NK细胞对靶点的识别导致NK细胞活化和脱颗粒,脱颗粒指含有穿孔素和颗粒酶的颗粒的胞吐。除了依赖于颗粒胞吐的途径外,另一条涉及TNF家族死亡受体及其配体(如TRAIL和FasL)之间相互作用的途径也可导致靶细胞凋亡。NK细胞还能够分泌促合成细胞因子(包括IFN和TNF),它们具有直接的抗肿瘤作用;还有许多趋化因子(包括MCP-1、MIP1-α、MIP1-β、RANTES、淋巴细胞趋化素和IL-8);以及GM-CSF等生长因子,它们都有助于适应性免疫反应的激活。
16.1 NK细胞在治疗中的应用
由于NK细胞能够识别和裂解肿瘤细胞,因此人们对NK细胞能否作为治疗工具寄予了希望。为了将NK细胞应用于临床,科学家们对其开展了许多研究,并进行了200多个(见clinicaltri-als.gov)治疗性试验,旨在增强其体内效应器的能力。
输注纯化的已活化NK细胞
这一策略包括在健康供体中纯化NK细胞,并在将它们注射到患者体内之前用免疫刺激性细胞因子(IL-2或IL-15)进行培养(Fig.16.1a)。已证明这种方法是有效和安全的,但其限制因素仍然是输注的NK细胞在患者体内持续和增殖的能力不足。鉴于如今对ILC复杂性的了解,在未来,还可能设计针对不同ILC亚群的新治疗策略。例如,在因血液系统恶性肿瘤而接受造血细胞移植的患者中,有证据表明表达活化NK细胞受体的ILC,可能通过其增强组织修复的能力来对急性移植物抗宿主病(GVHD)起到保护作用。这些数据需要进一步证实,但它们可能为ILC输注或利用参与粘膜愈合的ILC衍生分子(如IL-22)进行给药治疗开辟了道路。
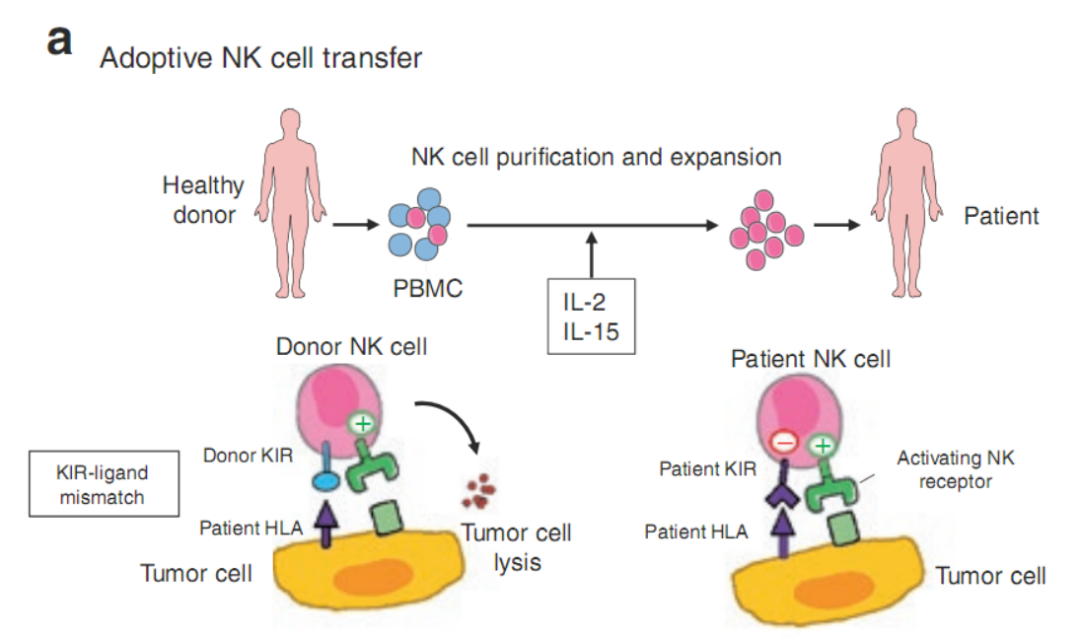
Fig. 16.1a NK细胞从健康捐赠者的外周血中纯化出来,并在注射到患者体内之前在体外用细胞因子(IL-2或IL-15)激活。当供体不表达识别患者HLA分子的KIR时,可以使输注的NK细胞不接收癌细胞的抑制信号,可获得最佳反应。
修饰NK细胞基因提高过继性细胞免疫治疗的效果
目前已开发出增强NK细胞抗肿瘤功能的新基因治疗方法,并正在临床前和临床试验中进行研究。如旨在利用嵌合抗原受体(CARs)增强NK细胞肿瘤特异性的方法(Fig.16.1b),正在通过各种临床前研究以探索表达CD19或CD20受体特异性的CAR-NK细胞在B细胞病理中的应用。或者,在临床前研究中,逆转录病毒转导NK细胞以表达NKG2D或TRAIL显示其肿瘤识别和杀伤的能力得到改善。另一种策略是使用TGF-27的显性负性受体II保护NK细胞免受肿瘤微环境中TGF-β的免疫抑制作用,或通过强制表达IL-2或IL-15来提高NK细胞在体内的存活率。
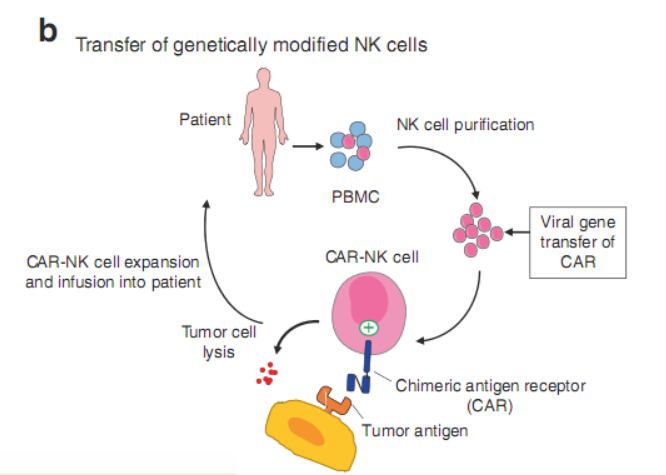
Fig. 16.1b NK细胞是从患者的外周血中纯化出来的,并经过基因改造,以表达一种针对肿瘤抗原(CAR)或其他能够更有效地将NK细胞导向其目标的分子的嵌合受体。
输注细胞因子
目前正在进行的相关临床研究,包括测试细胞因子(如IL-2、IL-15和IL-12)在几种癌症中的有效性和副作用(Fig.16.1c)。在Rosenberg等人的一项早期研究中,淋巴因子激活的杀伤细胞(LAK细胞)和IL-2的结合导致黑色素瘤或转移性肾细胞癌患者的应答率为20%。然而,这种方法的主要问题是:免疫系统以非特殊的方式过度激活,导致神经病变、毛细血管渗漏综合征和肾功能衰竭,进而导致细胞毒性。IL-15是IL-2的一个重要的替代品,且已经在转移性黑色素瘤和转移性肾细胞癌患者中进行了研究。
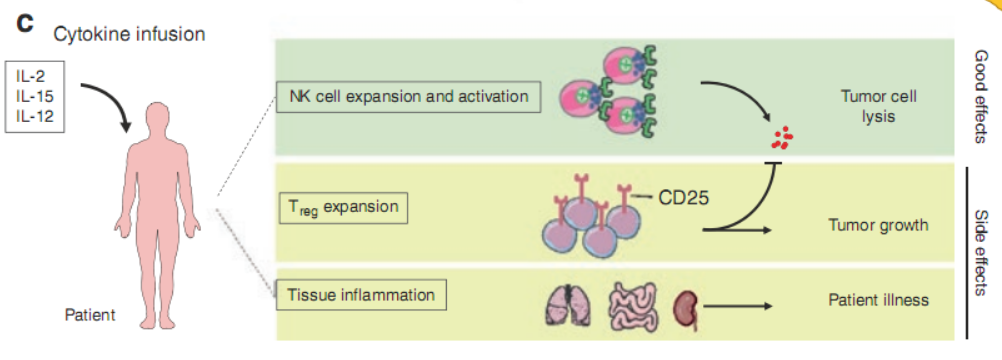
Fig. 16.1c 向患者施用免疫刺激性细胞因子以诱导自体NK细胞的激活和扩增。诱导最强抗肿瘤反应的细胞因子是IL-2,但也会引起显著的副作用,例如调节性T细胞(Treg)扩张和组织内浸润,这使得其难以使用。
肿瘤抗原特异性抗体的输注诱导ADCC
许多临床批准的针对肿瘤相关抗原的治疗性抗体(如利妥昔单抗或西妥昔单抗)通过激活NK细胞介导的ADCC 发挥细胞毒作用(Fig.16.2a)。为了提高IgG Fc区激活受体Fc RIIIA的亲和力,人们尝试了许多不同的方法,包括插入突变或糖基化。如近期批准用于治疗T细胞淋巴瘤的莫加木珠单抗(一种低岩藻糖抗CCR4单抗)和奥比妥珠单抗(用于治疗慢性淋巴细胞白血病(CLL)的抗CD20单抗)。
输注针对抑制性NK细胞受体的抗体
这种方法的目的是,通过单克隆抗体阻断抑制性NK细胞受体来提高自体NK细胞的反应性从而达到治疗患者的目标(Fig.16.2b)。对于未修饰的单克隆抗体(如利妥昔单抗),NK细胞介导的细胞毒性仍受抑制性受体的控制。通过使用阻断某些抑制性受体与其配体相互作用的抗体,有可能增强体内抗肿瘤NK细胞的反应。虽然NK细胞没有真正特异的分子,但有一些表面受体主要由NK细胞表达,并在调节其功能中发挥主要作用。这些分子激活负信号通路,并在控制细胞毒性中作为免疫检查点发挥作用。在下一段中,我们将重点关注这种方法。
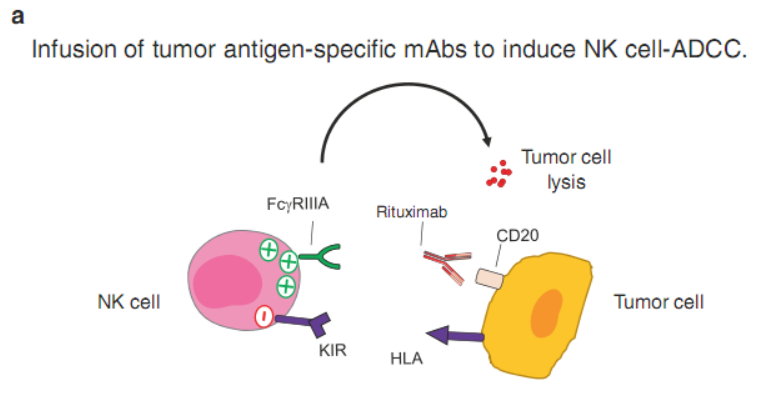
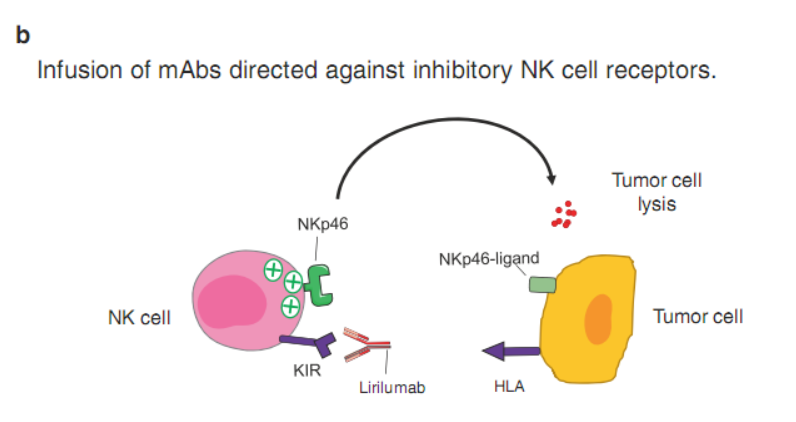
Fig. 16.2 输注NK细胞特异性单克隆抗体。(a)针对肿瘤抗原的单克隆抗体也可以与NK细胞表达的Fc RIIIA受体结合,并诱导NK介导的ADCC。(b)输注针对抑制性NK细胞受体的单克隆抗体可阻断与配体的相互作用,并使NK细胞有效杀死靶细胞
16.2 免疫检查点抑制剂(ICI)
几十年来,免疫系统在癌症患者中的作用一直没有得到重视,在一般情况下,肿瘤通过激活调节免疫稳态的途径,有效地抑制了免疫反应。已证明免疫检查点抑制剂(ICI)(如阻断抗体)是有效的,对几种癌症类型具有可控制的安全性(Fig.16.3)。它们的使用使一些癌症患者(如转移性黑素瘤和非小细胞肺癌患者)的治疗取得了显著进展,并获得了超过10年的长期生存期。因此,免疫反应抑制途径的发现是一个开创性的发现,极大地提高了我们对免疫的理解。
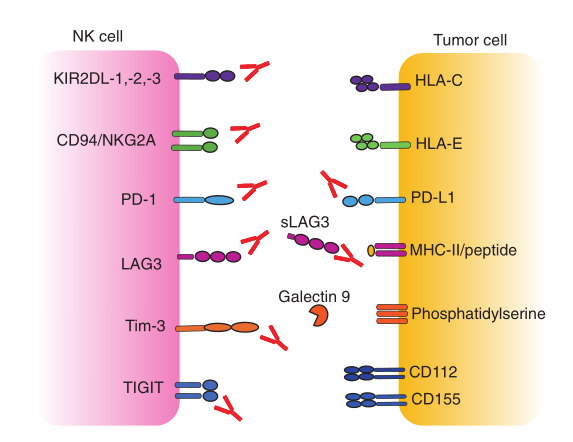
Fig 16.3 NK/靶细胞表面受体/配体抑制相互作用。几种抑制性受体和共受体协同调节NK细胞功能。与基于患者和肿瘤特异性特征开发的阻断性单克隆抗体的联合使用可以解放针对NK细胞活化的阻断。
大多数抑制性受体在其细胞质结构域中含有一个或多个磷酸化的ITIM,并可招募蛋白酪氨酸磷酸酶(SHP-1/2或SHIP)。一项横跨整个基因组的生物信息学研究揭示了300多种至少包含一个ITIM域的I型和II型整合膜蛋白的存在。但是在这些受体中,只有少数是治疗方法出现过的靶向受体(Table 16.1)。
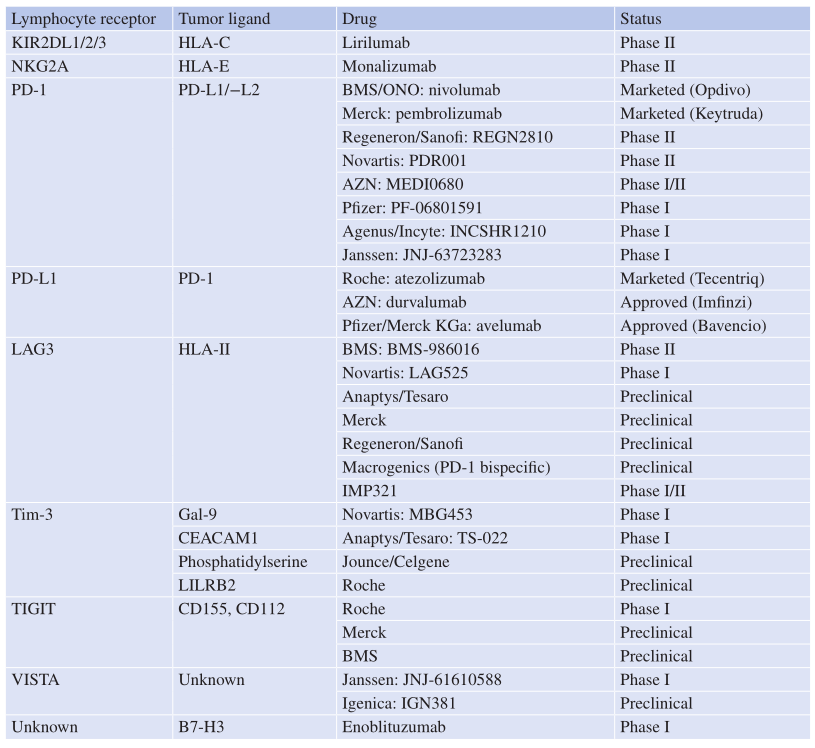
Table 16.1 临床开发中的NK细胞受体/配体靶向药物
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
本篇文章来源于微信公众号:OncoLab