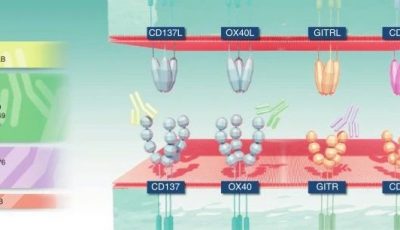
16.2.1 KIRs
KIR2DL1、KIR2DL2和KIR2DL3是抑制性受体,与靶细胞上的HLA-C结合后,参与调控NK细胞的细胞毒性和细胞因子的产生。KIR受体在NK细胞抗肿瘤反应中的作用在接受了单倍体相合骨髓移植实验的急性髓系白血病(AML)患者中得到了证实。
事实上,接受KIR/HLA-C不匹配骨髓移植的亚组患者在不出现GVHD(移植物抗宿主病)的情况下疾病复发率显著降低,在后续研究中也表现出更高的生存率。这表明,供体来源的同种异体反应性NK细胞能够介导安全持久的抗肿瘤免疫反应。
为了用药物模拟这种治疗策略,科学家研发了一种阻断HLA-C与三种抑制性KIR受体结合的治疗性单克隆抗体:1-7F9,它是一种完全的人IgG4,可增强NK细胞对表达HLA-C的肿瘤细胞的细胞毒性。其疗效已在体外使用由自体或异体NK细胞靶向患者来源的AML细胞,以及在人源化的AML小鼠模型中得到证实。
该方法的有效性也在同基因肿瘤模型中得到了验证。用特异性单克隆抗体阻断Ly49C/I(小鼠KIR的同源受体)可以在保留正常组织的同时,诱导NK细胞选择性杀伤肿瘤细胞。其也将运用于杂交瘤衍生产品IPH2101的临床开发。多个I期临床试验测试结果表明,KIR阻断剂是安全的,且副作用很小,值得做进一步临床研究。
随后,研究人员研制出具有相同抗原特异性的稳定重组IgG4 的lirilumab(针对KIR的抑制性受体,主要是IPH2102,BMS-986015),以提高单抗的稳定性和生产的可行性。
目前已在多个I期和II期临床试验中进行了测试:作为老年AML患者的维持性单一疗法(NCT01687387),或与多发性骨髓瘤中的肿瘤靶向单抗埃洛妥珠单抗(NCT0225263)或AML中的DNA低甲基化剂5-氮杂胞苷(NCT0239917)或骨髓增生异常综合征(NCT02599649)、CLL(慢性淋巴细胞白血病)中的利妥昔单抗(NCT02481297)联合使用。
有趣的是,体外和体内研究表明,lirilumab可以增加利妥昔单抗诱导产生的ADCC。
最近,一项II期临床研究测试了lirilumab作为单一疗法治疗多发性骨髓瘤患者的疗效,该研究因无明显治疗效果而提前终止。作者认为,这可能是由KIR2D+NK细胞的反应性降低导致,这些细胞表面的KIR2D表达会发生减少。但是,在其他临床试验中尚未检测到这种物质的减少,所以这一猜想仍有待证实。这些结果可能表明,至少在某些恶性肿瘤中,需要适应性的治疗方案(间歇性阻断)或使用联合治疗来诱导有效的抗肿瘤反应。
例如,鉴于抗PD-1阻断单克隆抗体临床试验的成功,以及它们能诱导促进NK细胞激活的免疫刺激性细胞因子(如IFNγ)的能力,在临床治疗中联合使用lirilumab和nivolumab,可以在实体瘤(NCT01714739)和血液恶性肿瘤(NCT01592370)的治疗中同时恢复NK细胞及T细胞的功能。在晚期实体瘤患者中进行的两个I期临床试验中,与nivolumab单一疗法相比,这种联合疗法没有显示出额外的不良反应。
最近,一项I期/II期试验证明了lirilumab联合nivolumab的治疗方法对晚期具有耐药性的头颈癌患者的治疗是有效的。这是一项单组临床试验,虽然没有对照人群,但有可靠的头颈癌历史对照数据来作为判断依据。这项研究表明,头颈部癌症患者对lirilumab的耐受性良好。虽然数据仍在进行跟踪和完善,但在单组临床试验的小研究背景下,从治疗效果角度观察到的结果十分令人鼓舞。在6个月和12个月时,使用lirilumab和nivolumab联合治疗的患者的总生存率分别为90%和60%。相比之下,受美国食品药物管理局批准的仅使用nivolumab治疗的患者的总生存率分别为55.6%和36%。
这些初步临床数据表明,联合使用lirilumab和nivolumab可以有效治疗头颈癌患者,这项成果在某种程度上类似于其他癌症适应症的报道,例如用PD-1或CTLA-4免疫检查点抑制剂治疗的黑色素瘤。同时,该试验结果可以帮助我们深入评估免疫相关生物标志物。
最近发布了一项随机、双盲、安慰剂对照的II期临床试验(EffiKIR)的结果,该试验评估了lirilumab作为单一药物对老年AML 患者的疗效(NCT01687387)。尽管该研究未达到主要疗效终点,但证实了lirilumab作为单一疗法具有安全性。具体的试验分组为,两组患者在不同治疗间隔接受不同剂量(每3个月0.1 mg/kg或每4周1 mg/kg)的单剂lirilumab,而第三组患者接受安慰剂。lirilumab组和安慰剂组在无白血病生存率(LFS)和其他疗效终点方面均无统计学显著差异。试验每个月1 mg/kg组因LFS与安慰剂组无明显差异而终止。该试验的数据分析仍在进行中,后续将进一步完成对本试验结果的分析。
现在仍有6项涉及lirilumab的试验在进行中,试验涉及一系列实体癌和血液癌适应症,并与包括nivolumab在内的其他药物联合使用(见clinicaltrials.gov)。
16.2.2 NKG2A
NKG2A是一种由大多数NK细胞和部分细胞毒性T淋巴细胞表达的抑制性受体,可识别人类的HLA-E分子和小鼠的Qa-1分子。
与经典的HLA I类分子不同,50–80%的实体瘤或白血病/淋巴瘤患者的HLA-E表达保留,甚至增加。而一项针对NSCLC的研究表明,在肿瘤微环境中NK细胞的激活受体和KIR表达较低,但NKG2A的表达不受影响。同时,HLA-E在肿瘤细胞上高表达,在周围上皮细胞上呈阴性。
NKG2A在肿瘤浸润的NK细胞和T细胞上的表达也已在乳腺癌和宫颈癌中得到证实,并且似乎与肿瘤细胞分泌的IL-15和TGF-β有关。一项针对黑色素瘤患者的研究表明,表达NKG2A的肿瘤抗原特异性CD8+T细胞的效应器功能受到其抑制。
因此,只有在肿瘤稳定表达经典HLA I类分子且不表达HLA-E的患者中,肿瘤浸润性CD8+T细胞才是NSCLC患者的有利预后因素。此外,HLA-E表达增加(在20%的结直肠癌患者中有记录)会造成机体出现大量CD8+T细胞浸润的不良后果。
所有这些结果表明,NKG2A是一个重要的检查点,可以直接作用于浸润的淋巴细胞,可以通过阻断它来提高机体抗肿瘤免疫反应。在一项临床前试验中,一种针对NKG2A(Z270)的人源化单抗在体内和体外试验中都表现出了可以有效增强NK细胞对白血病和淋巴瘤细胞的细胞毒性。这种抗体后来被开发运用于临床治疗,名为莫那利珠单抗(IPH)。
目前,它作为单一药物运用于妇科恶性肿瘤的II期临床试验(NCT02459301)、口腔鳞状细胞癌的术前治疗(NCT02331875),或与西妥昔单抗(抗EGFR单抗)联合治疗头颈癌(NCT02643550)、与伊布替尼(BTK抑制剂)联合治疗CLL(NCT02557516)、与杜瓦鲁单抗(抗PD-L1单抗)联合治疗各种实体瘤(NCT02671435)。
16.2.3 PD1
PD-1是一种结合PD-L1和PD-L2的抑制性受体,PD-L1和PD-L2的特异性配体表达于多个肿瘤或感染细胞上,也表达于炎症灶中的专职抗原呈递细胞(APC)。
研究者最早是在T、B和髓样细胞上发现PD-1的表达,而最近有研究发现在多发性骨髓瘤和卵巢癌患者的NK细胞上也存在PD-1的表达。体外研究表明,NK细胞上PD-1与肿瘤细胞表达的PD-L1结合会抑制NK细胞对肿瘤细胞的杀伤能力,而PD-1阻断单抗可以恢复NK细胞功能,促进NK细胞向肿瘤部位迁移。
在过去几年中,已经开发出几种阻断PD1/PD-L1相互作用的抗体(Table.16.1),目前已用于治疗晚期实体瘤。其中,nivolumab已被证明能在T淋巴细胞中诱导与细胞毒作用、NK细胞功能相关基因的表达,如IFNγ和颗粒酶B。这些数据表明,在T细胞和NK细胞中,抗PD-1/PD-L1单抗可以通过相同的分子机制来提高机体抗肿瘤免疫反应。
在小鼠体内进行的PD-1阻断试验中,可以观察到小鼠机内出现抗肿瘤免疫反应恢复的现象。同时,在实体癌和血液癌患者中进行的临床试验上,也可以观察到运用抗PD-1/PD-L1单抗的单一疗法对疾病的治疗是有效的,它可以刺激机体出现有利的临床反应。重要的是,这些反应通常是持久的,且对大多数人没有严重毒性。只有少数使用PD-1或PD-L1特异性抗体治疗的患者会出现强烈的不良反应。
使用该疗法时肿瘤的快速减少率通常在10%到40%之间,具体速率取决于患者自身。为了解释这种变异性,从组织学角度对治疗前从患者处收集到的各种肿瘤活检进行了检查,其组成与在患者观察到的反应等级有关。
检查结果明确了对抗PD-L1/PD-1疗法有反应的三种免疫特征表型。第一个特征是“炎症”表型,其特征是在肿瘤实质中,肿瘤细胞周围存在大量免疫细胞。在这些样本中,浸润的免疫细胞可能表现出PD-L1染色。这一特征表明机体预先存在抗肿瘤免疫反应,但该反应可能已被肿瘤中的免疫抑制所阻遏。事实上,抗PD-L1/PD-1单抗在临床上最常用于炎症型肿瘤患者的治疗,并且治疗效果显著。
第二个特征是“免疫排斥”表型,其特征也是存在大量免疫细胞,但它们位于肿瘤细胞周围的基质中,不穿透实质。
第三种是“免疫沙漠”表型,其特征是肿瘤的实质或基质中缺乏造血细胞。这种表型可能反映了机体存在抗肿瘤免疫缺失,因此这类肿瘤患者对抗PD-L1/PD-1疗法不产生反应也就不足为奇了。
相比之下,并非所有具有免疫炎症特征的肿瘤都对抗PD-L1/PD-1治疗有反应。在这些情况下,我们考虑是否其他免疫检查点才是抑制机体抗肿瘤免疫反应的原因。
16.2.4 LAG3
淋巴细胞活化基因3,又称LAG3,是一种属于免疫球蛋白超家族的细胞表面分子,由活化的T淋巴细胞、NK细胞、B细胞和浆细胞样树突状细胞表达,具有多种生物学效应。
LAG3是MHC II类分子的配体,它与MHC II类分子结合时具有很高的亲和力。它是一种免疫检查点受体,负性调节T细胞的细胞增殖、激活和内环境稳态,据报道它可以激活Treg的抑制功能。
在发现LAG3早期,LAG3缺陷小鼠的实验表明,LAG3在NK细胞中发挥着至关重要的作用。但是,由于LAG3也被发现在肿瘤浸润的CD8+T细胞上表达,并抑制其增殖和IFNγ的产生,因此,针对LAG3的研究主要集中在其抗体在调节适应性免疫中的作用。
LAG3现在是制药公司开发针对癌症和自身免疫病新疗法的各种药物的主要目标靶点。LAG3特异性单克隆抗体的预期作用机制是解除NK细胞和T细胞的负调节。
MHC II类分子通常仅由APC表达,但据报道一些癌细胞也会表达它们。研究表明,LAG3与黑色素瘤细胞表达的MHC II类分子的相互作用可以保护黑色素瘤细胞免受FAS介导的细胞凋亡。
LAG3还编码另一种剪接变体,该变体可转化为可溶性LAG3(sLAG3),具有免疫佐剂活性。尽管促进LAG3编码sLAG3不是使用LAG3特异性单克隆抗体进行临床试验的预期目标,但其可能有利于患者治疗。
有趣的是,sLAG3被认为只与APC一小部分脂筏微结构域中的MHC II类分子结合。同样有趣的是,一种临床级可溶性LAG3蛋白(LAG3-Ig融合蛋白,IMP321),同时也是一种生理性高亲和力MHC II类分子粘合剂,已被证明在短期体外试验中可以诱导NK细胞和CD8+T细胞产生IFNγ和TNF。IMP321的I期和II期临床试验仍在进行,其分别作为标准化疗的辅助疗法或联合抗PD-1治疗的免疫刺激药物。BMS-986016是一种抗LAG3单克隆抗体,目前正在进行II期临床试验。
许多其他LAG3抗体仍在临床前研究中,有待进一步发掘。LAG3可能是比PD-1更好的检查点抑制剂靶点,因为它既能激活T细胞和NK效应细胞,又能抑制Treg抑制活性。针对LAG3联合nivolumab(NCT01968109)的治疗策略目前正在研究中,受试者为局部晚期(转移性和/或不可切除的)实体瘤患者。
16.2.5 Tim-3
Tim-3是一种由先天性和适应性免疫细胞表达的I型糖蛋白。它首先被鉴定为在产生IFNγ的CD4+T辅助细胞1(Th1)和CD8+细胞毒性T细胞上选择性表达的分子。同时它也是功能成熟的NK细胞组成性表达的分子。Tim-3在被激活后,通过降低细胞毒性和产生细胞因子,来作为NK和T细胞的抑制性受体发挥作用。
在晚期黑色素瘤、NSCLC和滤泡性B细胞非霍奇金淋巴瘤患者的T细胞上也发现有Tim-3。在这三种癌症中,所有Tim-3+T细胞共同表达PD-1,并表现出增殖和细胞因子产生缺陷的特点。
最近的一项研究表明,晚期黑色素瘤患者循环NK细胞中Tim-3的表达增加,并出现了衰竭表型。因此,用单克隆抗体阻断Tim-3信号可以促进肺腺癌患者外周NK细胞的细胞毒性和IFNγ产生增加。因此,NK细胞中Tim-3的表达可以作为人类恶性肿瘤的预后生物标志物。
抗Tim-3阻断单克隆抗体目前正在进行I期临床试验,即将公布的证据表明,它们可与抗PD-1疗法结合使用。事实上,在临床运用抗PD-1治疗的背景下,治疗失败与替代免疫检查点(最显著的是Tim-3)的上调相关,而当抗Tim-3单克隆抗体与抗PD-1药物一起使用时,可以有效减少患者对抗PD-1治疗的耐药性。
16.2.6 TIGIT
TIGIT(T细胞免疫球蛋白和ITIM结构域)是免疫球蛋白超家族的一种受体,在NK细胞、效应和记忆T细胞以及Treg细胞上表达,在这些细胞上,它作为一种共抑制受体发挥作用。
它结合的两种配体CD155(PVR)和CD112(PVRL2,nectin-2),在APC、T细胞和包括肿瘤细胞在内的多种非造血细胞上表达。
CD226(DNAM-1)的配体与TIGIT相同,但其亲和力较低。重要的是,TIGIT可以抑制CD226和CD155之间的相互作用。TIGIT参与诱导CD226磷酸化和SHP1(含有SH2结构域的肌醇-5-磷酸酶1)的募集,并导致NK细胞的细胞毒性、颗粒极化和细胞因子分泌受到抑制。
在与肿瘤细胞上高度表达的CD155和CD112相互作用后,TIGIT负向调节抗肿瘤反应。事实上,在两种不同的肿瘤模型中,TIGIT缺陷小鼠的肿瘤生长出现明显延迟,而TIGIT在广泛的肿瘤浸润淋巴细胞上高度表达。
在黑色素瘤患者的CD8+T细胞中,TIGIT与PD-1联合阻断可进一步改善细胞增殖、细胞因子的产生及脱颗粒。在临床前模型中,该联合疗法可能会导致机体对肿瘤产生完全排斥反应。
有趣的是,TIGIT不仅能与PD-1协同作用,还能与Tim-3协同作用,削弱机体抗肿瘤反应。因此,TIGIT与PD-1或TIGIT与Tim-3联合阻断可促进抗肿瘤免疫并诱导肿瘤消退。一种人类抗TIGIT单克隆抗体(MTIG7192A,RG6058)与抗PD-1疗法联合应用于各种实体瘤的I期临床试验正在进行中。
16.3 Perspectives
最近在肿瘤治疗方面的突破是科学家几十年来的研究的成果,它可以帮助我们更好地理解癌症的生物学基础,释放免疫系统的力量。
针对免疫检查点的治疗方法在不同类型癌症患者中都取得了显著效果。尽管抗PD-L1/PD-1的单克隆抗体在临床上取得了成功,并随着阻断其他免疫检查点的抗体的临床发展,在联合治疗中发现了更好的临床疗效(Table.16.1),但是只有一部分患者在使用其治疗后会产生长期免疫应答反应。
此外,患者个体的免疫状况会受一系列因素影响,包括肿瘤的固有特性及环境因素,如传染源。这表明我们需要对癌症免疫有更广泛的认识,需要进一步的研究来确定参与NK细胞毒性调节的所有受体,以便开发阻断与其配体相互作用的单克隆抗体,从而增强NK细胞的抗肿瘤免疫反应。
只有通过对体内肿瘤进行活体组织检查,确定最有可能对阻断不同免疫抑制性受体的靶向治疗方案有反应的患者,才能决定针对肿瘤和患者的靶向治疗方案。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
本篇文章来源于微信公众号:OncoLab