内容简介
创新性及研究意义

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab
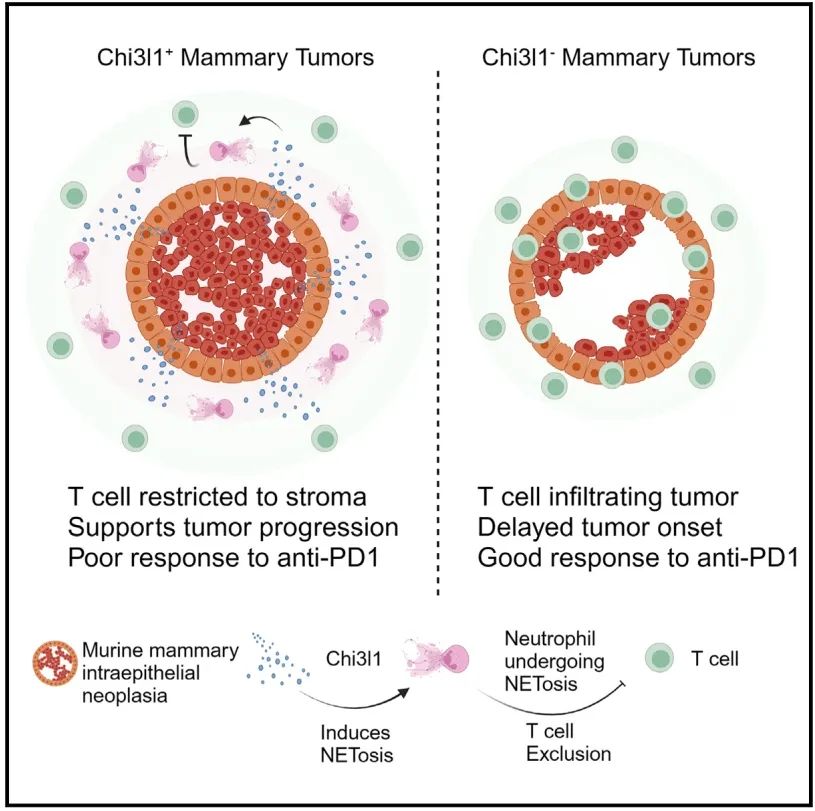
杂志名称:Immunity 发表日期:2023.11.18 DOI:10.1016/j.immuni.2023.11.002. PubMed:https://pubmed.ncbi…

内容简介
创新性及研究意义

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab