28.4 树突状细胞的活化
单独使用GM-CSF和Flt3L的研究已经显示出低毒性但疗效有限,这证实了树突状细胞(DC)在启动和动态平衡中的生理作用。这些研究表明,虽然它们有助于APC的分化,但不足以促进APC进入肿瘤,还需要激活信号。尽管这些信号可能来自免疫原性细胞死亡释放的物质,但通过引入病原体相关分子模式(PAMP)来触发强效的先天免疫反应可能更为有效。
TLR是进化上保守的先天免疫受体,能够识别PAMP和一些潮湿物质。TLR的配体,如脂多糖(LPS)、游离单链或双链RNA(ssRNA或dsRNA)和低甲基化DNA基序,不仅能结合并激活典型的TLR途径,还能激活其他细胞质炎症途径。这些途径的综合刺激导致成熟信号,增强DC的抗原呈递和交叉呈递能力,并随之激活T细胞。
TLR既存在于细胞表面(如TLR1、2、4、5和6),也存在于内体(TLR3、7、8和9)。它们的分布决定了它们识别PAMP和DAMP配体的能力。TLR7经典地识别游离的单链RNA,该TLR的激动剂是FDA批准用于临床的第一个PAMP类似物——咪喹莫特。TLR7在多发性骨髓细胞系中高表达,尤其在浆细胞样树突状细胞上表达最高,这些细胞通过诱导I型干扰素α/β发挥关键的抗病毒作用。咪喹莫特是一种能够激活TLR7并诱导强效抗病毒免疫反应的咪唑并喹啉衍生物;它最初被批准用于治疗皮肤病毒感染引起的生殖器疣,随后被批准用于治疗基底细胞癌和光化性角化病,标签外的适应症还包括皮肤病毒感染如传染性软疣。
临床前研究还调查了咪喹莫特在其他非病毒来源癌症中的应用。在小鼠皮肤乳腺癌模型中,局部应用咪喹莫特联合局部放射治疗导致肿瘤完全消退,并在远端部位观察到异常反应,提示诱导了T细胞介导的抗肿瘤免疫反应。在该模型中,反应与肿瘤病变中T细胞的增加有关,异常效应依赖于CD8+ T细胞。类似的试验也在皮肤转移性黑色素瘤或乳腺癌患者中进行了小系列或病例报道;局部应用咪喹莫特可诱导促炎肿瘤微环境并导致一些肿瘤消退。许多系列或病例报道也显示了咪喹莫特在皮肤T细胞淋巴瘤和B细胞淋巴瘤中的抗肿瘤作用,现在这种佐剂已成为一种常见的非标签使用方法。
在使用咪喹莫特和人类癌症-睾丸抗原NY-ESO-1多肽疫苗治疗黑色素瘤的组合方法中,患者接受Flt3L预处理,并将咪喹莫特应用于疫苗部位。不幸的是,这种疫苗三联方案的临床应答率并不理想。在27名患者中,只有12名可评估,其中仅一小部分人接受了咪喹莫特治疗,只有一名患者经历了部分应答。
咪喹莫特的全身治疗已经在临床前模型中进行了评估。口服治疗在结直肠癌、肉瘤和肺癌模型中显著诱导了干扰素的产生,并抑制了肿瘤生长。在淋巴瘤模型中,静脉注射R848(一种鸟苷衍生物,可作为TLR7和TLR8的激动剂)与局部肿瘤照射相结合,可诱导持久的CD8+ T细胞抗肿瘤免疫反应,清除全身疾病,并防止肿瘤再发。一种新型的咪唑喹啉,3M-052或MEDI9197,也是一种TLR7和TLR8配体,具有允许组织滞留的脂尾。在临床前模型中,MEDI9197被证明在靶区和远端肿瘤内注射后可抑制肿瘤生长。PD-L1和CTLA-4的阻断增强了这种抗肿瘤作用,即使仅使用检查点阻断模型也是如此。治疗转移性疾病的I期试验目前正在进行中,最近的试验队列将MEDI9197与抗PD-L1治疗相结合,希望重现临床前研究中的协同抗肿瘤免疫反应。
关于I型干扰素(IFN)在控制肿瘤生长中的作用已有广泛研究。I型IFN似乎对启动抗肿瘤免疫反应至关重要。临床前研究表明,这不仅仅是由于IFN在刺激细胞毒性T细胞方面的作用,更是由于其在诱导DC成熟方面的作用,尤其是小鼠中BATF3+ CD8+ CD141+ DCs(人类α+ DCs的对应物)。这些DCs最能将肿瘤抗原交叉递送给CD8+ T细胞。
TLRs是有效的IFN刺激因子;然而,还有其他细胞质模式识别受体(PRRs)也能诱导免疫反应。诱导IFN的关键之一是STING受体,它是cGAMP的受体,cGAMP是细胞质DNA的降解产物。STING的激活已被证明能强烈激活I型干扰素的转录。临床前研究表明,将刺激剂DMXAA(也称为ASA404)注入小鼠B16黑色素瘤中,足以启动肿瘤特异性CD8+ T细胞并实现肿瘤的免疫排斥。尽管DMXAA在化疗结合下在人类非小细胞肺癌(NSCLC)的大型III期试验中未显示出显著活性,但后来发现这是由于其与人类STING的结合较差所致。ADU-S100是一种新型的环二核苷酸,可以结合并激活人类和鼠类的STING,目前正在进行肿瘤内注射的早期试验。
研究发现,癌细胞可能通过下调STING通路来避免在快速分裂过程中因DNA损伤反应而诱导干扰素的产生。溶瘤病毒领域利用了这一点,开发了两种主要方法:一种是使用经过改造以降低正常组织毒性的致病病毒(如单纯疱疹病毒和牛痘病毒),另一种是使用在人类细胞中通常不具毒性但能够在干扰素途径被抑制的癌细胞中感染和繁殖的病毒(如新城疫病毒)。
溶瘤病毒不仅能诱导肿瘤溶解和抗原释放,还能通过病毒成分激活固有的PRR。虽然这些病毒在初期的临床疗效有限,但额外的免疫刺激,如生长因子或细胞因子,可以增强病毒感染诱导的免疫反应。JX-594是一种痘苗病毒,设计成在感染细胞中表达GM-CSF,已被证明能在肿瘤细胞中选择性复制,并在肿瘤内或全身接种病毒后,在临床前模型和早期临床研究中显示出抗肿瘤免疫效果。这些研究显示,在小鼠和人类中,T细胞向肿瘤中的渗透增加,肿瘤相关血管系统中断,导致肿瘤细胞血流量减少和迅速坏死。这种效应是肿瘤特有的,因为正常血管的内皮细胞不受影响,从而保留了正常的干扰素反应。肝癌和黑色素瘤的临床试验发现,JX-594耐受性良好,应答率令人鼓舞。
类似地,单纯疱疹病毒通过不表达阻断MHC分子上抗原呈递的基因和其他关键基因,并将GM-CSF注入病毒基因组,显示了显著增强的免疫原性。被称为Talimogene laherparepvec或T-VEC(以前称为OncoVEX GM-CSF)的临床试验表明,在接受治疗的肿瘤中,可以有效地诱导肿瘤坏死和远端肿瘤的炎症,并且在黑色素瘤、头颈癌、乳腺癌和其他转移性恶性肿瘤患者中显示了显著的应答率,包括一些完全缓解。在晚期黑色素瘤患者中的III期研究显示,与单独使用GM-CSF相比,T-VEC的应答率更高,总体存活率有改善的趋势(p=0.051),这导致T-VEC被批准用于临床。
溶瘤病毒与免疫调节剂(如检查点阻断抗体)的结合展示了巨大的希望;这些试验(例如,NCT03069378,NCT02965716)和溶瘤病毒领域的进展由Puzanov教授在本系列的其他部分进行了详细综述。
STING是一种识别游离DNA的细胞质模式识别受体(PRR),而内体TLR9是另一种能够感应游离DNA的PRR,特别是低甲基化的CG富集型寡核苷酸(CpG)岛DNA,这种DNA常见于原核基因组中。TLR9在浆细胞样树突状细胞(pDCs)和其他树突状细胞(DC)亚型中有不同程度的表达,在B细胞上也有表达,B细胞也可以是有效的抗原提呈细胞(APC)。
有趣的是,B细胞淋巴瘤起源于表达高水平TLR9的成熟B细胞。含有CpG的配体可以激活淋巴瘤B细胞,就像它们对非恶性B细胞所做的那样,增加共刺激分子的表达。在淋巴瘤模型中,CpG配体抑制恶性B细胞的增殖。当与诱导免疫原性细胞死亡的全身化疗相结合时,CpG在注射部位和远端病变处以CD8+ T细胞依赖的方式诱导抗肿瘤反应和疾病消退,表明CpG增强了肿瘤反应性T细胞的启动。
虽然肿瘤树突状细胞也可能对TLR9配体产生反应,但在携带TLR9表达肿瘤的体细胞TLR9缺陷小鼠模型中,这种效应仍然存在,这表明由肿瘤细胞而不是宿主APC递呈抗原可能足以诱导强大的免疫反应。
TLR9激动剂Agatolimod(PF-3512676)已用于人体临床试验,包括三项联合局部照射和瘤内给药的试验。在接受治疗的45名惰性B细胞淋巴瘤患者和15名真菌病患者中取得了临床反应,包括一些完全反应。
CpG已被证明在非B细胞恶性肿瘤中也能诱导肿瘤消退。在小鼠神经胶质瘤模型中,瘤内注射CpG可以增加T细胞的渗透,消除肿瘤,并防止再次发生。在间皮瘤、乳腺癌和黑色素瘤的小鼠模型中,CpG注射也能启动类似的T细胞介导的抗肿瘤反应。在人类中,另一种TLR9激动剂Litenimod(CpG-28)作为肿瘤内注射给34例复发的多形性胶质母细胞瘤患者,取得了一些部分反应。
上述CpG分子被归类为CpG B型(CpG-B),因为它们最佳地激活B细胞。而CpG-C分子SD-101则旨在同时激活B细胞和浆细胞样树突状细胞(PDC)。在肿瘤内给药的临床前和临床试验中,SD-101显示出良好的效果,目前正在研究其在淋巴瘤和实体肿瘤中的应用,包括与抗PD1抗体的联合研究(NCT02521870,NCT02731742,NCT02927964,NCT03007732)。
如上所述,CD141+树突状细胞在肿瘤中的重要性在于其强大的交叉呈递抗原的能力,从而启动强大的CD8+ T细胞对肿瘤抗原的反应。这些细胞表达非常低水平的TLR7、TLR8和TLR9;然而,它们表达高水平的TLR3,这是一种位于内体的对双链RNA(dsRNA)有反应的PRR。由多聚赖氨酸和羧甲基纤维素稳定的多肌胞苷多胞酸(Poly-ICLC,又称Hiltonol)是一种稳定的双链RNA“宿主靶向”病毒模拟物,具有广泛的固有和适应性免疫增强作用。由于其强烈诱导I型干扰素(IFN)的能力,被证明是一种有前途的疫苗佐剂。
在癌症试验中,Poly-ICLC最初被用作干扰素诱导剂,具有可预测的高毒性。然而,在低剂量时,它显示出更广泛的宿主防御刺激、强大的佐剂作用,以及抗增殖和抗病毒作用。
Poly-ICLC的抗肿瘤和抗病毒活性被认为依赖于其对TLRs和MDA5(另一种细胞质PRR)的刺激,伴随着IFN和其他细胞因子的诱导以及对MHC分子的诱导。同样,dsRNA诱导各种共刺激因子如B7-H2、CD40和OX40,这些可能有助于克服肿瘤的免疫逃逸。
在多种小鼠肿瘤模型中,Poly-ICLC的给药已被证明可以延长生存期。在小鼠淋巴瘤模型中,腹腔注射Poly-ICLC显著延长了生存期,并与腹膜巨噬细胞的肿瘤杀伤活性相关。Poly-ICLC还延长了胶质瘤、黑色素瘤和纤维肉瘤啮齿动物模型的存活率。Poly-ICLC被整合到基于多肽的胶质瘤疫苗中,显示了其诱导肿瘤浸润淋巴细胞和干扰素信号的能力。在宫颈癌小鼠模型中,Poly-ICLC作为E7 HPV肿瘤抗原的佐剂,显示了抗原特异性CD8+ T细胞的扩张和肿瘤的消退。
虽然单剂Poly-ICLC可以诱导肿瘤反应,但我们团队在小鼠淋巴瘤A20模型中开发了一种联合方法。在该模型中,Poly-ICLC在低剂量辐射和瘤内Flt3L治疗后用于激活瘤内DC。尽管这种方法在大约三分之一的动物中诱导了肿瘤消退和治愈,但增加检查点阻断和抗PD-1单抗的使用,可以导致几乎所有肿瘤的消退。这进一步支持了通过诱导瘤内炎症和调节免疫抑制的肿瘤微环境来实现最佳抗肿瘤免疫反应的重要性。
Poly-ICLC已被用于数十个多发性实体恶性肿瘤和淋巴瘤的临床试验,并且更多的临床试验正在进行中,这些试验结合了化疗、放疗和/或其他免疫佐剂。虽然临床成功各异,但数据表明,Poly-ICLC能够诱导对肿瘤抗原的免疫反应。基于这些和其他对人类的研究,Poly-ICLC因此成为多种癌症和HIV疫苗的特别有效的免疫佐剂,因为它在增强抗原摄取、交叉呈递和将肿瘤抗原免疫反应向Th1表型倾斜方面发挥了辅助作用。
在一项对22名复发性恶性胶质瘤患者的试验中,使用了体外负载合成TAA多肽的自体DC,同时肌肉内注射Poly-ICLC,结果显示强大的抗原特异性T细胞反应,并提示延长了生存期。在晚期卵巢癌患者中进行的另一项基于多肽的疫苗试验中,研究人员将来自NY-ESO-1的重叠长肽与Poly-ICLC结合使用。虽然这种多肽单独没有诱导免疫反应,但在接受Poly-ICLC的11名患者中,有10名患者的NY-ESO-1特异性抗体和抗原特异性T细胞反应显著增强。
另一种表达NY-ESO-1的多种肿瘤类型的疫苗通过将肿瘤抗原与在DC上表达的DEC-205的抗体连接,将全长NY-ESO-1蛋白附着在DC上。这种抗体-多肽结合物与Poly-ICLC联合使用,结果显示该佐剂耐受性良好,并在一小部分患者中观察到转移性疾病的显著临床消退。另一项对癌症睾丸抗原MAGE-A3类似处理的患者进行了全肽和Poly-ICLC治疗,随后进行了自体干细胞移植和体外扩增T细胞过继转移,结果在接受治疗的25名患者中,超过四分之三的患者出现了细胞和体液抗原特异性反应。
目前正在进行单独和联合使用Poly-ICLC进行瘤内注射,以实现原位疫苗接种的研究。在一项针对转移性恶性肿瘤患者的单剂瘤内Poly-ICLC试验中,一名晚期面部横纹肌肉瘤患者出现了显著的瘤内炎症和坏死,随后肿瘤显著消退。
在另一项旨在增强非范围效应的研究中,瘤内注射重组Flt3L和Poly-ICLC与低剂量放射治疗相结合。早期报告显示,在一些晚期滤泡性淋巴瘤患者中,肿瘤内树突状细胞增加,治疗后的肿瘤和全身疾病消退。鉴于最近的临床前研究结果证明了这种方法与检查点阻断相结合的有效性,即将开展的新研究将探讨这种瘤内ISV方法与全身抗PD1单抗联合使用的效果(Fig.28.2)。
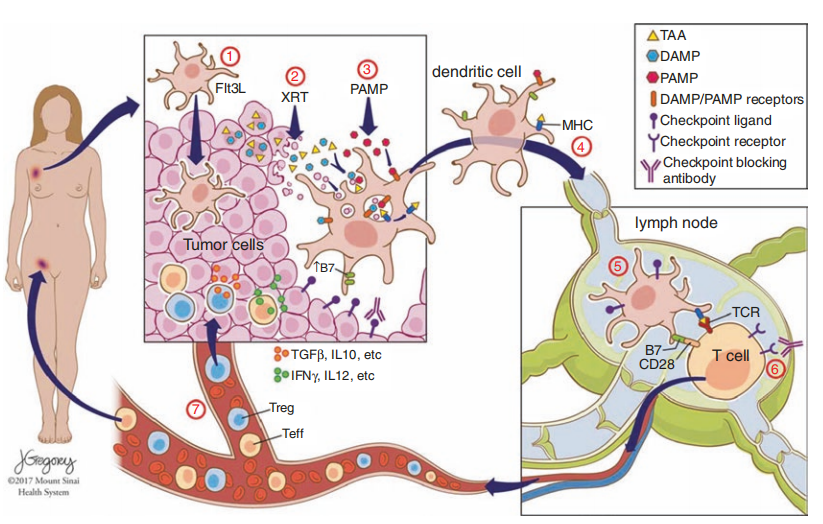
Fig 28.2 新的ISV方案。瘤内注射Flt3L诱导树突状细胞(DC)的招募;低剂量辐射使树突状细胞吸收抗原;瘤内注射PAMPs(如Poly-ICLC)激活树突状细胞;激活的树突状细胞迁移到引流淋巴结;在引流淋巴结中,树突状细胞与肿瘤抗原特异性T细胞相遇并激活它们;衰老或耗尽的肿瘤特异性T细胞的激活阈值可以通过添加检查点阻断(如抗PD-1单抗)来克服;激活的T效应细胞进入全身的肿瘤部位,发挥系统性抗肿瘤作用,并促进肿瘤特异性记忆的形成。
28.5 调节免疫抑制细胞亚群
虽然我们迄今介绍的大多数单一疗法和联合疗法能够在一小部分患者中诱导肿瘤特异性T细胞反应,但许多患者对这些疗法仍然难以产生效果。这可能是由于T细胞反应被肿瘤微环境中的其他因素所抑制,例如髓系细胞和淋巴样细胞亚群的强大免疫抑制作用。肿瘤细胞通过分泌免疫抑制趋化因子和细胞因子以及直接细胞接触,促进免疫抑制树突状细胞、肿瘤相关巨噬细胞(TAMs)和髓源性抑制细胞(MDSCs)的发展和募集。这些白细胞与免疫抑制共刺激配体和肿瘤细胞表达的细胞因子协同作用,限制对肿瘤细胞的免疫反应。因此,为了有效地诱导针对肿瘤抗原的免疫反应,可能需要破坏这种免疫抑制环境(Fig.28.3)。
调节效应T细胞反应的关键细胞是调节性T细胞(Tregs)。大量文献表明,肿瘤细胞通过分泌趋化因子招募肿瘤内的Tregs,这些趋化因子损害T效应细胞的增殖,削弱其脱颗粒和细胞毒活性。正如前面提到的,某些化疗药物(如环磷酰胺、蒽环类药物和铂类药物)不仅对癌细胞具有细胞毒作用,还优先耗尽Tregs,而对效应T细胞的影响较小。在接受化学免疫治疗的患者中,一项研究表明,CD8+和NK细胞的数量和功能迅速恢复,而CD4+细胞,特别是Tregs,在长达一年的时间里仍处于耗尽状态。
虽然化疗可以在疫苗接种前起到调节作用,但大多数药物也可能阻碍最佳的淋巴细胞反应。因此,为了更有针对性地耗尽Tregs,一些疫苗试验加入了Daclizumab,这是一种人源化的抗CD25抗体,可以耗尽Tregs。虽然这些早期试验的最终临床效果有限,但这种治疗有效地耗尽了循环中的Tregs,可以考虑与其他组合免疫疗法或疫苗方法一起使用。
与肿瘤细胞类似,肿瘤相关巨噬细胞(TAMs)和髓源性抑制细胞(MDSCs)表达高水平的抑制性表面抗原,包括PD-L1,并通过细胞因子和直接调节使肿瘤内的T细胞衰老或失去最佳的细胞毒效应功能。它们的存在和普遍性与不良预后密切相关并不令人惊讶。尽管MDSCs和TAMs缺乏允许靶向的抗原特异性表面标记,但Bruton酪氨酸激酶(BTK)在MDSCs中表达,而用Tec-Kinase抑制剂伊布替尼治疗小鼠和人类MDSCs显著损害了这些细胞的迁移和免疫抑制细胞因子的产生。
虽然伊布替尼最初是针对BTK开发的,但它也作用于其他Tec家族的激酶,如IL-2诱导的T细胞激酶(ITK),这使T细胞向效应表型倾斜,从而进一步对抗免疫抑制微环境。这种免疫抑制途径的阻断在最近的一项基于CpG的ISV临床前研究中进一步得到验证,显示伊布替尼增强了抗肿瘤反应。目前,伊布替尼正与包括检查点阻断抗体在内的各种免疫调节化合物联合使用,取得了良好的临床反应。
其他免疫调节化合物的临床和临床前研究也显示出希望。例如,来那度胺在疫苗方案中可能起到佐剂作用。一项观察癌细胞直接免疫抑制活性的临床前试验发现,肿瘤浸润性淋巴细胞(TIL)在与恶性细胞孵育时,与淋巴瘤细胞的免疫突触形成受损,从而阻断了T细胞的细胞毒活性。而这种突触形成的缺陷在用来那度胺治疗后得以逆转。
最近关于来那度胺联合利妥昔单抗治疗淋巴瘤的研究发现,这种组合增加了ADCC介导的杀伤力。多发性骨髓瘤的试验表明,当与来那度胺一起使用时,PD-1阻断的效果有所改善。将来那度胺与各种免疫疗法结合使用的临床试验正在进行中,包括血液系统和非血液系统的免疫疗法。
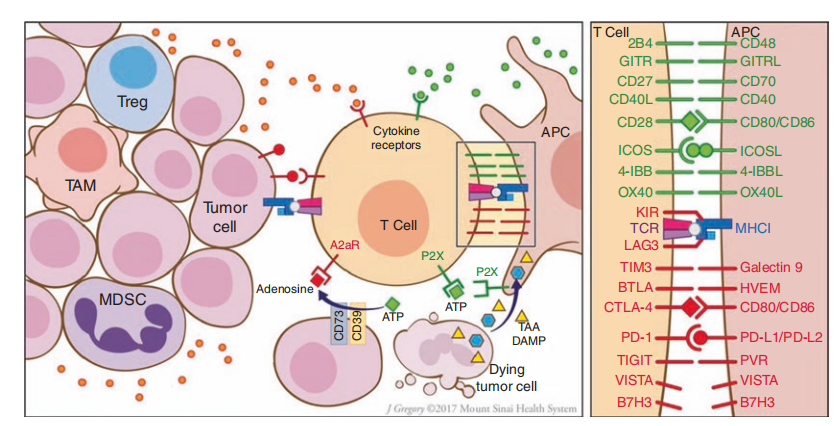
Fig 28.3 调节肿瘤微环境的刺激和抑制成分。右图显示了T细胞和抗原提呈细胞(APC)之间的界面,这在许多方面反映了T细胞和肿瘤细胞之间的配体-受体相互作用,提供了许多可靶向的共刺激和抑制配体。此外,肿瘤细胞和被招募的免疫抑制细胞(如Tregs、TAMs和MDSCs)通过释放细胞因子来扭曲效应反应,并通过激活的损伤相关分子模式(DAMPs)转化为抑制性腺苷,从而促进免疫逃逸。
总结
癌症免疫治疗领域正在迅速发展,许多新的检查点阻断抗体和激动型抗体正在进行临床试验。虽然这些疗法提供了巨大的希望,但我们从CTLA-4和PD-1阻断的研究中知道,具有炎症特征的肿瘤对免疫介导的治疗最为敏感。因此,局部免疫疗法(如ISV方法)专注于将抗原提呈细胞(APC)引导至肿瘤,并结合检查点激动剂/拮抗剂、酪氨酸激酶抑制剂或其他免疫调节药物,刺激免疫原性细胞死亡和炎症途径。这样的组合疗法可能会提高临床应答率,并实现更持久的免疫记忆。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 郑梦怡
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab