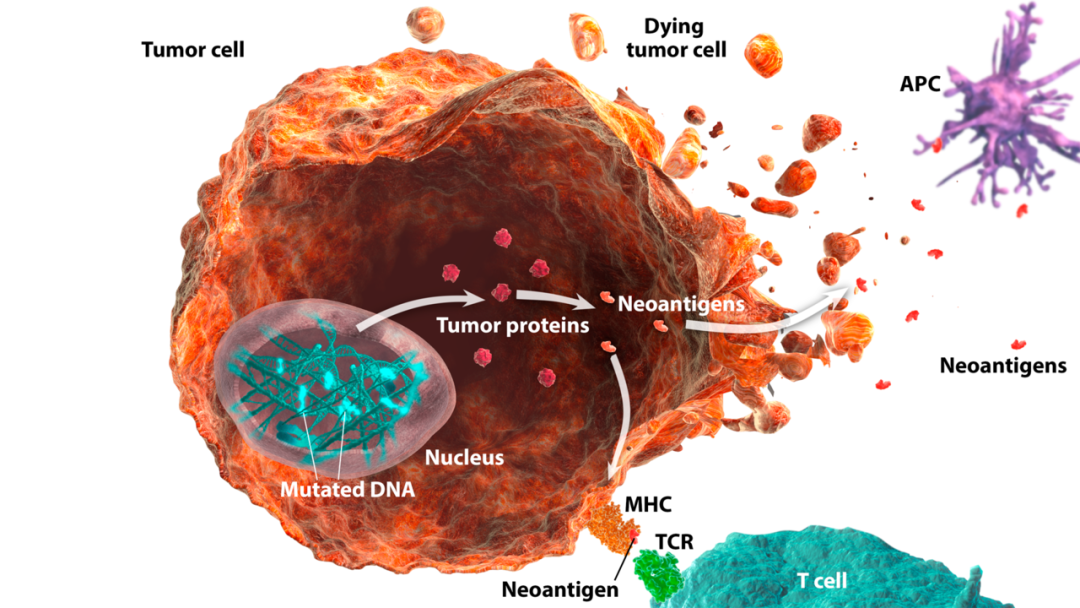
4.4 新表位特异性免疫反应的临床意义
新表位特异性反应在免疫检查点阻断疗法中的临床价值最为明显。抗PD-1和抗CTLA-4单抗治疗黑色素瘤和非小细胞肺癌的病例报道表明,新抗原诱导的CD8+T细胞的应答(基于TCR识别突变肽的多样性)与临床应答有关。例如转移性黑色素瘤或非小细胞肺癌(NSCLC)患者的T细胞反应,可通过对新表位的PD-1+循环T细胞的数量(通过流式细胞仪显示)和患者的临床检测得出该结论。此外,临床观察表明,外周血中的新表位特异性免疫反应可以作为几种实体肿瘤的预后标志物。
与感染相关的炎症引起的组织疤痕可能导致遗传畸变,随着时间的推移可能会导致肿瘤发生。对肺部感染过结核分枝杆菌的肺腺癌患者的观察表明,分枝杆菌抗原(“旧的”结核病变)的免疫反应导致编码表皮生长因子受体(EGFR)的基因发生突变,而该突变与癌症的发生有关。更引人注目的是,与那些在癌症诊断时没有肺部“旧”结核病灶的患者相比,这些有肺部“旧”结核病灶的患者的1年生存预后更差。但患有“陈旧性结核病变”和同一肺腺癌的患者没有EGFRL858R突变(发生在EGFR基因的第21外显子,它编码受体的细胞内酪氨酸激酶结构域),这一现象与接受酪氨酸激酶抑制剂Gefitinib治疗的肺癌患者的阳性临床结果有关。EGFRL858R突变已被证明是在接受Gefitinib治疗的NSCLC患者中产生新的表位,可诱导产生抗体反应。而另一种EGFR 相关突变,EGFRT790M,研究发现在大约60%的NSCLC患者中存在这种突变,这种突变可以产生HLA-A2限制性的新表位,这些新表位与有利的抗肿瘤免疫反应相关,可用于设计更优的免疫疗法。
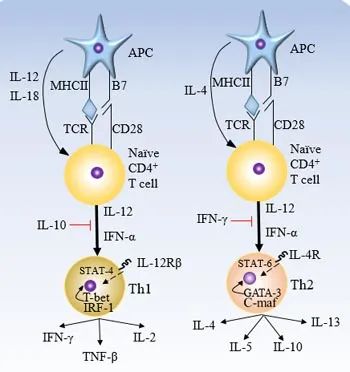
多肽的激活性是它们刺激T细胞活化的能力,实际上可以因其分子结构的突变变化而改变细胞免疫反应环境。Paul Allen和他的同事在20世纪90年代中期证明,葡萄球菌肠毒素A的多肽类似物(来源于血红蛋白的葡萄球菌肠毒素A)在消除效应的同时,还能抑制辅助性T细胞(Th1或Th2表型的CD4+T细胞)的增殖。虽然血红蛋白肽中的一些突变抑制了T细胞的增殖,但其他的突变对T细胞没有有害影响。进一步的研究表明,免疫受体酪氨酸激活基序(ITAM)的部分磷酸化是细胞内TCR Zeta(ζ)链中不可缺少的组成部分,在免疫突触过程中可以完全消除T细胞反应甚至导致T细胞死亡。重要的是,这种现象可能是由于TCR与呈现突变多肽的HLA分子的结合,更重要的是,突变本身的性质和突变在表位序列中的位置。不可否认的是,癌症病变(如慢性感染)中的局部炎症环境也可能导致染色体畸变,导致TCRζ链的明显下调或丢失。这些具有开创性的发现首先在结肠癌的临床前小鼠模型中被报道,后来在肾癌患者的TIL和非霍奇金淋巴瘤患者的外周血T细胞中也有报道。
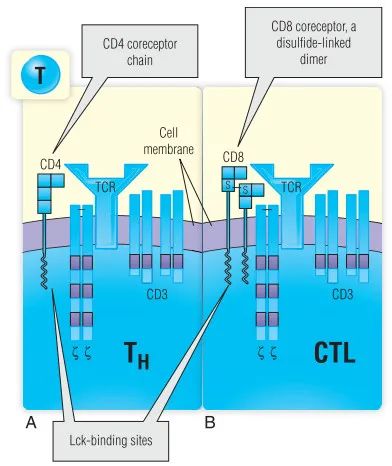
感染性疾病模型的临床前研究可能提供一个关于TCR谱系形成与新表位特异性免疫反应相关的思路。对腹腔感染甲型流感野毒株(HK/PR8)的小鼠脾和支气管肺泡灌洗液中衍生的T细胞的分析表明,动物的CD8 TCRVβ谱系是由一次病毒攻击形成的,能够有效地识别和响应另一种野毒株的二次攻击,而不是其他任何一种病毒的变异版本(HK/PR8-NPN3A)。此外,虽然野生型病毒株的攻击提供了更广泛的TCRVβ库,但病毒的突变毒株诱导了更集中和狭窄的抗原特异性T细胞亚群,具有微妙的TCR重排模式。
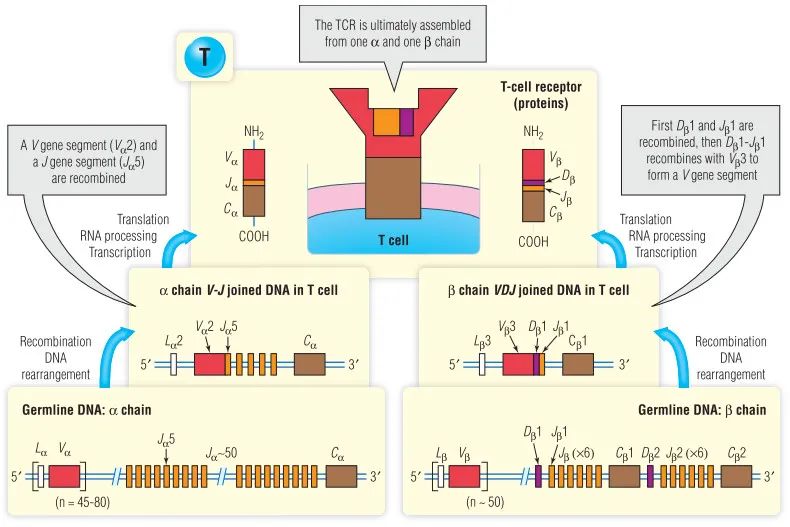
此外,野生型病毒(NP366,ASNENMETM)的免疫原性表位在突变病毒株诱导和再攻击的小鼠中诱导了可测量的CD8+T细胞反应。相反,NP366表位的突变版本(NPN3A366,ASAENMETM)只含有一个氨基酸变化(NPN3A366,ASAENMETM),并不能促使野生型病毒攻击小鼠的T细胞间MHC和TCR之间的强结合,从而显示出高“失败率”(很大比例的含TCR的突变表位四聚体在最短的时间内从TCR解离),从而需要更多地依赖CD8与MHC的联合受体结合来激发免疫反应。这与癌症的免疫反应有关;T细胞对新表位的反应性可能由于HLA限制性元件和TCR之间的结合动力学不佳而减弱。然而,用更广泛的个性化新表位接种疫苗可能有助于启动免疫系统,以重新唤醒对肿瘤有反应的较小数量的中央记忆T细胞,或者在不是相互排斥的情况下,产生新的(尚未激活的)抗原特异性T细胞池。
4.5 利用基础免疫学改进临床免疫治疗方法
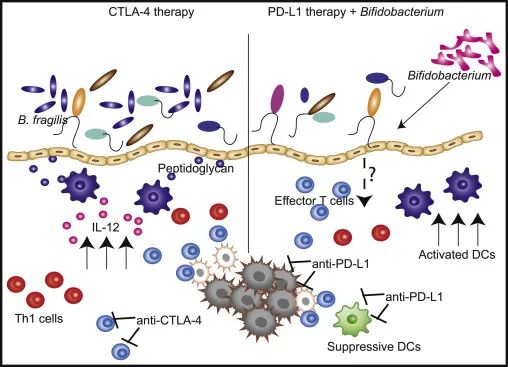
肠道共生细菌对健康和疾病中免疫反应的形成(和重塑)的影响一直是当前免疫学研究的核心。最近研究表明,在转移性黑色素瘤患者中,抗CTLA-4治疗诱导T细胞对部分“免疫原性”肠道细菌(如Thetaiotaomicron和B.Fragilis)产生免疫应答,此过程与临床疗效相关。在对肿瘤高度敏感的小鼠模型中,引入双歧杆菌,显著改善了对肿瘤负荷的细胞毒性淋巴细胞依赖性的控制。双歧杆菌接种结合抗PD-L1单克隆抗体注射,进一步加强了这些动物的肿瘤控制,从而强化了肠道微生物区系在决定抗癌免疫反应中的关键作用。因此,用免疫阻断疗法或T细胞免疫疗法补充肠道细菌中的生物活性物质可能会潜在地改善晚期癌症患者的新抗原特异性免疫反应。
靶向激活CD8+T细胞脂肪酸氧化(FAO),促进细胞记忆维持的小分子和细胞因子可作为癌症和感染性疾病主流治疗方案的辅助手段。例如,抗糖尿病药物二甲双胍激活了5′-腺苷一磷酸活化蛋白激酶(AMPK),并改善了FAO在记忆CD8+TIL中的作用,在化学诱导的皮肤癌小鼠模型中证实有效。IL-15通过上调线粒体生物合成和诱导肉碱棕榈酰转移酶的表达来促进脂质代谢,肉碱棕榈酰转移酶是线粒体β-氧化的关键酶。这一过程已被证明在小鼠的记忆CD8+T细胞中上调,并提高了它们的存活率。在肿瘤治疗中,IL-15已被评价为一种辅助佐剂,对TIL的增殖和增强肿瘤抗原特异性T细胞的细胞毒活性有显著作用。
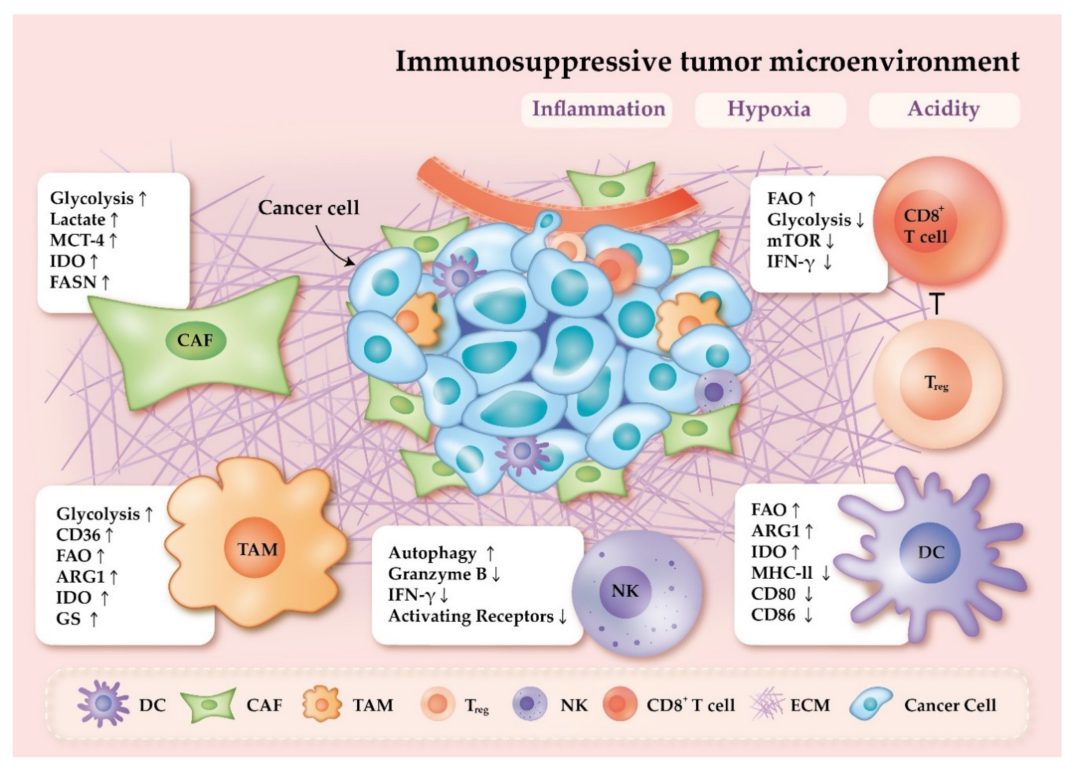
T细胞的免疫耐受性对于预防明显的病理状态是必要的,而Treg数量的增加对基于细胞的免疫疗法的成功具有重要意义。虽然输注间充质基质细胞来下调严重炎症后会产生转化生长因子-β并激活Treg,但回输到肿瘤患者体内的T细胞产品只允许含有最低限度的Treg亚群,以优化癌症特异性T细胞介导的抗肿瘤活性。此外,肿瘤微环境中慢性炎症时产生的IL-17可以诱导转化生长因子-β的产生,抑制CD8+T细胞的反应。TAA也可以刺激Tregs,即给予NY-ESO-1/ISCOMATRIXTM治疗性疫苗的黑色素瘤患者的NY-ESO-1157-170特异性Treg反应;NY-ESO-1119-143和TRIG-334-48(来源于另一种癌症睾丸抗原,癌症/睾丸抗原家族24)可以诱导黑色素瘤患者Th1细胞和FoxP3+ Tregs的增殖,从而促进免疫应答。需要更多的研究来更好地理解某些突变是否代表针对癌症突变的Tregs的名义上的表位。
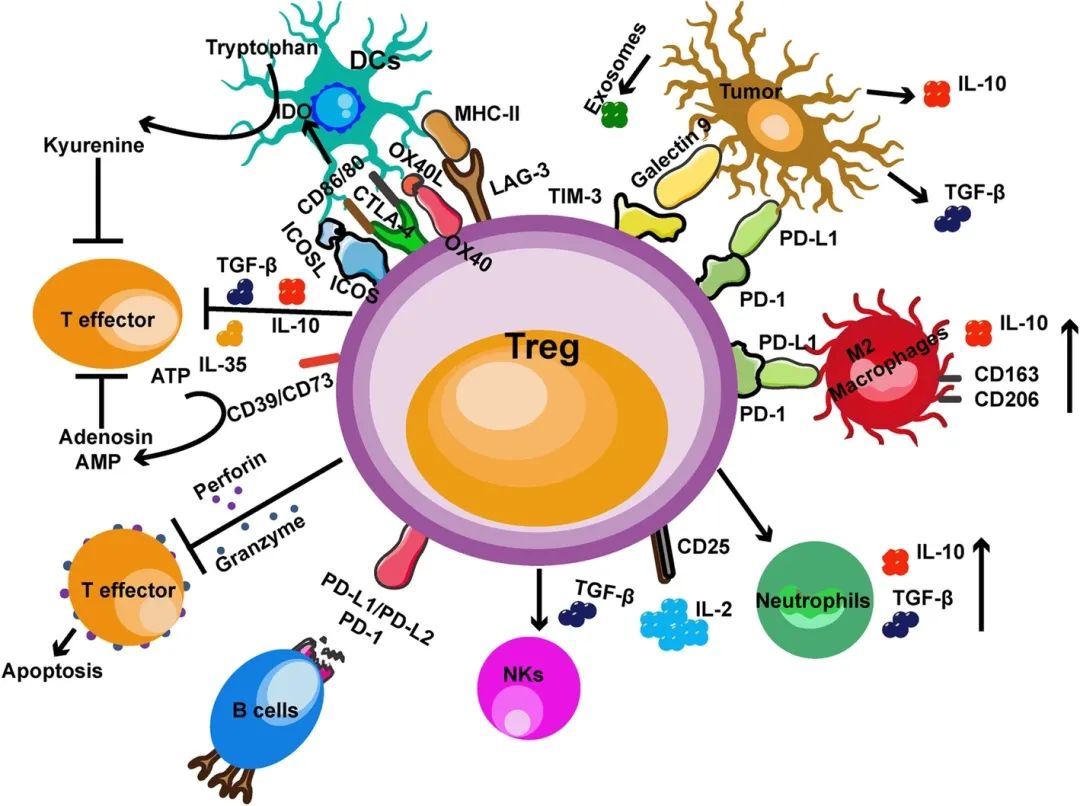
基础研究产生的新信息需要考虑纳入T细胞产品的临床前评估。例如,CNC Homolog 2(BACH2)是一种转录因子,它可促进宿主中调节性和中央记忆性T细胞的生成和维护,同时抑制免疫效应器机制,因此BACH2以及BTB结构域可能是表征T细胞群体的有用工具,这些T细胞群体可能会持续存在于患者体内,以对抗转化的细胞。缺乏BACH2的小鼠能够在肿瘤微环境中产生强烈的T细胞反应(以CD4+和CD8+ T细胞增殖和干扰素-γ产生为标志),伴随着FoxP3+调节性T细胞数量的减少,这随后将改善对肿瘤的控制。BACH2缺乏还增加了颗粒酶和穿孔素等细胞毒分子的基因转录。从翻译的角度来看,这一发现对增强靶向细胞免疫治疗中T细胞介导的抗肿瘤效应有直接意义。调节病变组织中新抗原反应性T细胞(即TIL)和外周血T细胞中BACH2的表达,可以提高免疫细胞的质量和疗效。
利用新的技术平台在疾病组织中筛选特异性TCR,即深度(TCR)测序、肽微阵列、细胞微阵列和TCR表位对接研究,对于我们目前对疾病机制和免疫动力学的研究有很大贡献。这可能使我们能够更详细地描述对抗癌的长期免疫保护至关重要的免疫谱系。将数学知识和对肿瘤动力学以及肿瘤进展算法的生物学理解结合起来,将对这一领域大有裨益。此外,使用这些技术对健康个体和患者的不同解剖部位的临床样本进行比较研究,为下一代生物疗法的开发提供新的信息。
TIL和PBMC中TCR的差异,以及癌症患者的突变负荷与检查点抑制剂的成效有关。在转移性黑色素瘤和非小细胞肺癌患者中很明显,他们的突变负荷最高,对抗PD-1和/或抗CTLA-4治疗反应良好。“挖掘”针对癌症突变的生物学和临床相关的TCR可能导致通过克隆和转移特定的TCR到PBMC来产生用于治疗的T细胞产品。
这些例子突显了一个已经讨论了几十年的话题的重要性,例如在针对HIV的细胞免疫反应领域:针对突变表位的定制免疫反应应该给予多少关注和提供多少多样性?考虑到(1)原发肿瘤的突变与复发的相似性;(2)原发肿瘤和远处转移所表现出的突变多样性;(3)基因表达的“局部”印记(并非所有编码DNA的基因都可能完全或在某些点被翻译成RNA,然后再转化成蛋白质),与组织环境(如肺和肝转移)有关。
这些问题将代表临床相关研究的问题,并对生物学和临床相关研究的设计产生影响。例如,如果TIL在临床检测到复发时可以立即从原发肿瘤获得,那么应该考虑原发肿瘤与相应复发恶性肿瘤的相似性和差异性。
对于癌症抗原的体液免疫反应,它在介导患者临床相关和有益的抗肿瘤反应方面的重要性需要更多的重视。沿着这些思路,肽微阵列的研究有利于发现血清中循环抗体识别的自然呈现的表位以及来自患者的B细胞的表位的敏感性和特异性。在癌症患者的血清中,疾病相关表位可能包括属于新抗原的表位,并且可以利用高含量的肽微阵列(HCPM)平台进行筛选。HCPM是一种新的技术,可用于分析许多研究领域的抗体,该技术是最近开发的,目的是对血清中众多表位的反应性进行客观的观察。这项先进的技术可以在每个单独的微阵列载玻片上显示290万个对应于独特表位的肽序列(点)。仅使用少量样本(即每张玻片4μL的生物流体),就有可能在包含整个人类蛋白质组的HCPM微阵列芯片上以高度详细的16聚肽的水平识别相关端点的免疫识别模式。HCPM平台在芯片设计、预处理和分析方法以及技术方面有着丰富的使用经验,在各种临床环境中的不同应用也有一定经验,如细菌感染、病毒感染、结节病和百日咳,这些有力地表明该平台还能够获得针对突变型和野生型靶分子的特异的血清反应性。这项技术还可以用来检测癌症患者外周血中对“私有”新表位的体液免疫反应。HCPM研究的结果有助于开发新的基于抗体的疗法,包括识别CARS的新的且与临床相关的癌症相关靶点,或者通过ADCC增强针对(细胞内)突变抗原的细胞免疫反应。另一方面,疾病中的B细胞依赖性免疫反应可能有助于调节T细胞驱动的“免疫病理”环境,如在移植后淋巴增生性疾病(PTLD)患者中观察到的那样。早期对癌症相关抗原的研究和鉴定支持这样一种假设,即癌症患者中存在强烈的B细胞反应,即存在强烈的抗癌T细胞反应。例如,癌症睾丸抗原MAGE或NY-ESO-1+,它们是临床上相关的T细胞靶点,通过B细胞反应被鉴定出来,目前被用于临床方案,以诱导针对NY-ESO-1+癌症病变的疾病修饰性T细胞反应。
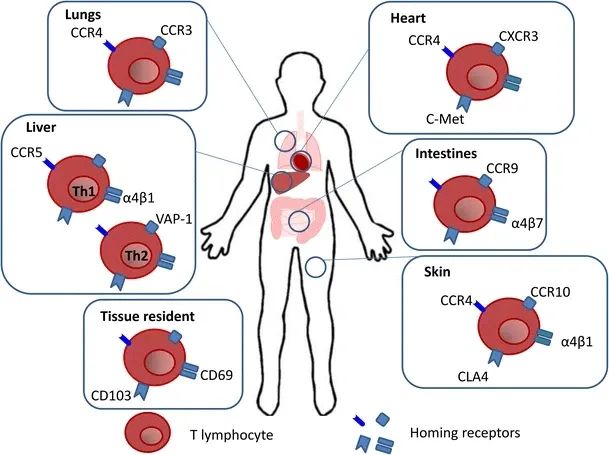
哪里可以获得抗突变的反应性的T细胞?来自外周血液的免疫细胞表达其表面的组织特异性归巢标记(如用于中枢神经系统的VLA-4,用于肺部的CXCR3,用于肠道的CCR6),可用于测量来往于相应目标器官的外周血单个核细胞(PBMC)之间的循环T细胞。例如,VLA-4+T细胞的富集将导致T细胞往返于患者的肿瘤病变,然后可以检测T细胞对新表位的识别和针对转化细胞的潜在免疫反应性。此外,在靶器官中识别的一些表位与在PBMCs中观察到的识别模式重叠,另一些则不重叠,而是在PBMCs或TIL中被唯一识别。与此相一致的是,在20例HLA-A2+乳腺癌患者的肿瘤和血液样本分析中,15例患者中发现TIL和PBMC来源的T细胞具有18种相同的TCR特异性。2016年有报道称,TCR的互补决定区(CDR)3是与靶细胞上的HLA-肽复合物结合的复合物的一部分,在胶质瘤患者的PBMC和TIL之间差异很大。重要的是,该系列研究还发现,在伴有低级别胶质瘤的TIL TCR谱系中,外周血中存在一种独特的TCR信号,而胶质母细胞瘤患者则表现出更广泛的TCR选择。我们在胶质母细胞瘤患者中也注意到了这一点,其中一些体细胞突变可以被PBMC识别,但TIL不能识别,反之亦然。这些研究产生的信息已经转化为晚期癌症患者的临床产品,即将与更好预后相关的TCR谱系基因一同转移到PBMC中,在考虑到使用先进的基因转移技术的可行性的情况下,以重新输注作为辅助治疗。事实上,罗森博格博士在美国国立卫生研究院的团队已经使用针对新表位表达特定TCR的自体T细胞产品来治疗带有特定突变的晚期癌症患者。关键的例子包括用CD4+IFN-γ+TIL重新识别源自受体酪氨酸蛋白激酶erbB-2(ERBB2)或HER-2相互作用蛋白(ERBB2IP)的HLA-DQ*06限制性新表位来治疗转移性胆管癌患者和转移性结直肠癌患者,以及接受了针对KRASG12D突变(HLA-C*08*02限制性)驱动突变的TCR转移T细胞产物,随后表达KRASG12D突变的转移灶消退。后一种策略是通过对从10名转移性胃肠道癌症患者的肿瘤组织样本中分离出的TIL进行TMG筛查,以检测新表位特异性反应性。携带HLA-C*0802等位基因的患者对他们的肿瘤细胞有TIL反应(针对KRAS),这表明患者体内的限制性HLA元件可能会限制KRAS的治疗靶向,因为其他(KRAS)突变可能对细胞免疫系统不可见,且这些突变可能不是自然处理的,最终会呈现给患者的细胞免疫谱系。
识别和验证临床上和生物学上相关的新表位仍然是一个挑战,即表位是否以代表性的方式表达,它们是否在肿瘤细胞上被加工和呈递,以及是否有“合适的”TCR谱系可用并能够对其产生反应-导致免疫效应功能,从而最大可能地促进强大和持久的抗肿瘤免疫反应。一种可能的方法是根据癌症患者的全基因组序列设计和产生潜在的新表位。一旦这些新表位被化学合成,它们就可以被提交给T细胞培养的大规模体外筛选,以便仔细挑选高质量的突变特异性T细胞,这些T细胞可以扩增并重新注入患者体内。以非互斥的方式,可以克隆仅针对突变型TAA而不是野生型肽的序列的TCR,并随后将其转移到受体靶细胞(T细胞)中,用于癌症患者的主动细胞治疗。
PBMC可以作为一个非常好的起点来筛选患者体内循环(和再循环)的新表位特异性T细胞群体。罗森伯格研究小组指出,外周T细胞能够识别突变表位/新表位的事实是,PD-1+T细胞群体富含肿瘤新抗原特异性T细胞,这更多地反映了接触过抗原的T细胞的谱系,而不仅仅是“耗尽”的T细胞。这与早期转移性黑色素瘤患者的TIL研究结果相呼应:PD1+TIL识别肿瘤细胞突变。然而,肿瘤病变的异质性还需要进一步研究,包括对“突变体多样性”的解剖学研究,以及从单个癌症病变中可获得的相应免疫效应细胞的多样性。针对共有或私有突变的TCR转移的一个要点是,呈现癌症表位的HLA限制性元件因个体不同而不同。因此,并不是所有的患者都能从单一的TCR-HLA匹配的T细胞产品/TCR转移中受益,而是一种更个性化的方法,考虑到新的表位结构、相应的TCR序列以及HLA限制元件。这方面的一个例子是与EB病毒(EBV)诱导的炎性T细胞反应相关的PTLD的发生。具有HLA-A2、A11、B5、B18、B21、Bw22和B35背景的个体比具有HLA-A03或HLA-DR7(CD4+T辅助细胞反应)遗传背景的个体在实体器官移植后发生PTLD的风险更大,而具有HLA-A1、B8或DR8背景的个体似乎对PTLD具有保护作用。在乙型肝炎病毒(HBV)诱导的肝细胞癌患者的靶向免疫治疗中,也要仔细选择特异性TCR和HLA限制,重点是HBV特异性表位和潜在的新表位。
荷兰癌症研究所的Ton Schumacher研究小组最近表明,由于肿瘤患者自然产生的新表位特异性T细胞反应可能会被沉默,而且从健康人的外周血液中分离出的T细胞可能含有识别新表位的TCR,后一种选择可能代表着产生抗突变表位反应性T细胞的起点。CTL系识别5种不同的HLAA2限制性新表位,从不同健康供者的PBMC中建立,并对表达同源(突变)T细胞表位的患者来源的黑色素瘤细胞株产生干扰素-γ和/或CD107a。此外,识别新表位的T细胞和肿瘤细胞表达的表位表现出很强的肽-β结合动力(MHC-class I-HLA2微球蛋白-表位相互作用的半衰期),然后可以克隆并异源表达一个针对突变特异性T细胞量身定做的“改进的”TCR谱的人的T细胞。这已经在癌症患者的PBMC中被证明,使用来自MHC型相合捐赠者的T细胞,在临床上被证明在感染性疾病的背景下是可行的,即通过在异基因造血干细胞移植后将CMV特异性T细胞从与HLA I类限制性等位基因相匹配的同种异体捐赠者转移到CMV感染患者(和无功能的免疫系统)。此外,使用HLA-I类匹配的TIL(见Table 4.2)也产生了类似的观察结果,这些TIL被证明对来自HLA-B*2705匹配患者的自体肿瘤细胞上识别的突变的靶表位有反应(即没有重新刺激和扩增),这表明,即使在TIL中,前体T细胞也存在,在暴露于“驱动”突变(即KRAS、Smad4、P53或甚至是个体之间共同的突变)的表位之后,在TIL中也会产生类似的结果。
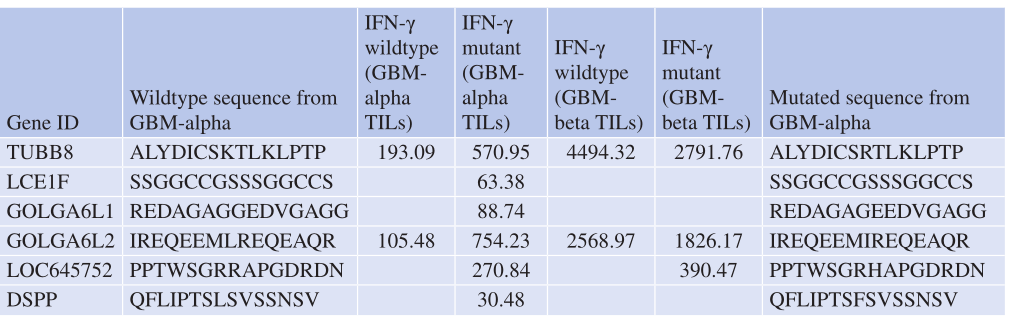
Table 4.2 MHC-I相匹配的不同患者的TIL突变表位的共同识别
做好准备:增强应对突变体靶点的TCR库
使用标准抗癌药物(即吉西他滨、地西他滨、顺铂和阿霉素)激活先天免疫可以促进巨噬细胞和树突状细胞等抗原提呈细胞的激活,并促进抗原处理、激发促炎免疫反应,即产生IL-12。此外,地西他滨的化学免疫治疗也被证明能诱导CD8+ T细胞介导的强大的抗癌细胞毒反应,而与单独化疗相比,它与细胞因子激活的杀伤细胞一起用于胰腺癌患者可以提高无进展生存率。辅助癌症治疗后的新抗原特异性细胞免疫反应的增加尚未进行深入研究,但可能是未来评估的重点——旨在提高患者突变体对其免疫谱系的“可见性”。抗癌免疫反应可以通过“标准治疗手法”增强的一个强有力的论点是,在接受全脑放射治疗(WBRT)的脑转移患者中,免疫反应被激活,导致远处病灶的肿瘤消退。晚期黑色素瘤相关脑转移患者在WBRT的基础上加用伊匹单抗(抗CTLA-4)似乎有更大的生存优势。沿着这些思路,对放疗诱导的CTL反应的临床前评估表明,随着HLA-I类抗原处理和呈递的改变,突变的格局发生了变化,随后伴随着对肿瘤负担的加强控制。
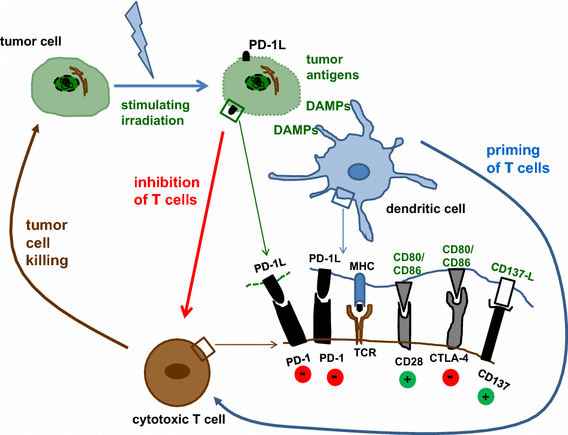
一般而言,电离辐射可促进免疫刺激事件,如(1)增加HLA分子表达,MHC-I表达,(2)产生与细胞毒性T细胞识别有关的特异性多肽,(3)通过释放肿瘤相关抗原促进细胞毒性T细胞活性。后一种过程导致效应细胞的激活和运输,促进原位细胞免疫反应,尽管也可能发生远距离反应。在这个特殊的背景下,剂量和分级似乎在诱导抗肿瘤免疫效应方面起着决定性的作用。Demaria组在乳腺癌和结肠癌模型上的临床前研究显示,除CTLA-4阻断外,联合局部分割放疗方案(8gy×3,6gy×5)有明显的抗肿瘤T细胞反应的迹象,其他临床前/临床研究能够支持这种联合方法的相关性。考虑到单克隆抗体对CTLA-4和PD-1调节的免疫抑制作用在转移性非小细胞肺癌、黑色素瘤和肾癌中的抑制作用,进一步研究辐射对局部和远处的潜在辅助作用是必要的。Postow等人报道了一例被诊断为转移性黑色素瘤的患者,用伊匹单抗治疗;在一个阶段,患者接受了低分割放射治疗,以治疗椎旁转移;患者接受了28.5Gy的治疗,分3次进行,为期7天。4到5个月后,椎管旁肿块和一组先前发现的远处肺门淋巴结病变和脾脏病变(不是放射靶点)明显减少。治疗10个月后CT仍显示病情稳定。在更大的患者群体中再现这些效应需要考虑许多生物学和临床变量,其中包括能够提供关于辐射诱导的免疫反应的定性和定量预测数据的数学模型。甚至可以反映“突变负荷”和T细胞浸润的图像分析也可能提供一种预测工具,同时也是一种用来衡量针对突变抗原的T细胞反应应该如何“集中”和缩小或扩大的工具(见Fig 4.3),以便提供更高的存活率。
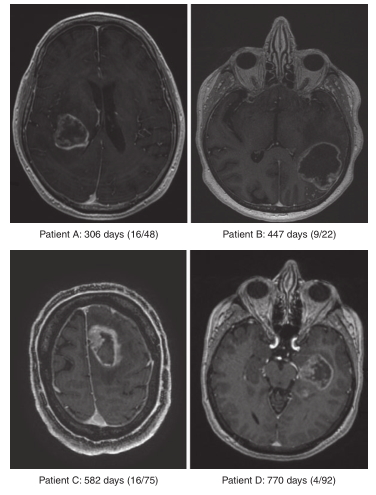
Fig 4.3 对4例胶质瘤患者(WHO分级为4级)进行MRI扫描,以(I)术后数天的存活时间和(Ii)患者TIL所识别的突变表位数(由IFN-γ产生所确定的突变表位数与所识别的突变总数之比)为指标。集中的TIL应答似乎与提高存活率有关,这一观察结果需要在更大规模的研究中进行随访。
尽管数据表明非常集中的免疫识别在临床上更有利(根据存活率定义),但需要进行更多的基础和临床研究,以可视化突变负荷、识别的靶点数量、定制T细胞移植物靶向突变的可能性以及随后的临床反应性之间的联系。因此,在放疗和免疫检查点阻断联合治疗后,患者体内新表位特异性T细胞的激活是改善临床结果的关键,因此值得在有着良好控制的临床环境中进一步探索。对新抗原反应性T细胞表面组织归巢标记和记忆标记的全面分析,这些分析的结果与患者转移的解剖位置之间的关系,以及与T细胞的功能的关系对于丰富我们对癌症靶向细胞免疫治疗的理解是至关重要的。从接受治疗的患者身上获得的临床样本可以进行这些免疫学分析,即在“标准”或免疫治疗策略期间的不同时间点抽取的外周血液。进一步优化靶向T细胞治疗的另一个主要难题是缺乏对抗原处理和提呈的理解,即哪些表位是自然提呈的,它们各自的组织表达模式是什么,它们相应的HLA限制以及它们驱动抗原特异性T细胞反应的能力,基于能够对单个突变的靶表位发生反应的TCR谱系。对抗原特异性T细胞群体的“免疫学适应性”的进一步研究可能会影响基于细胞的治疗的效果,并进一步帮助定制T细胞产品。例如,T细胞治疗癌症、病毒感染和自身免疫性疾病的最新进展突出了工程T细胞的广泛治疗潜力。尽管人类原代T细胞的位点特异性遗传操作仍然具有挑战性,但它们在定制T细胞产品方面有着巨大的临床前景,例如,使用CRISPR和TALEN方法对T细胞进行基因组编辑,以及对T细胞不对称分裂进行详细分析,以便更好地理解和定义突变表位的质量,从而更好地产生即时免疫效应细胞和长期记忆T细胞。有关暴露于病原体和“环境因素”如何影响TCR谱系和最终疾病易感性的新的临床相关见解将有助于破译癌症患者针对突变表位的适应性细胞免疫反应中的分子“决策过程”,并提供必要的工具来加强治疗决策,为恶性肿瘤患者提供更有效、多层次和长期的细胞免疫反应。
— THE END —
▉ 往期文章目录
基础免疫学系列
肿瘤免疫学系列
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(下)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(上)
生信入门学习笔记系列
基础实验技术系列
Annexin V/PI染色检测细胞凋亡–OncoLab实验室
仪器操作系列
蔡司LSM800激光共聚焦显微镜操作视频–中西医结合基础研究中心
IN Cell Analyzer2200高内涵细胞成像分析系统操作教程–中西医结合基础研究中心
文献分享系列
年度巨献:神刊CA发布最新癌症数据:全球1000万人死于癌症,中国占比超3成
HLA–I分子加工和递呈抗原功能受损是免疫检查点抑制剂耐药的重要原因
作图投稿选刊系列
GraphPad+AI制作可发表级别的柱状图–OncoLab实验室
PubMed中如何按影响因子筛选检索结果并显示影响因子及分区?
如何使用EndNote软件插入参考文献(附6813种杂志参考文献格式文件)
中医中药系列

关注本号~

加入读者交流群~
本篇文章来源于微信公众号:OncoLab