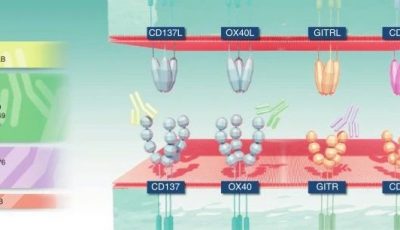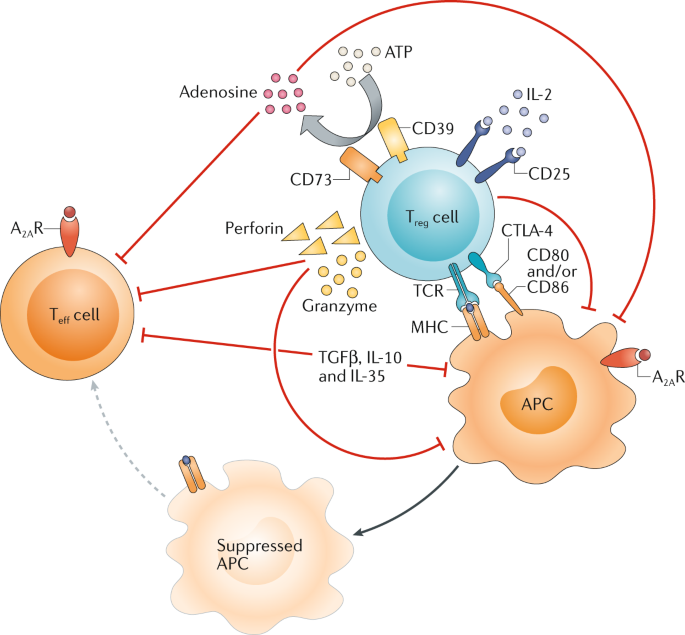
6.4 调节性T细胞与肿瘤的关系
Tregs在体内通过抑制自身反应性T细胞来动态调节免疫稳态。肿瘤组织来源于健康组织,因此抑制自身免疫的Treg可能会限制抗肿瘤免疫反应,因为它们的主要功能就是保护组织免受过度炎症造成的损害。小鼠实验结果显示出Tregs可显著抑制抗肿瘤免疫反应,在人类肿瘤中Tregs的存在也与不良预后相关。
6.4.1 调节性T细胞在抑制抗肿瘤免疫中的作用
Tregs在抑制抗肿瘤免疫中的作用已经在几种小鼠模型中得到证实。在小鼠和人类中,Foxp3基因的突变或消除会导致致命性的自身免疫反应,因此Foxp3缺失的小鼠种系不能用于抗肿瘤免疫的研究。虽然在靶向CD4、CD25的抗体、环磷酰胺等药物的作用下成年小鼠的Tregs数量会受到抑制或者所剩无几,但这些治疗也会影响激活的效应器T细胞,这与实验解释相矛盾。因此取而代之的是诱导性Treg靶向性的基因修饰,它已被用于瞬时耗尽成年小鼠的Tregs,以研究它们在抑制抗肿瘤免疫中的作用。有一种小鼠模型是在Foxp3位点(Foxp3DTR)的控制下插入人白喉毒素受体(DTR)。注射白喉毒素后,所有表达FOXP3的细胞都被耗尽,从而可以直接评估Tregs在抑制抗肿瘤免疫中的作用。
使用 Foxp3DTR 小鼠建造的各种有植入性肿瘤的小鼠模型体内 FOXP3+Tregs 均被耗尽。与没有耗尽Tregs的小鼠相比,Tregs耗尽后的小鼠的肿瘤生长被抑制,生存时间延长。这些机制研究表明,Tregs在抑制小鼠的抗肿瘤免疫中起着重要作用,Tregs的特异性耗竭能够抑制肿瘤的生长和延长小鼠的生存期。然而,Foxp3DTR小鼠注射白喉毒素后Tregs的耗竭并不是肿瘤微环境中Tregs所特有的,这些小鼠尽管有抗肿瘤免疫反应,但很快就会患上自身免疫性疾病。这再次强调了Tregs在维持外周耐受方面的重要性,并表明全身消耗Tregs可能不是癌症患者可行的治疗选择。
6.4.2 肿瘤中调节性T细胞的局部扩增
Tregs存在于许多健康组织中,随着肿瘤的生长,Tregs可能因抗原刺激增加和后续增殖而发生局部扩增(Fig 6.4a)。肿瘤组织中对MHC呈递的肽段具有特异性的Tregs会受到额外的抗原刺激,导致局部Tregs的扩增。同样支持这一推测的是,有研究发现,肿瘤内的Tregs与传统的CD4+T细胞有不同的T细胞受体谱,而且Tregs的T细胞受体很大程度上偏向于少数人群。此外,DC通常是肿瘤中增殖最多的免疫细胞类型。正常组织中存在的抗原特异性Tregs的扩增可能部分解释了肿瘤中Tregs的增加,并且这一机制可能与Tregs从外周向肿瘤的募集增强同时存在。
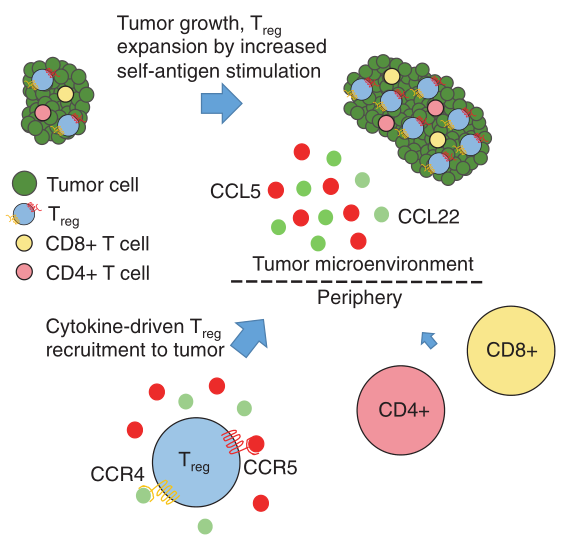
Fig 6.4 肿瘤微环境中Tregs的来源。随着肿瘤的生长,Tregs的自身抗原提呈增加,随后增殖,在肿瘤微环境中出现的频率也会增加。
6.4.3 调节性T细胞向肿瘤组织的转运
为了执行它们的功能,激活的Tregs需要被运输到组织内的炎症部位。白细胞的运输通常是通过趋化细胞因子来控制的,这些细胞因子被称为趋化因子。趋化因子与一组特定的细胞表面跨膜G蛋白偶联受体相互作用。例如,在淋巴结的正常生理条件下,趋化因子受体CCR7在Tregs上的表达使得它们重新聚集到T细胞区,在那里它们可以获得丰富的IL-2。Tregs在淋巴结内T细胞区的募集突出了趋化因子受体和配体能够将特定细胞靶向运输到特定位置的功能。同样,肿瘤或肿瘤微环境中的其他免疫细胞分泌的特定趋化因子也可以通过与Tregs上受体相互作用来主动招募Tregs。
在肿瘤中,特异性趋化因子/受体的相互作用依赖于肿瘤的组织来源和肿瘤微环境中产生的细胞因子环境。最常报道的Tregs被招募到肿瘤微环境的机制是通过趋化因子CCL22与Tregs上表达的CCR4的相互作用。这一途径是在乳腺癌中首次发现的,随后也相继发现了其在包括卵巢癌、结肠癌及头颈癌等多种肿瘤中均发挥重要作用。肿瘤细胞可以主动分泌趋化因子,肿瘤相关巨噬细胞(TAMs)则是趋化因子的另一个主要来源。肿瘤浸润的CD8+T细胞分泌CCL22也可以推动Treg向肿瘤募集。
正常炎症情况下,募集Tregs来限制免疫应答造成的组织损伤。这类似于肿瘤通过局部扩增或趋化因子介导Tregs募集到肿瘤中。这说明肿瘤可以利用正常的生物学过程来促进其在体内的生存。多种小鼠肿瘤模型的研究表明,Tregs在抑制抗肿瘤免疫中起着核心作用。
6.4.4 调节性T细胞与预后
许多研究评估了肿瘤微环境中Tregs的出现频率与临床结果之间的关系,包括头颈部、卵巢、乳腺、胰腺、胃、肺、肾以及肝癌和黑色素瘤。这些研究通常使用FOXP3作为Tregs标记物。有一些其他研究也通过观察CD8+T细胞与Tregs的比率来判断肿瘤内Tregs出现的频率。最近对15,500多个癌症病例中17种不同类型癌症的Meta分析发现,在所有癌症类型中,肿瘤中Tregs的频率越高,总体存活率越低(Fig 6.5)。其中许多研究使用组织学手段进行观察,观察时单独使用FOXP3染色或使用1-2个其他标记物来识别Tregs。
然而,Tregs及其与预后的关系偶尔会产生相互矛盾的结果,一些研究得出较高Tregs的频率与较差的临床结果相关,而另一些研究表明,较高的Tregs频率与较好的临床结果相关。在一些大肠癌、乳腺癌、卵巢癌和胃癌的研究中发现了这些相互矛盾的结果。
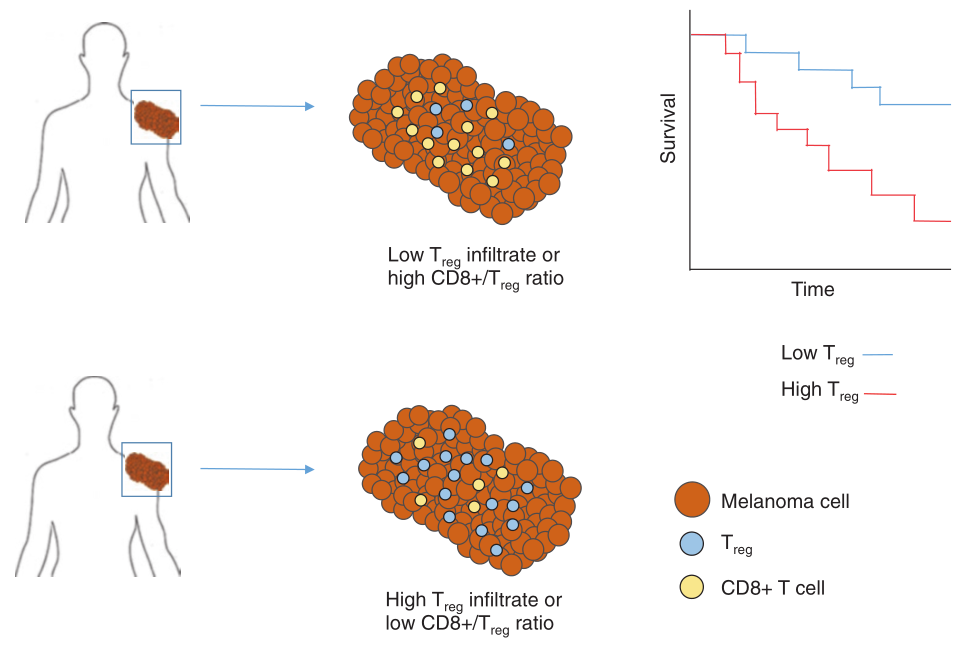
Fig 6.5 肿瘤中Tregs的出现频率越高,预后越差。
鉴于肿瘤中Tregs出现的频率和预后之间的关系尚不清楚,最近的工作试图进一步阐明FOXP3+Tregs在肿瘤中的作用。如上所述,FOXP3主要由Tregs表达,但在活化的T细胞中也有较低水平的瞬时表达。鉴于人类CD4+FOXP3+T细胞可以同时包含有Tregs和激活的效应性T细胞,依赖于FOXP3组织学分析而不使用其他标记的研究可能难以准确识别Tregs。错误地将效应性T细胞识别为Tregs可能是报道出现多种结论的原因。
最近一项评估CD4+FOXP3+Tregs在结直肠癌中的作用研究中试图评估FOXP3+Tregs与FOXP3+效应T细胞在控制结直肠癌预后中的作用。这些研究者发现有两种截然不同的结直肠癌免疫浸润:炎症性和抑制性。有趣的是,作者发现FOXP3表达的作用严重依赖于免疫浸润的类别。在抑瘤性肿瘤患者中,FOXP3+Tregs的频率较高,且FOXP3的高表达与较差的临床预后相关。在第二组炎症性肿瘤患者中,FOXP3+效应T细胞概率较高。在这一炎症性组中,FOXP3的高表达水平与较好的总体存活率相关。这项重要的研究强调,并不是所有表达FOXP3的人类CD4+T细胞都是Tregs,旨在评估Tregs在肿瘤中的作用的研究需要仔细地将FOXP3+细胞分类为Tregs和激活的效应T细胞。还需要对其他癌症类型进行更多的研究,以充分了解Tregs在人类癌症中的预后意义。
6.5 免疫疗法与调节性T细胞
6.5.1 改变调节与炎症之间的平衡
免疫疗法的一个特点是恢复对肿瘤的免疫反应。肿瘤微环境中衰竭的CD8+T细胞具有转录功能障碍的特征。表达抑制性受体的CD8+T细胞存在一系列功能障碍,其中PD-1的表达水平较高,同时伴有附加的抑制性受体的表达,如LAG-3、TIM-3和TIGIT,这些指标与功能障碍的严重程度相关。阻断抑制性受体可以部分或全部恢复先前衰竭的细胞的功能,或防止进一步衰竭。
然而,并不是所有的患者都对检查点抑制有反应。肿瘤内表达PD-L1的患者对PD-1/PD-L1阻断反应失败的一个可能解释是,他们的肿瘤可能富含Tregs。PD-L1+肿瘤中Tregs频率的增加可能会导致衰竭的细胞由于抑制性细胞因子的存在、缺乏共刺激或无法获得呈递的抗原而无法转化为效应细胞。此外,Tregs分泌IL-35可导致CD8+T细胞表达多种抑制性受体,甚至在PD-1/PD-L1阻断的情况下也可能使CD8+T细胞无反应。CD8+T细胞上多个抑制性受体的表达可能是患者免疫治疗后缺乏应答的重要原因,目前许多临床试验正在研究同时阻断多个抑制性受体。
6.5.2 针对调节性T细胞的治疗的潜在直接作用
部分患者在阻断CTLA-4或PD-1/PD-L1后抗肿瘤免疫功能增强。人们一直致力于了解表达CTLA-4和PD-1的效应CD8+T细胞的分子功能障碍,以及阻断这些抑制性受体提高效应细胞功能的途径。然而,CD8+效应T细胞并不是唯一表达这些抑制性受体的细胞。效应CD4+T细胞和Tregs都可以表达抑制性受体,阻断它们,特别是对Tregs的阻断,可能会影响它们的功能。
人们了解的免疫治疗机制是那些由效应性CD8+ T细胞控制的机制,但抑制受体对Tregs的潜在影响也是一个高度活跃的研究领域。PD-1可以在Tregs上表达,但PD-1信号在Tregs中的作用尚不清楚。CTLA-4在Tregs上也有表达,CTLA-4在抑制Tregs免疫应答中的作用已阐明。然而,阻断CTLA-4对Tregs和效应T细胞的相反的作用在抗肿瘤免疫中的作用目前仍是亟待阐明的较为有前景的研究领域。
CTLA-4 在 Tregs 中成组成性表达,是其关键的接触依赖性的免疫抑制机制之一。尽管人们已经认识到 CTLA-4+Tregs 在介导免疫抑制中的作用,但抗肿瘤免疫的增强很大程度上归因于CTLA-4对常规CD8+ T细胞的阻断作用。CTLA-4阻断的功效主要通过 CD8+T细胞实现,这与 CTLA-4 以细胞内信号转导方式限制 T 细胞活化的发现相一致。然而,抗 CTLA-4的给药也可能会耗尽或改变CD4+FOXP3+ CTLA-4+Tregs 的功能,从而增强抗肿瘤免疫。
CTLA-4阻断可以使Tregs减少,这可以通过一个小鼠模型来证明,实验采用CTLA-4阻断抗体的Fc受体(FcR)基因突变的小鼠模型,在该小鼠模型中,CTLA-4阻断抗体的FcR部分(介导抗体依赖的细胞毒性的部分抗体)发生了突变。在没有FcR结合的情况下,CTLA-4阻断对肿瘤生长的作用大部分丧失,说明抗体依赖的Tregs的细胞毒性消除可能有助于CTLA-4治疗的疗效。其次,研究表明,CTLA-4疗效取决于肿瘤微环境中Tregs的清除。这些研究表明,CTLA-4+Tregs的缺失可能在阻断CTLA-4后的反应中起作用,但也可能是阻断Tregs的配体影响其功能。例如,Tregs上的CTLA-4与DC 上的CD80/CD86相互作用,导致吲哚胺2,3-双加氧酶(IDO)的表达。表达IDO的DC可以有效地抑制T细胞的激活。然而,如果CTLA-4被阻断或CTLA-4+Tregs被耗尽,这可能会阻止DC上IDO的上调,从而导致抗肿瘤免疫增强。总之,CTLA-4及PD-1/PD-L1阻断与增强抗肿瘤免疫的关系及作用机制是目前的重点研究领域。充分评估检查点抑制对Treg出现频率和功能的影响很重要。
6.6 关于调节性T细胞在免疫肿瘤学中的重要性的展望
Tregs是一种重要的CD4+T细胞亚群,可控制外周免疫耐受和免疫稳态。然而,Tregs也可以限制抗肿瘤免疫,就像在各种各样的小鼠癌症模型中所证明的那样。越来越多的人支持Tregs在各种人类癌症中限制抗肿瘤免疫的重要性。因此,Tregs在癌症中的有效治疗靶点可能仅限于在肿瘤内Tregs选择性或优先利用,而不会引发有害的自身免疫或炎症反应的一些靶点。虽然最近已经描述了选择性调节肿瘤内Tregs的新潜在治疗靶点,但进一步以Tregs为重点的研究显然是有必要的。Tregs是否限制了检查点阻断(即PD-1/PD-L1或CTLA-4阻断)的效果是另一个尚未解决的重要问题。Tregs在正常生理和癌症免疫学中发挥的核心作用表明,未来的免疫疗法必须仔细考虑它们对肿瘤和外周Treg功能的不同影响。
— THE END —
▉ 往期文章目录
基础免疫学系列
肿瘤免疫学系列
肿瘤免疫学-第6章:调节性T细胞的作用、作用机制以及对癌症的影响(上)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(下)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(上)
文献分享系列
年度巨献:神刊CA发布最新癌症数据:全球1000万人死于癌症,中国占比超3成
HLA-I分子加工和递呈抗原功能受损是免疫检查点抑制剂耐药的重要原因
生信入门学习笔记系列
基础实验技术系列
Annexin V/PI染色检测细胞凋亡-OncoLab实验室
仪器操作系列
蔡司LSM800激光共聚焦显微镜操作视频-中西医结合基础研究中心
IN Cell Analyzer2200高内涵细胞成像分析系统操作教程-中西医结合基础研究中心
作图投稿选刊系列
GraphPad+AI制作可发表级别的柱状图-OncoLab实验室
PubMed中如何按影响因子筛选检索结果并显示影响因子及分区?
如何使用EndNote软件插入参考文献(附6813种杂志参考文献格式文件)
中医中药系列

关注本号~

加入读者交流群~

本篇文章来源于微信公众号:OncoLab