1.免疫检查点阻断响应和抵抗的基因组特征
Valsamo K. Anagnostou – 约翰霍普金斯大学,巴尔的摩,马里兰州
Valsamo Anagnostou聚焦于影响免疫治疗反应的肿瘤固有特征,指出多项研究显示,高肿瘤突变负荷与免疫检查点阻断的反应相关,这在微卫星不稳定性背景下得到证实。然而,在将突变负荷作为ICB反应生物标志物时,多种技术和生物学因素(肿瘤样本纯度,检测方法的统一,其他影响因素)带来了挑战。然而,整合外显子和转录组分析可以更好地预测对ICB的反应。
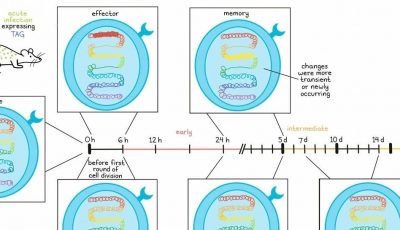
例如,多组学分析表明,某些特定的基因组特征与泛癌症反应相关,而有些则是癌症类型和谱系特异性的。在化学免疫治疗下消退的肿瘤具有更高程度的染色体不平衡,这表明染色体缺失可以消除单倍体区域中的突变,因此,这些突变持续存在并与ICB反应相关。Valsamo及其同事因此假设,存在一些突变亚群(“持久突变”),它们在生物学上是不同的,不太可能通过染色体缺失而被删除(这对细胞来说是致命的事件),从而导致持续的肿瘤免疫控制。这些持久突变可以是单倍体区域中的单拷贝突变或多拷贝突变,不同于容易丢失的二倍体区域中的单拷贝突变。
在肺癌的例子中,基线肿瘤中存在的一组候选突变相关新抗原在ICB耐药肿瘤中被消除,并可能推动耐药性的出现。新抗原的丢失要么是通过免疫消除含有新抗原的细胞,要么是通过导致新抗原丢失和耐药克隆扩增的遗传事件。事实上,在肺癌示例中,几种具有免疫原性的新抗原突变通过遗传事件被消除,与这些遗传事件导致肿瘤抵抗是一致的。通过量化持久性肿瘤突变负荷(pTMB;单拷贝或多拷贝持久突变),发现持久突变的比例以及多拷贝与单拷贝突变的相对贡献取决于癌症谱系,并且与总体肿瘤突变负荷明显不同。
事实上,许多肿瘤类型根据计算总体TMB或pTMB的不同而改变分类(低vs高突变负荷)。肿瘤非整倍性和持久突变在肿瘤类型之间表现出一系列关系,而驱动基因中的持久突变很少,除了tp53。与总突变负荷、容易丢失的突变负荷或肿瘤非整倍性相比,持久突变负荷更能区分应答患者。持久突变在肿瘤进化过程中持续存在,具有较高pTMB的肿瘤更容易发炎,与细胞毒活性和免疫治疗反应相关。
总之,Anagnostou指出,理解肿瘤免疫反应的基因组调控是关键,并可以为患者筛选策略提供指导。TMB并不能完全捕捉肿瘤的外来性,持久突变代表了整体TMB中不可编辑的一组,不会被染色体缺失或治疗选择压力消除。因此,持久突变可能导致更持久的新抗原驱动的免疫应答,从而在免疫治疗中获得长期临床效益。
2.MEDI1191 联合德瓦鲁单抗(D)肿瘤内用药(IT):晚期实体瘤首次人体试验更新
Eduardo Castañón – Clínica Universidad de Navarra, Pamplona, Spain
一种名为MEDI1191的编码IL-12的mRNA脂质颗粒制剂,可通过肿瘤内(i.t.)注射促进局部IL-12产生,并增强小鼠模型中的先天和适应性CD8+ T细胞依赖的抗肿瘤免疫。Eduardo Castañón展示了一个首次人体试验的1期临床试验结果,该试验研究了肿瘤内MEDI1191和静脉(i.v.)抗PD-1(德瓦鲁单抗)在治疗过多次的晚期实体瘤患者中的联合应用。
共有61名患者参加了试验。在剂量递增部分1A,皮肤或皮下病变患者在第1天和第22天接受MEDI1191治疗,然后每4周接受一次德瓦鲁单抗治疗。在1B部分(皮肤或皮下病变患者)和1D部分(深部病变患者,所有情况下均有肝转移),患者在第1天、第29天和第57天同时接受MEDI1191和杜瓦鲁胺治疗,然后每4周接受杜瓦鲁胺治疗,每8周接受MEDI1191治疗。
治疗持续最多两年,或直至疾病进展或不可忍受的毒性。未观察到剂量限制性毒性或最大耐受剂量。最常见的不良事件是疲劳和发热,最常见的3级不良事件是贫血。在注射和未注射的局部或远端病变中观察到抗肿瘤活性,证实了放射状效应。在未注射的靶病变处进行了反应评估。总体反应率为8%,其中5例证实为部分缓解(PR),包括3例先前接受过抗PD-(L)1和/或抗CTLA-4治疗的患者。25%的患者疾病稳定(SD),其中2例未证实PR。反应持续最长可达22个月,中位反应持续时间尚未达到。
在不同剂量队列中,血清IL-12在注射后24小时达到峰值,IFNγ、CXCL9、CXCL10和CXCL11水平在MEDI1191或MEDI1191加德瓦鲁单抗的第一剂和第二剂治疗后的24小时也有所上升。然而,这些细胞因子或趋化因子的增加与MEDI1191的剂量无关。配对活检显示,大约40-50%的患者肿瘤PD-L1表达增强,肿瘤浸润CD8+和CD3+Ki67+细胞增加。PR/SD患者与进展病患者相比,在抗肿瘤关键基因特征的表达上有更大的增加趋势。
3.在PD-1耐药肿瘤中激动剂对联合免疫治疗的作用
Elizabeth M. Jaffee – 约翰霍普金斯大学,马里兰州巴尔的摩市
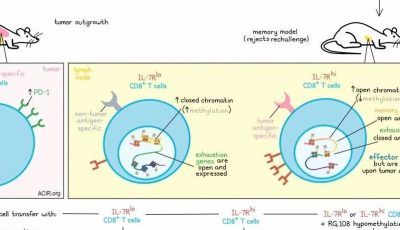
免疫疗法在某些癌症治疗中取得了重大突破,但大多数癌症仍然存在抵抗性,即使有T细胞浸润也是如此。在研究这类肿瘤中T细胞反应的质量时,伊丽莎白·贾菲及其同事发现这些T细胞并非有效的效应器,他们假设诱导更高质量的效应T细胞反应可能增强抗肿瘤免疫力。
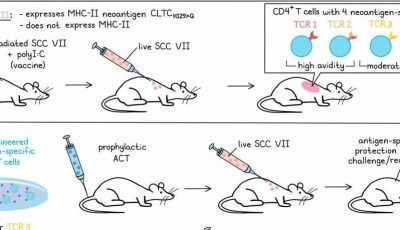
在研究TCR亲和力作为T细胞质量的潜在特征时,贾菲发现在非耐受小鼠模型中,低亲和力TCR的T细胞反应可以通过疫苗加强,而高亲和力T细胞反应可以自行清除肿瘤。在耐受小鼠中,即使接种疫苗,低亲和力TCR也不足以发挥作用,只有高亲和力TCR加疫苗才能诱导T细胞定位和肿瘤清除。然而,通过将OX40或4-1BB激动剂添加到低亲和力TCR的T细胞和疫苗中,可以诱导IFNγ的产生和肿瘤的清除。
更近期,贾菲和其他人评估了新辅助/辅助临床试验的患者样本。在第一组治疗中,治疗只包括疫苗,该疫苗诱导了淋巴结聚集物的浸润,显示出T细胞激活和单核细胞PD-L1上调的迹象。患者的无病生存期和总生存期显著改善,这可能与间皮素特异性CD8+ T细胞的扩增和T细胞亲和力的增加有关。
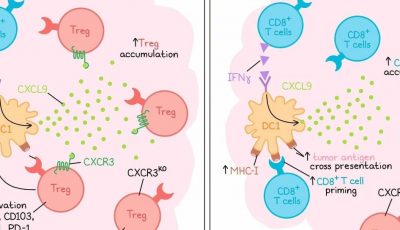
深入研究发现,肿瘤中CD4+和CD8+T细胞都增加了,但没有激活。基于这些结果,研究人员在第二组中加入了抗PD-1。在这种情况下,淋巴聚集物,可能是三级淋巴结构,正在积极形成并活化T细胞和B细胞。还发现Th17 T细胞(可能源于Tregs的重新编程)离开这些聚集物并与肿瘤细胞共定位。在长期生存的患者中,Th1:Th2比例增加,肿瘤中耗竭的CD4+和CD8+ T细胞减少。添加抗PD-1增加了抗原呈递单核细胞并减少了抑制性单核细胞,这提示巨噬细胞的重新编程。还注意到抗PD-1增加了Tregs,当与肿瘤细胞共定位时,这些细胞与预后较差有关。
在两组治疗中,治疗前的中性粒细胞(表达IL-8R)与预后较差有关。在治疗后的样本中,中性粒细胞水平较高与CD4+和CD8+ T细胞耗竭和病人生存期较短有关。在两组患者中,表达CD137的CD8+ T细胞亚群的增加与颗粒酶B表达和更长的生存期相关。为了增强这个亚群,研究者测试了将激动剂抗CD137添加到疫苗和抗PD-1中。在胰腺癌小鼠模型中,这种三联疗法是唯一减轻病情负担的治疗方法。
在患者中,三联疗法是本研究中第一个诱导病理反应的治疗方法,其中10名患者中有3名达到近完全缓解。中位无病生存期尚未达到,许多患者已经两年了。从每个治疗组的患者免疫应答中观察,每组中的总CD8+ T细胞数量逐渐上升。另一方面,Tregs在第二组中增加,但在第三组中随着激动剂抗CD137的添加而减少。克隆扩张随着每个治疗组的增加而增加,在第三组中观察到大量的高度扩张克隆。第二组中,转运、耗竭和细胞骨架重塑标志物的表达增加,第三组中细胞骨架重塑和趋化因子/转运进一步富集,这表明浸润T细胞的运动性增加。

加入读者交流群~
(添加请备注单位姓名)

关注本号~
本篇文章来源于微信公众号:OncoLab