31.3 当前的和新出现的治疗反应、耐药性和毒性预测因素
31.3.3 基于血液的治疗反应预测因子
循环无细胞DNA,特别是循环肿瘤DNA(ctDNA),作为一种非侵入性生物标记物,已引起广泛关注,其通过定量分析来自肿瘤细胞的独特突变DNA,可用于监测治疗反应。在黑色素瘤和结直肠癌治疗中,ctDNA已被证实能够反映传统方法(如放射学评估)测量的疾病负担变化,并可能更早地识别疾病状态的改变,无论是治疗响应还是疾病进展。然而,是否可以将这种早期检测用作临床决策的触发因素以改善长期治疗结果,目前还不清楚。此外,尽管初步证据表明治疗早期的ctDNA动态变化与最终治疗结果存在相关性,但将ctDNA作为免疫治疗预测标记物的潜在临床用途尚需进一步研究确认。
随着对癌症治疗监测手段的不断探索,将来可能研究使用个性化的、序列独立的肿瘤标记物,如异常甲基化的ctDNA,作为一种非侵入性监测方法。考虑到表观遗传变化在调控免疫检查点阻断反应中的潜在作用,评估具有已知影响免疫治疗结果的分子靶标的甲基化特异性ctDNA的可能性,将是一个非常有意义的研究方向。至于其他可能预测检查点阻断反应的血清学标记物,除了乳酸脱氢酶(LDH)外,目前尚未确定有明显临床实用价值的独立标志物,而LDH本身更多地被认为是预后指标。
就像基于肿瘤活检的分析一样,循环免疫标记物在免疫检查点阻断治疗前后的变化也被研究以预测治疗效果。在几项回顾性研究中,治疗前的中性粒细胞/淋巴细胞比率(NLR)已被证实是预测ipilimumab治疗效果的独立因素,较低的NLR与预后无病生存期(PFS)和总生存期(OS)的改善相关。然而,这一指标在需要类固醇治疗的患者中应用受限,而且目前还没有达成一致的最佳NLR界值以将患者分层为预后“好”或“差”。
在一小部分患者中,血液外周CD4+ T细胞上PD-1的表达与非小细胞肺癌(NSCLC)的不良预后相关,并且与对抗PD-L1治疗的反应呈负相关。相反地,治疗过程中循环调节性T细胞(Treg)数量的增加与对PD-1抑制剂治疗的无反应相关。此外,CXCL11的基线水平较高和可溶性MHC-I类相关链A(SMICA)水平较低可能预示着接受抗CTLA-4治疗的患者存活率较低。
在治疗开始的早期,外周血中表达诱导性T细胞共刺激分子(ICOS)的CD4+ T细胞的频率增加,这被证明是预测CTLA-4治疗效果的可靠生物标志物,特别是在治疗的前一两剂后。此外,治疗早期绝对淋巴细胞计数和嗜酸性粒细胞计数的增加也可能预示着使用ipilimumab治疗的患者总体生存率的改善。
31.3.4 治疗反应的无创性预测指标
目前,研究人员正在开发新的成像技术,旨在帮助预测免疫治疗的反应。然而,到目前为止,在常规临床实践中,非侵入性成像主要用于在治疗前后的分期和跟踪评估。尽管基于影像的疾病负担评估在治疗开始前具有预后和潜在预测价值,但依据实体瘤疗效评价标准(RECIST)的放射学评估在接受免疫治疗的患者中可能会有误导,尤其是因为这类治疗的独特作用机制和反应动力学导致的,只有少部分(3%-15%)患者会出现这种情况。
免疫治疗可能引起的假性进展现象,即相关的肿瘤炎症可能暂时导致肿瘤体积增加,甚至在之前未被检测到的微小转移部位出现新的病变。这一现象可能掩盖了一旦抗肿瘤免疫反应得到激活并最终引发病变缩小或消失的潜在趋势。为了准确解释这些“非典型”反应模式,提出了一套新的基于成像的评估标准,称为“免疫相关反应标准”(irRC),这一标准同样适用于评估其他基于常见肿瘤炎症作用机制的免疫治疗。这些新标准有望提供更准确的治疗效果评估,从而优化临床决策和治疗策略。
引入以免疫相关反应标准(irRC)为基础的新评估标准表明,传统的放射学评估在检查点阻断治疗的癌症监测中存在局限性,且其作为反应预测因子的能力有限。然而,值得注意的是,非典型放射学反应模式并不常见。在常规的临床实践中,放射学反应通常在免疫检查点阻断治疗开始后10至12周才能明确观察到,且任何早期观察到的反应都需要至少4周后通过重复扫描来确认其可靠性。实际上,有报道指出治疗后6至9个月才出现的严重延迟反应案例。
PD-1/PD-L轴,包括程序性细胞死亡蛋白1(PD-1)及其配体(PD-L1和PD-L2),是维持外周耐受的关键生理机制之一。这一轴是控制细胞毒性T细胞反应的重要调节因子,与许多其他的抑制性受体路径不同,其功能在几乎所有类型的炎症条件下都被广泛描述。PD-1主要在活化的T细胞和B细胞上表达,其表达是由T细胞受体(TCR)依赖的激活诱导的,表达水平和持续时间则取决于刺激的性质和持续性。PD-L1和PD-L2通常由某些巨噬细胞亚群表达,但在多种炎症条件下,也可由多种炎症细胞因子在多种造血及非造血细胞中诱导表达。PD-1/PD-L1轴在抑制T细胞的关键功能中起作用,这包括限制细胞因子的产生、抑制细胞的增殖及细胞毒性颗粒的形成。
然而,正在开发新的基于成像的指标,这些指标可能在治疗前或治疗初期就能提供诊断和治疗的重要见解,潜在地促进对那些可能无法从当前治疗方案中获益的患者进行快速的管理调整。例如,在一组接受ipilimumab和抗血管生成药物贝伐单抗治疗的患者中,利用Choi标准的放射学评估包括了肿瘤密度特征;遗憾的是,治疗过程中肿瘤密度的变化并未能有效预测治疗反应。而在按Keynote-001方案接受pembrolizumab单抗治疗的患者中,发现肿瘤的大小和密度,或者结合使用的综合指标(如Choi或修正的Choi标准)与总生存率有关。
值得注意的是,这种密度特征评估介绍了一种比RECIST或irRC更为复杂的反应模式分析方法,为未来在免疫检查点阻断治疗背景下,利用放射学/结构特征作为潜在的预后或预测因子的研究开辟了新途径。这些新发展有望为临床决策提供更精确的支持,特别是在评估免疫治疗的效果时。
31.3.5 肠道微生物组作为一种预测性生物标志物
癌症免疫治疗的一个新兴领域是研究微生物群系及其对免疫检查点阻断反应的影响,其中肠道微生物群的作用尤为关键。在一项开创性的研究中,通过动物模型和对接受CTLA-4抑制剂治疗的患者进行的粪便微生物移植实验,发现了三个关键观察结果:首先,患者对治疗的反应显著与肠道中某些特定的拟杆菌物种的丰富度相关;其次,接受CTLA-4抑制剂治疗后患者的肠道微生物组成发生了变化;第三,CTLA-4抑制剂的疗效依赖于微生物特异性T细胞反应的存在。
在另一项研究中,发现肠道中双歧杆菌的丰富度与小鼠更强烈的自发抗肿瘤反应相关,其特定的微生物“补充剂”不仅单独发挥作用,还可与PD-L1检查点阻断疗法协同增效。同样,接受PD-1抑制剂治疗的患者在肠道微生物组成和多样性方面表现出显著差异,这在治疗效果好与差的患者中尤为明显。
尽管肠道微生物组与环境、饮食、宿主免疫以及抗肿瘤免疫之间的交互作用已被广泛认识,但这些相互作用如何精确调节免疫检查点抑制剂的反应机制仍待进一步明确。这一领域的深入研究可能揭示新的治疗目标,为癌症免疫治疗提供更加个性化和有效的策略。
31.3.6 毒性的预测因子
基于免疫检查点阻断治疗的肿瘤特异性不完全,非靶向免疫刺激导致的免疫相关毒性(免疫相关不良事件,irAEs)是常见的。有时,irAEs的出现被认为可能预示着抗肿瘤免疫刺激的活性;然而,在使用CTLA-4和PD-1治疗的情况下,关于irAEs的发生与抗肿瘤临床益处之间的关联,不同肿瘤类型的报告常常显示出矛盾。
鉴于许多irAEs的潜在严重性,识别可靠的毒性预测标记与预测治疗反应同样重要。然而,目前尚未确定任何有效的预测标记。从机制上看,人们认为存在的自身反应性T细胞克隆可能因免疫检查点阻断而被重新激活,导致自身免疫毒性。这些克隆在治疗前可能只有低频率的存在,而且当前缺乏仅凭序列信息就可靠预测特定T细胞受体抗原靶标的技术,这使得对自身反应性T细胞群体的预测鉴定实际上无法实现。此外,目前尚不清楚为何一些预先存在但受到抑制的克隆会被重新激活,而其他克隆则不会。
在针对CTLA-4抑制剂治疗的患者进行的全血基因表达谱研究中,虽然在治疗中的样本中识别了潜在的胃肠道毒性预测信号,但未能确定独立的预测基因。这些研究结果提醒我们,在开发新的免疫治疗策略时,需要进一步探索和理解免疫相关毒性的生物学基础,以改善患者管理和治疗结果。
31.4 系统免疫和抗肿瘤免疫的静态与动态评价
传统的癌症治疗反应生物标记物分析方法主要依赖于治疗前从组织或血液样本中获取的静态时间点数据。然而,这种方法存在局限性,尤其是当样本被长期存档时,可能由于基因组特征和免疫分析的演变,使得生物标记物的准确性受到影响。这与样本的空间异质性和采样误差结合,可能解释了像PD-L1这样的预处理生物标志物仅具有适中的预测价值。此外,由于抗肿瘤免疫反应具有动态特性,仅靠对预处理样本的静态评估无法全面把握。
随着越来越多的研究聚焦于免疫检查点阻断反应的预测生物标记物,越来越明显的是,分析早期治疗样本中的适应性免疫特征(或从治疗前到治疗中的变化)在预测能力方面可能远胜于静态分析,这反映了肿瘤微环境的动态变化(Fig.31.3)。最近的研究进一步验证了这一点,其中一项研究表明,通过免疫组化和基因表达分析早期治疗样本得到的生物反应标记物远比仅分析预处理样本的标记物更为强大。在对基于组织和基于血液的分析的其他几项研究中也观察到了类似的动态发现。
综上所述,这些研究表明,在免疫监测中应采用新的范式,即常规评估早期治疗反应,以帮助指导治疗策略——至少在确定更有效的预处理生物标记物之前应如此(Fig.31.3)。重要的是,这样的分析应该被纳入现代临床试验的设计中——最终甚至可能成为标准的护理治疗流程的一部分(Fig.31.4)。
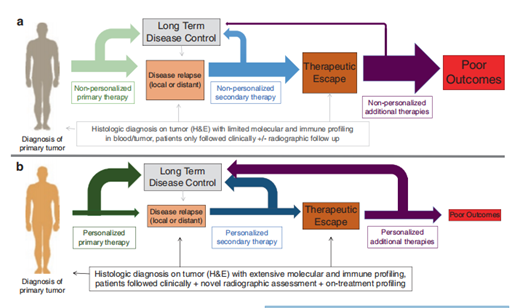
Fig 31.3 (A)动态和静态标记对免疫检查点抑制剂阻断的重要性。在传统的癌症治疗中,一旦诊断出原发肿瘤,通常会通过有限的分子分析和肿瘤组织以及可能的血液中的免疫图谱进行肿瘤评估。治疗通常是基于经验的非个性化方案,患者接受临床跟踪和可能的放射学随访。在这种情况下,相当大比例的患者会经历疾病复发,并接受非个性化的二次治疗——通常在最少或没有生物标志物评估的情况下进行。同样,反应的患者很少,大多数患者最终经历了治疗逃逸,总体结果较差。(B) 在癌症治疗的创新方法中,通过在治疗前进行广泛的分子和免疫图谱分析,来扩展原发肿瘤的组织学诊断。选择个性化的初级治疗方案是基于这些详细的见解,从而使更高比例的患者实现长期疾病控制。只有少部分患者发生疾病复发,此时,个性化的二次治疗方法被用来结合复发肿瘤的分子和免疫图谱以及肿瘤和血液的治疗响应图谱。较少的患者经历疾病逃逸,当这种情况确实发生时,基于更精细化的治疗策略,对个性化方法的响应更高。通过这种方法,治疗效果不佳的患者非常少见。
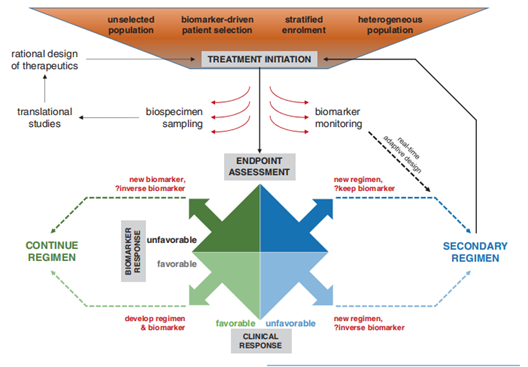
Fig 31.4 将生物标记物纳入肿瘤免疫学临床试验的设计,可以显著提高临床试验的效率和效果。现有的生物标记物能够用于指导患者选择和/或登记参加临床试验,其中已验证的生物标记物提供预测性信息以指导治疗方案的选择。此外,预后和预测性标记物可用于对参试者的入选进行分层,优化治疗转换和临床结果。为保持治疗的”未知性”并寻找与肿瘤组织学类型无关的反应生物标记物,需要招募多样化的人群进行试验。在临床试验中,对接受治疗的患者在治疗前和治疗期间进行生物样本采集,尤其强调纵向采样,以便收集关于治疗过程中动态变化的重要信息,包括抗药性的发展。采用适应性设计结合”即时”生物标记物监测,可以促进对那些似乎不太可能有反应的患者进行早期、基于生物标记物的治疗调整。达到相关的临床终点后,可能会进行临床和生物标记物结果的关联分析,从而作出接受或拒绝特定生物标记物、治疗方案或两者的关键决策。在出现不一致的情况时,生物标记物可以预测治疗失败,并可能随后被确认为用于反向治疗分配的生物标记物。对于未能从初始治疗获益的患者,根据生物标志物信息,可以特别或适应性地选择二次或后续的治疗方案,以期提高治疗的个体化和成功率。这种方法不仅增强了临床试验的策略性,还可能提高患者的生存质量和总体生存率。
31.5 将预测因素纳入临床试验和护理治疗标准
持续优化免疫检查点阻断策略的成功将依赖于最大化疗效和最小化免疫相关毒性,这两者都需密切关注生物标记物的发现。当前,由于缺乏可靠的预测无应答指标,现实世界中的临床实践还无法像临床试验那样精准地定位“强应答者”。因此,需要大量努力通过正在进行的临床试验来扩展免疫治疗的适用范围,而不仅仅是集中于已知可能获益较大的患者群体。
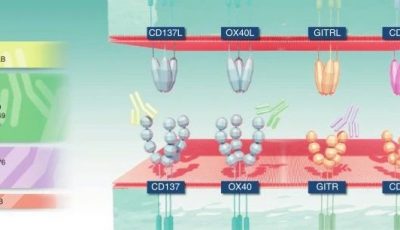
目前,许多新的检查点抑制分子正处于临床前和临床开发阶段,这包括针对抑制性检查点如LAG3、TIM3和TIGIT的分子,以及针对激活性(共刺激)检查点如OX40、4-1BB和GITR的分子。为了增加未来免疫治疗方案的复杂性,正在研究许多组合策略,这些策略不仅包括多种免疫治疗的结合,还包括检查点与分子靶向治疗的跨模式组合。
将生物标记物的发现纳入这些临床试验方案时,需要考虑几个关键因素:(1)所获得的生物标记物应能反映受治疗影响的生物隔室;(2)考虑药物的药代动力学和药效学特性,合理安排重复样本采集的时间和频率,并确保这些制剂能有效渗透到各个不同的组织隔室;(3)收集生物标记物的可行性与患者的接受程度;以及(4)将生物标记物的结果整合到治疗方案的设计与调整中的可能性(Fig.31.4)。这种综合方法将推动更为精确和个性化的治疗策略,从而提高治疗效果并降低不良反应。
目前,由生物标记物驱动的临床试验设计正在逐渐被应用,例如TITAN-RCC肾癌试验(NCT02917772),这些试验将动态临床结果纳入后续治疗变更的决策中,并进行必要的组织和血液评估,以确定在每个治疗决策点的反应相关性。此外,例如BIONIKK肾细胞癌研究(NCT02960906),探索基于分子肿瘤信号预测免疫或靶向治疗反应的可能性,并据此进行初始治疗分配。FRATION-肺部试验(NCT02750514)在分配患者到初始治疗组时,考虑了先前的治疗历史和肿瘤的PD-L1表达,并采用适应性试验设计,使得非小细胞肺癌患者在病情进展时能转移到新的联合治疗组。
两项临床试验(NCT02834013,NCT02923934)特别关注通过对一系列罕见癌症患者的治疗和研究,确定对ipilimumab和nivolumab联合治疗反应的生物标记物,这在独立队列中是难以实现的。
新佐剂设置非常适合开展探索性生物标记物研究,越来越多地被用于免疫检查点阻断。此类试验正在积极招募多种癌症类型的患者,如黑色素瘤(NCT02519322,NCT02736123,NCT02977052)、结直肠癌(NCT03026140)、胶质母细胞瘤(NCT02550249)、肾细胞癌(NCT02446860)和非小细胞肺癌(NCT02818920),以满足临床需求和并行生物标记物的发现。
尽管最终目标是识别可以通过非侵入性手段获取的强大的、预处理预测生物标记物,但由于免疫检查点阻断的独特作用机制,目前生物标记物的发现通常需要侵袭性生物样本与非侵入性采样进行比较。因此,成功识别预测因素将取决于提高参与临床试验的患者对活检程序的接受度,这可能会因地区的临床实践和文化习俗而有所不同。
31.6 总结和结论
我们已经进入了肿瘤免疫治疗的时代,这种治疗基于对抗肿瘤和全身免疫反应的深入了解,以及肿瘤的基因组和表观遗传学变化、肿瘤微环境的作用,还有宿主外部环境的影响。这些知识不仅为免疫检查点阻断反应的特征提供了科学基础,也为当前和新出现的预测指标建立了框架。然而,免疫治疗的复杂性在于尚未确定完美的预处理活检中的预测生物标记物。
随着研究的深入,越来越明显我们需要一种综合的方法和精确的预测模型来指导治疗。这包括测量肿瘤和血液样本在治疗过程中的纵向适应性反应。这些概念不仅应在临床试验中得到广泛接受,也应在标准护理的治疗设置中得到充分考虑。通过这种方法,我们可以在免疫检查点阻断治疗的背景下实现最优的治疗和监测策略,从而为患者提供最佳的治疗效果。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 温鑫
图文排版 | 郭子 杜轻松
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab