33.1 简介
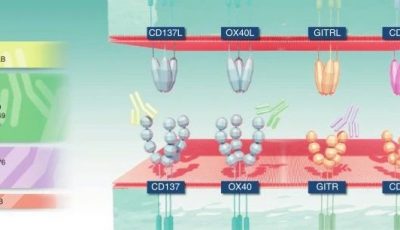
免疫检查点抑制剂是一类免疫调节药物,它们通过单克隆抗体阻断肿瘤细胞用来逃避免疫系统监视的通路。这类药物主要作用于T细胞表面的某些关键受体,包括细胞毒性T淋巴细胞相关蛋白4(CTLA-4)和程序性死亡蛋白1(PD-1)及其配体PD-L1。首个获批用于癌症治疗的免疫检查点抑制剂是抗CTLA-4的伊匹单抗(ipilimumab),其在III期临床试验中相比标准化疗显著延长了患者的总生存期(OS),目前已作为转移性黑色素瘤患者的一线治疗药物。然而,另一种抗CTLA-4抗体tremelimumab在治疗转移性黑色素瘤时,并未显示出超过标准化疗的生存优势,但其在其他肿瘤类型的联合治疗方案中正处于研究阶段。
第二类抑制剂针对PD-1及其配体PD-L1,已开发出多种抗体用于治疗晚期黑色素瘤以及包括非小细胞肺癌(NSCLC)、肾癌、膀胱癌、头颈癌和霍奇金淋巴瘤等多种肿瘤。在这方面,纳武利尤单抗(nivolumab)和帕博利珠单抗(pembrolizumab)为目前最先进的临床开发药物,已获批用于多种适应症。
在抗PD-L1药物方面,atezolizumab已被FDA批准用于治疗转移性NSCLC和晚期尿路上皮癌,avelumab用于治疗转移性默克尔细胞癌,而durvalumab则正在审批过程中,用于晚期或转移性尿路上皮癌的治疗。
使用这些免疫调节药物可能导致一系列免疫相关不良事件(irAEs),这些事件源于免疫系统的过度激活,从而减弱了免疫反应的抑制(Fig 33.1)。这些不良反应包括一些主要的疾病如胃肠道、内分泌和肝脏毒性反应,及其他较少见的炎症事件。所有这些不良反应具有不同的发病时间,需通过仔细监测、随访和管理来处理。
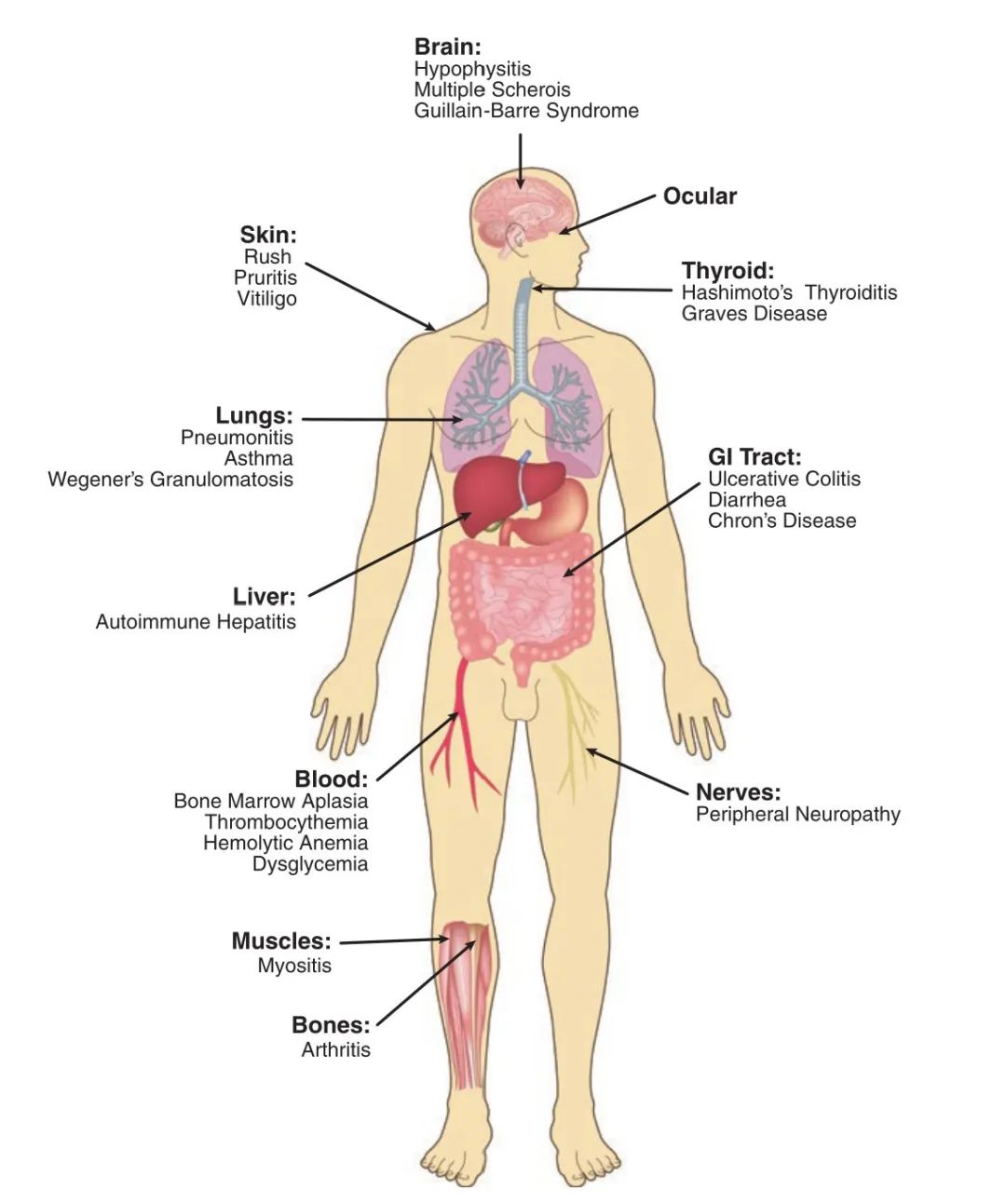
Fig 33.1 受免疫相关不良事件影响的机体组织
如果及时采取适当的干预措施,这些不良事件通常是可逆的;但如未能及早发现和处理,可能会严重威胁生命。针对ipilimumab相关的irAEs,管理指南已根据临床研究中获得的经验制定,并得到FDA的批准。
33.2 免疫相关不良事件发生率
在接受伊匹单抗(ipilimumab)治疗的患者中,最常见的不良事件包括腹泻、结肠炎、疲劳、瘙痒、皮疹和内分泌异常。对于使用PD-1抑制剂的患者,常见的不良事件则包括疲劳、皮疹、腹泻、瘙痒、关节痛和便秘。在单药治疗中,任何级别的免疫相关不良事件(irAEs)的发生率为15%至90%,而那些严重到需要免疫抑制治疗或停止免疫疗法的不良事件,其发生率估计在0.5%到13%之间。
当伊匹单抗与PD-1抑制剂联合使用时,约54%的患者出现了3至4级的药物相关不良事件,其中最常见的是结肠炎(17%)、腹泻(11%)和谷丙转氨酶水平升高(11%)。治疗irAEs所需的免疫抑制药物,特别是用于处理皮肤不良反应的外用药物,在联合使用伊匹单抗时的使用率(89%)较单独使用时(59%)有所增加。
随着伊匹单抗剂量从3 mg/kg增加到10 mg/kg,与严重不良事件的风险也从7%增加到25%,主要是由于腹泻发作次数的增加。相比之下,尼伏单抗(nivolumab)的剂量从0.3 mg/kg增加到10 mg/kg时,并未观察到类似的模式。派姆单抗(pembrolizumab)的严重不良反应发生率在使用2 mg/kg时为20%,在使用10 mg/kg时为25%,未随剂量增加而显著增加。因此,伊匹单抗的毒性似乎与剂量相关,而PD-1/PD-L1抑制剂的毒性并不明显随剂量增加。
33.3 免疫相关不良事件发生时间
伊匹单抗治疗引发的免疫相关不良事件(irAEs)的起始时间和结局因所涉及的器官而异。虽然这些不良事件大部分在治疗的前三个月内出现,但也有报告显示,即便在治疗结束几个月后,仍可出现一些特定的不良反应。这些反应通常是暂时性的,例如皮肤症状通常在首次使用伊匹单抗后的2至3周内首先出现。
免疫介导的结肠炎和肝炎的发病时间也有所不同,结肠炎一般在接受第二剂后约5至10周出现,而肝炎则在第三剂后的12至16周出现。内分泌功能障碍则可能从第四剂后的第九周开始显现,并且可能需要较长时间才能缓解,有时甚至可能是永久性的,如大多数脑垂体炎症状一样。免疫介导的肺炎和肾炎则更晚出现,分别在治疗开始后的8至14周和14至42周被观察到。这些信息强调了在使用伊匹单抗时对患者进行仔细监测和及时管理的重要性。
33.4 一般考虑
FDA已批准了针对伊匹单抗相关免疫相关不良事件(irAEs)的管理指南,这些指南是风险评估和缓解策略的重要组成部分。与伊匹单抗相比,抗PD-1抗体,特别是尼伏单抗(nivolumab)和帕博利珠单抗(pembrolizumab),通常具有更好的耐受性。然而,这些药物引发的不良事件也需要类似的管理方法。
管理指南为不同器官或系统的不良反应提供了特定的处理方法。通常,涉及的措施包括停止免疫治疗并开始使用类固醇进行免疫抑制,其剂量和治疗时长根据不良事件的严重程度和类型而定。
对于1级不良事件,建议仅进行对症治疗。2级不良事件需要暂停免疫治疗,并且如果症状持续,则应在出现症状后一周内开始口服类固醇治疗(例如,强的松0.5-1 mg/kg/天或等效剂量)。只有在不良事件减轻至1级或完全消失后,才可考虑恢复免疫治疗。对于3至4级的不良事件,应立即给予高剂量的糖皮质激素(例如,强的松1-2 mg/kg/天),并在症状减轻至1级以下时逐渐减少剂量。对于这些高级别不良事件,应永久停止免疫检查点抑制剂治疗。
在对大剂量皮质类固醇治疗无反应的严重毒性病例中,应考虑使用英夫利昔单抗(infliximab,5 mg/kg),一种针对肿瘤坏死因子α(TNF-α)的嵌合单克隆抗体。此药物的使用背景包括其在治疗自身免疫性疾病如克罗恩病和溃疡性结肠炎中的应用。组织学研究显示,伊匹单抗引起的免疫相关结肠炎中的结肠黏膜浸润了淋巴细胞和中性粒细胞,这与特发性溃疡性结肠炎类似。早期使用这些药物可以迅速缓解不良事件,减少长期依赖皮质类固醇的需要。
使用皮质类固醇治疗免疫相关不良事件(irAEs)似乎不会影响免疫检查点抑制剂的治疗效果。根据纪念斯隆凯特琳癌症中心2011年4月至2013年7月期间对298名接受伊匹单抗(3 mg/kg)治疗的患者的数据,103名患者(占35%)需要使用皮质类固醇处理irAEs,其中29名(占10%)对类固醇治疗未迅速反应,需要使用抗TNF治疗。这些免疫抑制治疗并未影响患者的总生存期(OS)或治疗失败时间。
关于免疫抑制剂是否会影响PD-1抑制剂的治疗效果的数据相对较少,但现有数据显示,使用免疫抑制治疗处理irAEs并未显著降低PD-1抑制剂的疗效。
免疫相关不良事件与免疫检查点抑制剂疗效之间的关系仍有争议。早期伊匹单抗的临床试验数据显示,出现irAEs的患者往往临床获益更大。一项对三项II期研究的汇总分析显示,未出现irAEs或irAEs较轻的患者的疾病控制率(DCR)为20%-24%,而irAEs至少为2级的患者DCR为34%-43%。这两组患者的平均生存时间(OS)分别为8.2个月和14.8个月。此外,两项针对高危黑色素瘤患者使用伊匹单抗的辅助治疗试验发现,无复发生存率与irAEs之间存在显著的相关性。相比之下,一项针对135名接受PD-1抑制剂治疗的非黑色素瘤患者的回顾性研究发现,客观缓解率(ORR)或OS与irAEs的发生率或类固醇的使用之间无显著相关性。
英夫利昔单抗的作用机制主要是阻断肿瘤坏死因子(TNF)向炎症部位招募中性粒细胞的能力,这一机制不太可能影响免疫检查点抑制剂的抗肿瘤活性。
33.5 器官特异性免疫相关不良事件
33.5.1 皮肤毒性
皮肤表现,包括皮疹、瘙痒和粘膜炎,是与免疫检查点抑制剂相关的最常见免疫相关不良事件(irAEs)。使用抗CTLA-4抗体的患者中约有47%-68%出现不同程度的皮肤毒性,而使用抗PD-1或抗PD-L1抗体的患者则约有30%-40%。
这些皮疹通常表现为网状或斑疹状,伴有轻度红斑,尤其常见于躯干和四肢,并可能伴有瘙痒感(Fig 33.2)。大多数免疫相关的皮疹可以通过使用基于皮质类固醇的外用药膏进行治疗。持续的瘙痒则可能需要口服抗组胺药物。
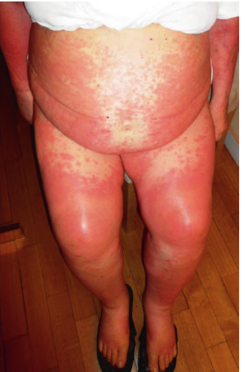
Fig 33.2 伊匹单抗治疗患者的皮肤皮疹
对于更严重的2级皮疹,尤其是已经存在的情况下,可能需要口服类固醇治疗。而对于3级至4级的严重皮肤反应,需暂停相关的免疫治疗,并开始静脉注射糖皮质激素。建议在这些情况下咨询皮肤科医生,并在可能的情况下进行皮肤活检以进一步诊断。
史蒂文斯-约翰逊综合征(Stevens-Johnson Syndrome)是一种较为罕见但潜在致命的疾病(Fig 33.3)。对于这种情况,建议立即采用静脉注射糖皮质激素治疗。如果症状没有改善,应考虑联合使用免疫抑制剂和皮质类固醇。
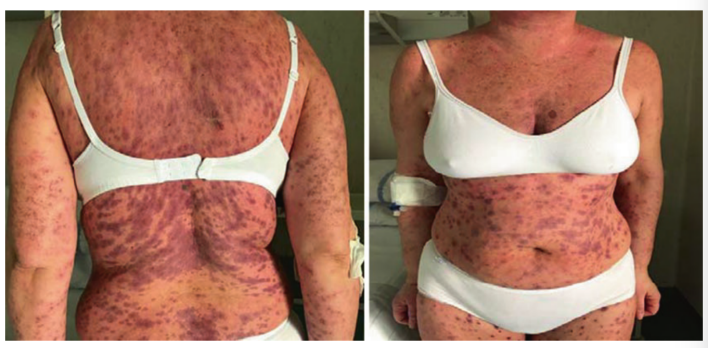
Fig 33.3 Stevens-Johnson综合征
白癜风是另一种常见病症,通常在接受免疫检查点抑制剂治疗后出现。其特征是真皮深层血管周围淋巴细胞的浸润,靠近黑素细胞,被认为是对治疗的免疫反应的一个标志。与使用伊匹单抗相比,使用抗PD-1抗体的患者更容易出现口腔粘膜炎,通常需要使用局部皮质类固醇和利多卡因进行治疗,并在排除了念珠菌感染后进行(Fig 33.4)。
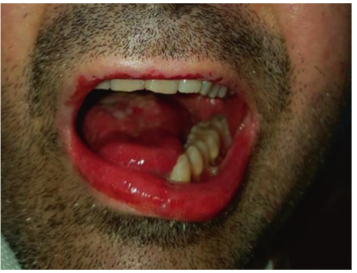
Fig 33.4 抗PD-1治疗引起的黏膜炎
33.5.2 胃肠道毒性
腹泻是接受免疫治疗的患者中常见的一种副作用,且需及时诊断和治疗以防止发展成严重不良事件。通常,腹泻会在治疗开始后6周内出现,使用抗CTLA-4抗体(如伊匹单抗)的患者中腹泻的发生率更高,与抗PD-1/PD-L1抗体相比尤为明显。据报道,接受伊匹单抗治疗的黑色素瘤患者中,大约30%会出现腹泻,其中3-4级的严重腹泻比例不足10%。在一项针对伊匹单抗的II期研究中,10 mg/kg剂量组的严重腹泻发生率高于3 mg/kg组(10%对比1%)。在III期研究中,同样的趋势也被观察到,其中10 mg/kg组的胃肠道毒性高于3 mg/kg组,前者有79%的患者报告腹泻,而后者为64%,且10 mg/kg组的3-4级腹泻发生率是3 mg/kg组的近两倍(34%对比18%)。
相比之下,在使用抗PD-1药物的患者中,仅有1-2%的患者出现3-4级腹泻。胃肠道毒性是联合使用尼伏单抗和伊匹单抗的主要不良事件,发生率约为40%,其中约9%的患者出现严重腹泻和结肠炎。
有时肠炎甚至在没有腹泻的情况下也可能引起小肠梗阻。活检表现为水肿的粘膜伴有大量中性粒细胞和/或淋巴细胞的浸润。目前尚无有效的预防措施来阻止腹泻或结肠炎的发展。使用布地奈德等药物治疗肠炎已进行评估,但未显示显著效果。
在处理腹泻时,确保适当的水分补充至关重要,并需排查其他可能导致腹泻的原因,如艰难梭菌感染。对于1级腹泻,通常使用洛哌丁胺进行对症治疗已足够。对于2级腹泻,应暂停免疫治疗并使用口服皮质类固醇(如强的松0.5-1 mg/kg/天或等效剂量)。若病情缓解,可以恢复治疗;若在3-5天内未缓解,应按照3-4级事件处理,包括使用高剂量静脉注射皮质类固醇(如甲基强的松龙1-2 mg/kg/天)和预防性抗生素治疗。如果对高剂量皮质类固醇治疗无反应,则建议使用英夫利昔单抗5 mg/kg,并在2周后视情况可能重复使用。因高肠穿孔风险,患者应接受临床监测。抗CTLA-4和/或抗PD-1治疗应永久停用。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 罗荷
图文排版 | 应正 赵栩
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab