38.1 引言
利用免疫系统来消灭恶性细胞一直是血液学家和肿瘤学家的长期追求。异体造血干细胞移植(HSCT)为这一梦想奠定了基础,这是首次在临床上成功验证免疫治疗在癌症中的潜力,尤其是在移植物对抗白血病的效果得到明确证明之后。尽管同种异体造血干细胞移植已成为常规治疗手段,但其主要局限性仍包括短期和长期的毒性、副作用,以及适合这种疗法的血液恶性肿瘤种类有限。此外,获取干细胞供体也存在一定困难。
经过数十年的深入研究,科学家们开发并验证了多种新的策略,以扩展免疫治疗的应用范围。靶向恶性细胞表面抗原是其中的关键一步,抗CD20单克隆抗体利妥昔单抗就是这一策略的典型代表。近年来,针对新受体的单克隆抗体、新一代将细胞毒性T细胞导向肿瘤细胞的双特异性抗体(BsAbs),以及基因修饰的T细胞和免疫检查点抑制剂(ICB)的发展,在多项临床试验中展现出了极大的潜力,有望成为癌症治疗的新前沿。这些新疗法能够突破“癌症免疫设定点”的屏障,克服癌症诱导的免疫逃逸机制。
在本章中,我们将回顾近期关于免疫肿瘤学在血液学领域应用的临床试验成果,期望这些研究能够激发该领域的进一步探索,从而显著改善癌症患者的预后。
38.2 直接靶向细胞表面抗原
体液免疫在血液系统恶性肿瘤中的抗肿瘤潜力早已被识别,并推动了针对恶性细胞表面分子发展的单克隆抗体技术。单克隆抗体的作用机制包括直接诱导细胞死亡、通过Fc受体介导的抗体依赖性细胞介导的细胞毒性(ADCC)/吞噬(ADCP)以及补体依赖性细胞毒性。通过将抗体与细胞毒素结合或促使细胞内化后的细胞毒性来增强杀伤效果,也是常见策略之一。
利妥昔单抗(rituximab)是首个成功开发并应用于临床的抗CD20单克隆抗体,在血液学领域取得了重大突破。然而,在接下来的十多年里,大多数靶向其他细胞抗原的单克隆抗体并未能展示出足够的疗效和安全性。随着对免疫编辑和单克隆抗体工程技术的深入理解,近年来这种情况开始好转,一些新的单克隆抗体在临床试验中展现出了令人瞩目的活性(Fig 38.1)。
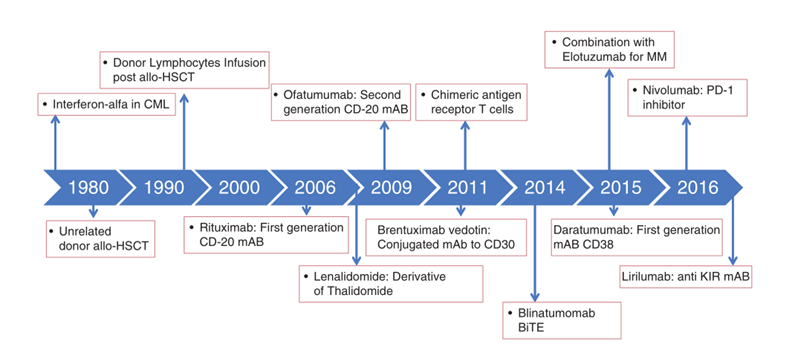
Fig 38.1血液系统恶性肿瘤免疫肿瘤药物发现与开发的关键时间点
38.2.1 CD20的成功故事
通过人源化小鼠抗体成功克服了异种免疫原性这一障碍,最终促成了利妥昔单抗的开发。这是首个针对CD20的单克隆抗体,在复发性CD20阳性弥漫性大B细胞淋巴瘤患者中显示出了前所未有的临床活性。在2002年发表的具有里程碑意义的随机临床试验中,法国GELA小组证明,在标准的CHOP方案中加入利妥昔单抗,能够显著提高弥漫性大B细胞淋巴瘤老年患者的缓解率,并将无事件生存期(EFS)和总体生存期(OS)延长至10年(分别为44%和28%)。自此关键试验以来,利妥昔单抗已被证明对几乎所有类型的CD20阳性B细胞恶性肿瘤有效,现已成为惰性和侵袭性非霍奇金淋巴瘤(NHL)以及慢性淋巴细胞白血病(CLL)的标准治疗手段。
近年来,两项大型随机临床试验进一步证实了利妥昔单抗在治疗伯基特淋巴瘤和成人B细胞型急性淋巴细胞白血病(ALL)中的优势。第二代针对CD20的单克隆抗体obinutuzumab(GA101)是一种通过糖基工程改造的II型人源化单抗,设计时考虑了其对免疫细胞上的FcγRIII受体具有更高的亲和力,在体外实验中表现出可能优于利妥昔单抗的效果。与利妥昔单抗相比,obinutuzumab表现出更直接的细胞死亡诱导作用和增强的ADCC/ADCP活性,但其补体依赖性细胞毒性(CDC)较低。此外,obinutuzumab与单个CD20四聚体结合,内化程度低于利妥昔单抗,这可能进一步增强了ADCC/ADCP效应。在一项大型随机试验中,obinutuzumab与氯苯达莫司汀联合使用相比于与利妥昔单抗的组合,在反应率和完全缓解率方面表现出优势,随后被批准用于治疗老年或不适合进行其他治疗的CLL患者。然而,值得注意的是,obinutuzumab联合氯苯达莫司汀的治疗方案毒性更大。
在CLL的治疗中,obinutuzumab正在与新型药物如Bcl-2拮抗剂Venetoclax和BTK抑制剂Ibrutinib联合使用,初步结果显示出很有希望的前景,表明在不久的将来,obinutuzumab可能会在CLL治疗中广泛应用。
此外,在GADOLIN III期临床试验中,obinutuzumab联合苯达莫司汀治疗复发性滤泡性淋巴瘤患者,相比苯达莫司汀单药治疗,显著延长了无进展生存期(PFS)。同样,在GALLIUM研究中,基于obinutuzumab的诱导和维持治疗显著延长了先前未经治疗的滤泡性淋巴瘤患者的PFS。然而,这些在滤泡性淋巴瘤和CLL中观察到的成功,未必能在更具侵袭性的淋巴瘤中得到重复。事实上,在GOYA研究中,这项大型随机III期试验比较了利妥昔单抗或obinutuzumab联合CHOP治疗的效果,涉及1418例未经治疗的弥漫性大B细胞淋巴瘤患者,结果未能达到其主要终点(研究者评估的PFS)。
38.2.2 靶向CD20以外的分子
38.2.2.1 阿仑单抗
阿仑单抗是一种针对CD52的单克隆抗体,CD52是一种表达在B细胞、T细胞和单核细胞表面的抗原。最初,阿仑单抗被批准用于治疗对氟达拉滨耐药的慢性淋巴细胞白血病(CLL)和具有del17p突变的CLL。虽然阿仑单抗对三分之一的氟达拉滨耐药患者有效,但其广泛的免疫抑制作用与严重甚至致命的机会性感染密切相关。
在CLL和其他淋巴瘤亚型的治疗中,阿仑单抗与化疗联合使用的大多数临床试验结果未能显示出相较于标准治疗的明显优势。此外,由于感染相关的高死亡率,一些研究甚至不得不中途停止。
同样地,由于其可能增加危及生命的感染并发症和较高的疾病复发率,阿仑单抗在非清髓性同种异体造血干细胞移植的预处理方案中使用也受到限制。2012年,阿仑单抗用于血液恶性肿瘤的商业化被中断,原因是制造商计划将其重新命名并用于多发性硬化症的治疗。不过,在一些国家,通过特定分发程序,仍然可以获得阿仑单抗用于CLL的治疗。
38.2.2.2 吉妥珠单抗
吉妥珠单抗是一种针对CD33表面抗原的单克隆抗体,耦联了强效抗肿瘤药物卡利凯霉素(calicheamicin),这是一种蒽环类抗生素。在急性髓性白血病(AML)中,CD33是一个特别有吸引力的靶点,因为它在大多数AML细胞中均有表达。吉妥珠单抗在治疗复发性AML的老年患者中显示出令人鼓舞的II期临床数据后获得FDA批准。然而,由于在一项大型随机试验中的负面结果(见Rowe和Lowenberg的最新综述),吉妥珠单抗的使用引发了广泛争议,最终被撤回。
尽管如此,来自四项随机试验的汇总数据重新激发了对在新诊断AML中使用吉妥珠单抗的兴趣,特别是在细胞遗传学表现更有利的患者中。此外,吉妥珠单抗在新诊断和复发的急性早幼粒细胞白血病(APL)患者中表现出特别高的活性,这些患者通常表达高水平的CD33b。鉴于过去三十年中缺乏新的AML有效药物,吉妥珠单抗的临床应用可能应根据这些新的研究结果重新评估。
38.2.3 新的研究热点
38.2.3.1 本妥昔单抗
本妥昔单抗是一种抗体药物偶联物(ADC),由靶向CD30的单克隆抗体与微管破坏剂MMAE通过可被蛋白酶切割的连接物耦联而成。CD30是肿瘤坏死因子(TNF)受体超家族的一个成员,主要在B细胞和T细胞活化后表达。CD30的表达已在多种血液系统恶性肿瘤和实体肿瘤中被报道。在血液学中,表达CD30的主要恶性肿瘤包括经典霍奇金淋巴瘤(cHL)、间变性大细胞淋巴瘤(ALCL)、原发性纵隔B细胞淋巴瘤、T细胞淋巴瘤以及EBV诱导的移植后淋巴细胞增生性疾病。
本妥昔单抗(BV)在复发/难治性CD30阳性淋巴瘤中表现出显著的临床活性,已被批准作为该病症及ALCL的单药治疗。在霍奇金淋巴瘤的单药治疗中,BV的总缓解率(ORR)为75%,其中近一半自体干细胞移植后复发的患者获得了持久缓解。一项评估BV作为一线单药治疗的II期临床试验针对不适合常规化疗的老年患者,显示出总缓解率达92%,其中完全缓解率为73%。
在多项I期和II期临床试验中,BV联合化疗和放疗表现出良好的耐受性和可行性。然而需要注意的是,BV不应与含有博莱霉素的方案联合使用,因为这会显著增加肺部并发症的风险。在一项II期试点研究中,BV与a型VD联合使用用于早期高危霍奇金淋巴瘤患者,结果显示,在经过2个和4个周期的治疗后,分别有90%(26/29)和93%(27/29)的患者PET扫描结果为阴性。目前,一项大型III期试验正在评估BV + AVD方案与ABVD方案在晚期经典霍奇金淋巴瘤(NCT01712490)中的疗效。
AETHERA研究探索了BV在复发性霍奇金淋巴瘤患者自体干细胞移植后作为巩固治疗的潜力。研究结果显示,BV组患者的中位无进展生存期(PFS)为42.9个月,而安慰剂组仅为24.1个月,支持了BV在移植后环境中的有效性。最新的数据进一步证实了BV在AETHERA研究中的优越性。一些研究还表明,BV可以在自体或同种异体干细胞移植后复发的患者中有效控制疾病。总体而言,BV在霍奇金淋巴瘤中展现出非常有前景的治疗效果。多个正在进行的III期随机试验可能会将BV纳入经典霍奇金淋巴瘤的标准治疗方案,这些试验正在评估BV与化疗联合用于未经治疗或复发的霍奇金淋巴瘤患者。
在小规模试验或病例报告中,BV也被用于治疗其他CD30阳性的淋巴细胞恶性肿瘤;然而,与经典霍奇金淋巴瘤相比,这些数据的稳定性较差。在58例复发或难治性系统性间变性大细胞淋巴瘤患者中,BV的总缓解率为85%,中位缓解持续时间为12.6个月。目前,I/II期研究正在招募患者,以评估BV联合化疗治疗CD30阳性原发性纵隔B细胞淋巴瘤(PMBCL)、弥漫性大B细胞淋巴瘤(DLBCL)和灰色地带淋巴瘤(NCT01994850)的效果。特别是在T细胞淋巴瘤中,进一步的研究至关重要,因为T细胞淋巴瘤通常对标准化疗耐药,迫切需要新的治疗方法来改善其预后。
38.2.3.2 达雷木单抗
达雷木单抗是一种靶向CD38的IgG1单克隆抗体。CD38是一种跨膜糖蛋白,由多种细胞类型表达,包括T细胞、B细胞、单核细胞、NK细胞和NK/T细胞。在多发性骨髓瘤(MM)细胞中,CD38的广泛表达使其成为一个重要的治疗靶点。最近的研究表明,达雷木单抗的生物学效应不仅限于传统治疗性单克隆抗体的功能,还可能涉及免疫调节。达雷木单抗可以减少调节性免疫细胞的数量,例如髓源性抑制细胞(MDSC)、调节性B细胞和新发现的CD38高表达的调节性T细胞亚群,这一作用允许CD4+辅助性T细胞和CD8+细胞毒性T细胞的扩增,并增加IFN-γ的产生。
在两项针对重度预处理的复发/难治性多发性骨髓瘤患者的临床研究中,达雷木单抗作为单药显示出显著的疗效,诱导了高比例的缓解,包括严格的完全缓解和延长的临床缓解。这些结果使其获得批准用于治疗已接受至少三种治疗方案(包括蛋白酶体抑制剂和IMID或两者)的多发性骨髓瘤患者。
早期发表的CASTOR和POLLUX试验数据分别评估了达雷木单抗与硼替佐米和地塞米松或来那度胺和地塞米松联合使用在既往治疗过的多发性骨髓瘤患者中的疗效。尽管这些研究的随访时间相对较短(分别为7.5个月和13.5个月),但在缓解率和无进展生存期(PFS)方面均显示出显著改善。在CASTOR试验中,达雷木单抗组的12个月PFS为60.7%,而对照组为26.9%;在POLLUX试验中,达雷木单抗组的PFS为83.2%,对照组为60.1%。
达雷木单抗的应用迅速扩展至一线治疗,并正在与其他抗骨髓瘤药物联合进行评估。在符合自体干细胞移植(HSCT)条件的多发性骨髓瘤患者中,IFM的CASSIOPEA III期大型随机试验正在比较标准治疗方案VTD(硼替佐米、沙利度胺和地塞米松)与达雷木单抗+VTD的疗效(NCT02252172)。在老年患者中,VMP(硼替佐米、美法兰和泼尼松)也在与达雷木单抗+VMP进行比较(NCT02195479)。如果这些研究结果能够证实其在多发性骨髓瘤中的疗效,达雷木单抗可能会成为“骨髓瘤中的利妥昔单抗”。
除了多发性骨髓瘤外,达雷木单抗在其他表达CD38的血液系统恶性肿瘤中的应用也值得探索。临床前数据支持评估达雷木单抗在高危慢性淋巴细胞白血病(CLL)中的作用,因其中的恶性B细胞群体通常高表达CD38。最近,达雷木单抗在难治性CD38+ NK/T细胞淋巴瘤中也取得了成功。
38.2.3.3 艾洛珠单抗
艾洛珠单抗是一种靶向CS1/SLAMF7受体的单克隆抗体。SLAMF7在正常和恶性浆细胞中高度表达,但在除NK细胞外的其他细胞类型中表达较少。艾洛珠单抗的作用机制与其他单克隆抗体(如达雷木单抗)有所不同。
艾洛珠单抗通过首先与NK细胞表面的SLAMF7受体结合,激活这些NK细胞。被激活的NK细胞能够识别并通过其CD16受体与艾洛珠单抗的Fc区结合。这种结合使得NK细胞能够锁定并杀死那些被艾洛珠单抗标记的恶性浆细胞,从而实现对肿瘤细胞的定向杀伤。
艾洛珠单抗作为单药在治疗复发/难治性多发性骨髓瘤(MM)时效果有限。然而,在I期试验中,艾洛珠单抗与其他抗骨髓瘤药物联合使用时显示出显著活性。在一项随机开放标签的II期研究中,艾洛珠单抗与硼替佐米联合治疗略微提高了150例先前治疗过的MM患者的无进展生存期(PFS)。1年的PFS率为39%,而对照组为33%;在最新的分析中,2年的PFS率为18%,而对照组为11%。
在一项大型随机多中心III期ELOQUENT-2试验中,研究比较了来那度胺和地塞米松联合或不联合艾洛珠单抗在治疗646例复发/难治性MM患者中的疗效和安全性。试验结果显示,艾洛珠单抗联合治疗组的总体缓解率(ORR)为79%,对照组为66%;中位PFS分别为19.4个月和14.9个月。这些结果促使艾洛珠单抗在2015年获得FDA的批准。
总的来说,艾洛珠单抗联合来那度胺在MM治疗中展现出一定的临床活性,尽管其疗效似乎不如达雷木单抗那样显著。进一步的研究仍然需要来明确艾洛珠单抗在MM治疗中的确切地位,特别是确定其最佳的联合治疗方案。
38.2.3.4 双特异性T细胞接合体
前面的章节中提到,单克隆抗体提供了一种比标准化疗更具选择性、且毒性更小的治疗方法。然而,单克隆抗体的一个主要缺点是,它们无法有效地将细胞毒性T淋巴细胞(CTL)招募到肿瘤区域,也无法将非炎症性肿瘤微环境转变为炎症性环境。
研究表明,肿瘤浸润的T细胞数量与不同癌症的临床结果直接相关。自利妥昔单抗开发以来,科学家们花费了十多年的时间,试图找到能够在肿瘤微环境中直接增加和激活特异性CTL的方法。这种研究的范式转变,成功催生了两种不同的临床策略:
1. 免疫检查点抑制剂(ICBs):通过抑制T细胞表面抑制性受体和配体的相互作用,如PD-1和CTLA-4,ICBs能够释放T细胞介导的免疫反应,使其在启动期和效应期更加活跃。
2. 嵌合抗原受体T细胞(CAR-T细胞):通过转导自体T细胞,使其表达特异性抗原结合域和细胞内信号受体,从而绕过T细胞耗竭,重新引导CTL特异性识别并杀伤癌细胞。
然而,由于在良好生产规范(GMP)设施中为每位患者制造个性化CAR-T细胞的成本、复杂性和时间延迟,科学家们探索了另一种重定向T细胞的策略,即双特异性抗体(BsAb)的发展。这种策略被认为是最重要的创新之一。
双特异性抗体(BsAb)又称双靶向抗体,具有同时结合两个不同目标的能力,使T细胞与癌细胞接触。这种技术能够让患者体内的CTL直接与癌细胞接触,并促使肿瘤的持续溶解。继急性淋巴细胞白血病(ALL)治疗中的成功之后,BsAb成为发展最快的抗癌疗法之一,目前已有50多种BsAb进入临床开发阶段。
例如,Blinatumomab是一种双特异性T细胞接合体(BiTe),由两个单链可变片段(scFv)组成,通过一个灵活的短连接体连接(Fig 38.2)。N端的scFv识别肿瘤相关抗原(TAA),C端的scFv则结合T细胞表面的CD3ε。两个臂之间的连接体赋予了Blinatumomab高度的灵活性,这种结构无需依赖T细胞受体(TCR)的特异性和肽抗原的呈递。
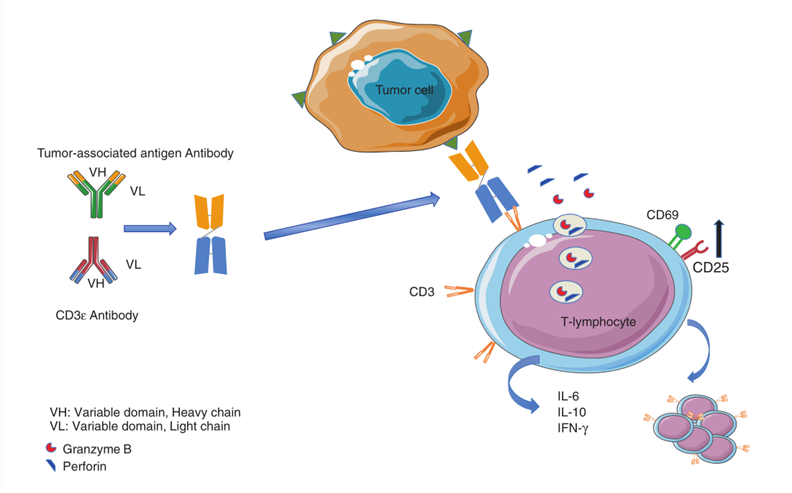
Fig 38.2 展示了Blinatumomab的结构和作用机制
因此,Blinatumomab可以绕过CTL上的MHC I-TCR轴,使多克隆T细胞能够被招募到肿瘤微环境中,从而克服肿瘤细胞上常见的MHC分子下调问题。体外实验表明,类似Blinatumomab(CD3/CD19)的BsAb可以触发效应T细胞与白血病细胞之间的免疫突触形成。这些突触允许T细胞释放穿孔素和颗粒酶(成孔蛋白),进一步引发细胞核的凝集和膜的起泡。此外,免疫突触还会导致免疫激活受体如CD25和CD69的上调,并促进促炎细胞因子如IL-2、IFN-γ和IL-6的产生。值得注意的是,在使用Blinatumomab后,CD4+和CD8+ T细胞的增殖和激活都不需要额外的IL-2补充。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 罗荷
图文排版 | 郭子 应正
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab