20.5 一线治疗
随着单一免疫检查点抑制剂在先前治疗过的患者中安全性和疗效的确立,一些患者实现了前所未有的长期生存,下一步就是评估该策略在一线治疗中的应用。
CHECKMate-012是一项I期多队列研究,评估了在晚期NSCLC患者中单独使用纳武单抗或与伊匹单抗(ipilimumab)、铂类化疗、厄洛替尼(erlotinib)或贝伐单抗(bevacizumab)的联合使用之间的效果差异。在纳武单抗的单一治疗组中,52例患者中有12例观察到明显的反应,整体反应率为23% (ORR, The Overall Response Rate),另外14例患者达到病情稳定(SD),确认疾病控制率(DCR)为50%。中位PFS(无进展生存期)为3.6个月,OS(总生存期)为19.4个月。
虽然PD-L1<1%的患者的疗效低于PD-L1阳性的患者(14% : 50%),但其1年的OS(79% : 83%)没有显著差异。
在联合免疫检查点治疗的研究中,78例化疗初治的NSCLC患者被随机分为三个治疗组,分别为纳武单抗3 mg/kg每2周一次组、伊匹单抗1 mg/kg每6周一次组和伊匹单抗1 mg/kg每12周一次组。两个药物的耐受性良好。每12周一次的伊匹单抗组与每6周一次的伊匹单抗组相比,ORR(47% : 38%)和中位PFS(8.1个月 : 3.9个月)数值较高。
但在对黑色素瘤和小细胞肺癌的研究中,我们观察到暴露于伊匹单抗的次数越多,联合疗法的疗效越高,因此选择每6周一次的伊匹单抗方案更适用于治疗NSCLC疾病。
两个队列的汇总结果显示,在13例PD-L1≥50%的患者中,有12例确认应答,1例未确认应答。
在CHECKMate-012报告的第三个队列中,56名未经治疗的NSCLC患者先接受了纳武单抗10 mg/kg联合铂类化疗的双联治疗(每3周进行一次,为期4个周期)然后再维持纳武单抗的单一治疗,直到肿瘤进展或产生不可接受的毒性。其他的组化疗方案为吉西他滨(gemcitabine)联合顺铂治疗鳞癌,培美曲塞(pemetrexed)联合顺铂治疗非鳞癌,卡铂联合紫杉醇(paclitaxel)治疗任何组织学类型的癌症。另一队列为纳武单抗5 mg/kg联合卡铂和紫杉醇。
任何等级的TAE(treatment- related adverse events, 治疗相关副作用)患者有35例(95%),有25例(45%)出现3或4级毒性。有4名患者(7%)出现3或4级肺炎。确认的ORR、中位PFS、中位OS、1年生存率和2年生存率分别为33%-47%、4.8-7.1个月、11.6-未达到、50%-87%和25%-62%。
对于接受纳武单抗5 mg/kg联合卡铂和紫杉醇治疗的14名患者来说,治疗效果显著提升,确认的ORR为43%,估计有效应答时间为19.6个月,中位OS未达到,1年OS为86%,2年OS为62%。
在随机开放标签的2期Keynote-021临床试验中,123名化疗初治的NSCLC患者被随机分成卡铂联合培美曲塞,再联合或不联合派姆单抗(Pembrolizumab)两组。
服用派姆单抗的患者出现3级或更高程度的不良反应(40% : 26%)。
实验结果显示,三药联合治疗组的ORR显著增加(55%:29%,P=0.001)。尽管使用派姆单抗组的中位PFS较高(13.0个月:8.9个月),但两组的OS(总生存期)没有差异,中位数未达到,估计6个月OS超过90%。
Keynote-024是一项开放标签的随机3期试验,在以前未经治疗且肿瘤细胞中PD-L1表达≥50%的NSCLC患者中,比较了每3周200 mg的派姆单抗治疗与铂类化疗的结果(Fig. 20.2)。有EGFR突变或ALK易位的患者被排除在研究之外。
化疗方案分别为顺铂联合培美曲塞、卡铂联合培美曲塞、顺铂联合吉西他滨、卡铂联合吉西他滨、卡铂联合紫杉醇。在筛选出的1934例患者中,对1653例患者进行了PD-L1评估,其中500例(30.2%)患者的PD-L1表达比例≥50%。
第一个观察终点为PFS(无进展生存期),我们在符合条件的305名患者中随机选择154人接受派姆单抗治疗,151人接受化疗。最常见的化疗是卡铂联合培美曲塞。
派姆单抗可以降低任何级别(73.4% : 90%)以及3级或更高级别(26.6% : 53.3%)的不良事件发生率。在接受派姆单抗治疗的患者中,有45例(29.2%)出现免疫介导的不良事件,最常见的是甲状腺功能减退(9.2%)、甲状腺功能亢进(7.8%)和肺炎(5.8%)。
此外,在因治疗导致的死亡事件中,接受派姆单抗治疗的占1例(0.6%),接受化疗的占3例(2%)。接受派姆单抗治疗的患者ORR较高(44.8%:27.8%)。
派姆单抗治疗组的中位FPS明显长于化疗组(10.3 vs 6个月,HR 0.50,P<0.01)。尽管两组均未达到中位数OS,但接受派姆单抗治疗的患者在6个月时的估计存活百分比也更高(80.2%:72.4%)。
来自Keynote-024的结果为未经治疗的NSCLC(排除EGFR突变或ALK易位)且肿瘤细胞PD-L1表达水平≥50%的患者建立了新的治疗标准,与标准化疗相比,其具有更少的毒性效应以及改善的ORR和PFS (Fig. 20.3)。
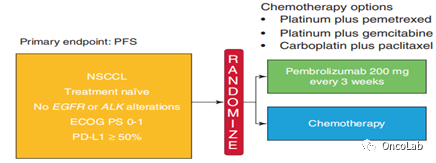
Fig 20.2 Keynote-024的设计。未经治疗的IV期NSCLC患者随机接受派姆单抗治疗或化疗。化疗方案分别为顺铂联合培美曲塞、卡铂联合培美曲塞、顺铂联合吉西他滨、卡铂联合吉西他滨、卡铂联合紫杉醇。
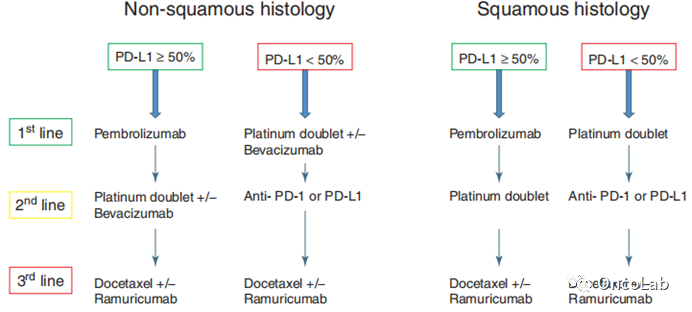
Fig 20.3 根据PD-L1的表达,治疗非癌基因驱动的晚期NSCLC的新算法
20.6 免疫检查点抑制剂疗效的预测因子
由于免疫检查点抑制剂对肿瘤的长期控制只在一小部分患者中体现,因此找到与免疫检查点抑制剂疗效相关的预测因子一直是人们非常感兴趣的。
研究最多的生物标志物是PD-L1,它可以通过免疫组织化学(IHC)检测到,通常在肿瘤细胞表面上调。多项研究表明,肿瘤缓解率与PD-L1表达之间存在关联,但没有PD-L1表达的患者也能受益。
在一项包括1567例接受免疫检查点抑制剂治疗的NSCLC患者的分析中,652例PD-L1阳性肿瘤患者的客观缓解率ORR为29%,而PD-L1阴性肿瘤患者的ORR为13%(相对比[RR]为2.08,95%CI为1.49-2.91,P<0.01)。
这种与PD-L1表达相关的ORR的区别在鳞癌和非鳞癌中都存在,与PD-L1阴性肿瘤相比,鳞癌的ORR分别为29%和14%,RR为2.12;95%CI为1.37-3.29,P<0.01;非鳞癌的ORR为32%和11%,RR为3.14;95%CI为2.15-4.54,P<0.01。
然而,虽然PD-L1阳性肿瘤患者24周的PFS显著高于PD-L1阴性肿瘤患者(35% : 26%,P<0.01),但两者1年的OS无差异 (28% : 27%,P=0.39)。
在7项对接受治疗的511名NSCLC患者的研究分析中也观察到了类似的结果,其中PD-L1阳性肿瘤患者的ORR更高(23.2% : 14.5%)。
预测针对PD-1或PD-L1的免疫检查点抑制剂作用效果的最合理和最直接的生物标志物是直接评估肿瘤细胞上PD-L1的表达量。然而,为了准确说明PD-L1的表达量,有几个因素需要考虑,包括PD-L1上调的机制、肿瘤浸润性淋巴细胞(TILs)的数量和IHC检测的方法。
PD-L1在肿瘤细胞中的表达可能是组成性的,也可能是适应性的(可诱导的)。这些机制不是相互排斥的,可以共存于同一肿瘤微环境(TME)中。
PD-L1的组成性表达是由于致癌途径的改变,包括9q24的扩增,其中包含PD-L1、PD-L2和JAK-2(PDJ扩增子),PTEN缺失,PI3K或AKT突变,以及MYC过表达。
干扰素(INF)也可以诱导PD-L1的表达,尤其是由激活的CD4辅助Th1细胞、激活的CD8细胞和自然杀伤(NK)细胞产生的INFγ。INFγ导致干扰素受体周围细胞中PD-L1表达上升,包括肿瘤细胞和TME内的细胞,如髓系细胞、基质细胞和T细胞(Fig. 20.4)。
诱导性表达比组成性表达更常见,其特征是肿瘤细胞和TILs结合处的PD-L1呈斑块状。相反,在大多数细胞中,组成性PD-L1表达更均匀,其PD-L1染色也因此更均匀。
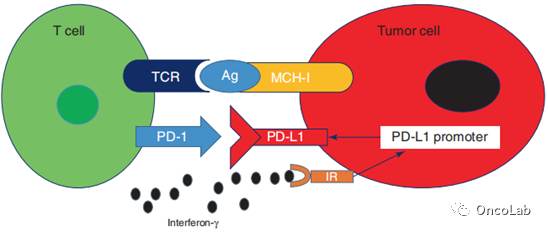
Fig 20.4 适应性免疫抵抗。INFγ结合干扰素受体(IR)导致PD-L1表达增加。
根据PD-L1表达的状态和TILs的存在,肿瘤可以分为四个不同的组(Fig. 20.5)。I型肿瘤具有TILs,且PD-L1呈阳性,而III型肿瘤有PD-L1表达,但没有TILs。II型和IV型肿瘤PD-L1呈阴性,前者无TILs,后者有TILs。
浸润性免疫细胞分泌的INFγ可以诱导肿瘤细胞表达PD-L1,I型肿瘤表现了肿瘤细胞对浸润的免疫细胞分泌的INFγ作出的适应性PD-L1诱导表达。而III型肿瘤表现为组成性PD-L1表达,这种表达与肿瘤细胞和INFγ分泌细胞之间的相互作用无关。
II型肿瘤既不表达TILs,也不表达PD-L1,可能代表免疫忽视,而在IV型肿瘤中,肿瘤细胞中存在TILs而没有诱导PD-L1表达,可能表明存在免疫耐受。
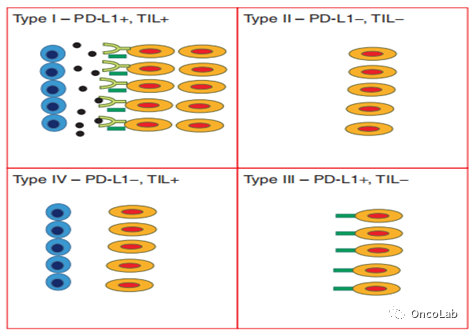
Fig 20.5 基于PD-L1表达和TILs的肿瘤分类
由于只有两个小的亲水性区域可用作IHC检测PD-L1的抗体的结合位点,与治疗性抗PD-L1的抗体相比,这些检测PD-L1的抗体会结合到PD-L1上的一个特殊位点。
此外,人们使用不同的IHC临界值来定义PD-L1阳性,并提供多种检测方法,而没有一个标准化的框架来比较这些方法,这使得解释结果和推断个别研究的结果变得困难。
程序性死亡配体1(PD-L1)IHC检测比较项目是为了解决抗体检测的标准化问题而启动的。在该项目的第一阶段,对38例NSCLC进行了4种最常用抗体的染色,包括DAKO 28-8、DAKO 22C3、Ventana SP142和Ventana SP263,它们分别用于纳武单抗、派姆单抗、阿特珠单抗(atezolizumab)和德瓦鲁单抗(duvalumab)的研究。
用DAKO和Ventana对肿瘤切片的抗体进行染色,然后对免疫染色玻片进行评估,由三名病理学专家对玻片上的PD-L1在TCs和ICs中的百分比进行独立评分。PD-L1染色的肿瘤细胞百分比在22C3、28-8和SP263检测中相当,而SP142检测的总体染色较低。
在以上四种检测方法中,有19例(50%)PD-L1染色均高于临界值,无论是哪种方法,都显示阳性结果;而5例(13%)均低于临界值。然而,14例(37%)PD-L1表达水平不一致,导致部分患者的PD-L1状态分类不同。免疫细胞上的PD-L1在四种检测方法中均有表达,但与TC表达相比,各检测方法之间的差异很大。
PD-L1检测的另一个问题是肿瘤的异质性。
在一项使用49例NSCLC活检组织标本的研究中,通过显色IHC和使用抗体E1L3N和SP142的自动定量免疫荧光来评估PD-L1在肿瘤细胞和间质中的表达。结果显示在不同的活检部位中,一些肿瘤的PD-L1表达结果不一致,有阳性区域,也有阴性区域。
在一项对109例肺腺癌患者进行的E1L3N抗体染色的研究中,PD-L1在原发肿瘤和N1转移的淋巴结之间有15-18%的表达差异,在原发肿瘤和N2转移的淋巴结之间有9.4-38%的表达差异,其差异的大小取决于阳性的分界值。
其他潜在的生物标志物包括突变负荷和驱动突变的因素的存在。由于突变后新肽的抗原性与其功能无关,没有功能作用的偶然突变可能会加强肿瘤抗原的抗原性,这表明更高的突变负荷可能会产生更多的新抗原,并增加患者从免疫检查点抑制剂受益的可能性。
事实上,黑色素瘤、NSCLC和膀胱癌等体细胞突变频率最高的肿瘤对免疫检查点抑制剂的反应的概率更高。
在一项评估34例NSCLC患者的研究中,将患者分为发现队列和验证队列。使用完整外显子组测序的突变负荷被评估可作为派姆单抗治疗的获益的预测因子。发现队列中的16位患者和验证队列中的18位患者的体细胞非同义突变的中位数分别为209和200。
在两个队列中,突变负荷高于中位数的患者的持久临床受益概率(DCB)(用部分缓解PR或稳定病情SD超过6个月来定义)和中位PFS显著升高。PD-L1阳性且非同义突变负荷高(200以上)的肿瘤患者,DCB高于低突变负荷的患者(91% : 10%)。
EGFR突变或ALK易位的患者通常不吸烟或轻度吸烟。由于不吸烟者的平均突变频率比吸烟者低十倍,因此推测不吸烟或轻度吸烟的患者从免疫检查点抑制剂中受益的概率较低。
在一项对58名接受抗PD-1或PD-L1抑制剂治疗的患者的研究中,野生型EGFR和ALK患者的ORR(23.3% : 3.6%,P=0.05)和中位PFS(2.58个月 : 2.07个月,HR=0.5,P=0.01)高于EGFR突变或ALK易位患者。
一种解释是由于在EGFR或ALK改变的患者中,TME内PD-L1表达和CD8阳性TILs的并存比率较低。
在一项对1903名患者的Meta分析中,将纳武单抗、派姆单抗或阿特珠单抗与多烯紫杉醇三项研究进行比较,根据EGFR状态对结果进行评估。在野生型EGFR患者中,使用抗PD-1或PD-L1抑制剂的免疫检查点阻断与OS显著改善相关(HR为0.66;95%CI为0.58-0.76)。相比之下,在EGFR突变肿瘤患者中,免疫治疗没有明显的效果(HR 为1.05;95%CI 为0.70-1.55)。
20.7总结
针对PD-1或PD-L1的免疫检查点抑制剂是治疗晚期NSCLC患者的重要步骤,在既往治疗的患者中该疗效明显优于多烯紫杉醇。最近,在既往未经治疗的并且TC PD-L1染色至少达到50%的肿瘤患者中发现,与一线铂基双联剂相比,PD-1或PD-L1的免疫检查点抑制剂可以使患者存活率提高。
此外,随机临床试验显示,与标准化疗相比,抗PD-1或PD-L1抗体的耐受性更好,这进一步提高了其被批准使用的可能性。然而,只能在一小部分患者中观察到这些免疫检查点抑制剂的益处,科研人员也一直在努力寻找可以预测治疗效果的因素。在TCs中进行PD-L1 IHC染色是一个不完美的生物标志物,因为在PD-L1阳性和阴性肿瘤中都能观察到免疫检查点抑制剂的治疗效果。
影响PD-L1染色准确性的可能因素包括,TILs对PD-L1表达的影响、现有抗体检验方法学之间的差异、阳性临界值以及肿瘤的异质性。例如,预计PD-L1阳性且具有TILs的(I型肿瘤)患者有适应性PD-L1表达,并且比PD-L1阳性但TILs很少或没有TILs的(III型肿瘤)患者更有可能从免疫检查点阻断中受益,但目前尚不清楚这些III型肿瘤患者的组成性PD-L1表达是否预示着他们能从免疫治疗中受益。
虽然与阳性染色相比,使用免疫检查点抑制剂治疗的PD-L1阴性IHC染色的NSCLC患者ORR较低,但即使是PD-L1阴性患者,其结果仍与多烯紫杉醇的标准化疗相似,且没有一项随机临床试验显示在二线化疗前给与免疫治疗会对生存造成不利影响。
此外,在EGFR突变的患者中,免疫检查点抑制剂与多烯紫杉醇相比,对PFS的影响既没有好处也没有坏处,这表明这些患者也适于接受抗PD-1或PD-L1抗体治疗。
缺乏PD-L1和TILs的(II型)肿瘤患者不太可能对单剂免疫检查点阻断有反应,这些患者可能是疫苗、抗CTLA-4或其他检查点抑制剂等联合治疗的最佳适用群体。
目前,针对PD-1或PD-L1的单剂单克隆抗体免疫治疗已成为晚期NSCLC患者的一种公认治疗方法,其帮助了许多患者减轻痛苦,延长寿命。尽管如此,该疗法仍有改进的空间,未来的研究可能会针对寻找确定这种疗法的最佳适用群体以及合理优化联合治疗的方案。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
本篇文章来源于微信公众号:OncoLab