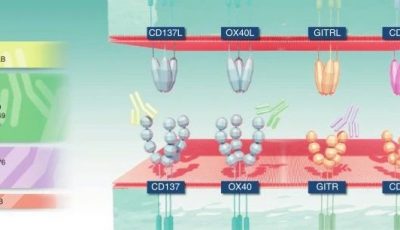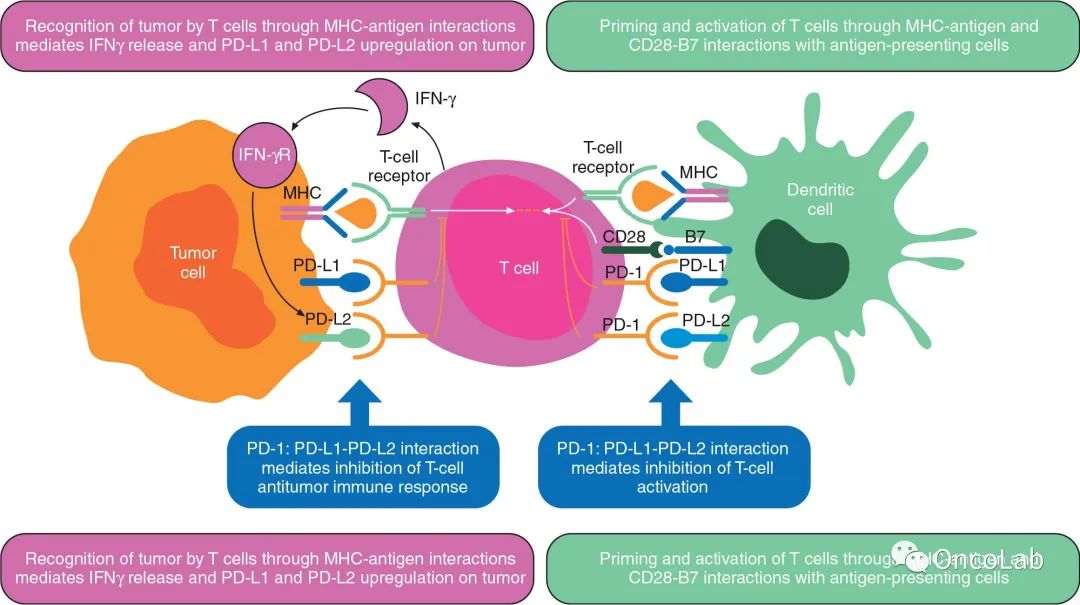
21.1 简介
肾细胞癌 ( RCC) 是最常见的肾癌类型,在美国是第八大常见癌症,发病高峰在 60 – 70 岁之间,男性居多。转移性肾细胞癌 (mRCC) 主要对细胞毒化疗耐药,也对放疗耐药。
基于几个有趣的观察结果,RCC 被认为是一种免疫反应性肿瘤。首先,在一些患者中发现转移性肺病灶可自发消退。其次,在 RCC 中,使用干扰素α (IFN-5α) 和白细胞介素 2 (IL-2) 等免疫刺激性细胞因子的免疫疗法也有一定的疗效,并且几十年来该免疫疗法一直是 mRCC 的标准治疗方法。
尽管 IL-2 可用于低剂量和高剂量方案,但美国食品和药品管理局 (FDA) 在 1992 年仅批准了高剂量方案。一项回顾性分析表明:在 259 名接受高剂量 IL-2 治疗的 mRCC 患者后,1986 年至 2006 年间报告的总体反应率 (ORR) 为 20%(9% 完全反应 (CR) 和 11% 部分反应 (PR))。
mRCC免疫治疗具有很大吸引力的原因之一是IL-2 疗法具有高 CR 率。但由于其非特异性抗肿瘤活性,IL-2 给药的剂量与药物的毒性相关,可引起全身炎症反应综合征和肝肾毒性。由于这些毒副作用,如今 IL-2 疗法的用途仅限于年轻和健康的合并症最少的患者。
晚期 RCC 的标准药物治疗包括血管内皮生长因子 (VEGF) 受体、酪氨酸激酶抑制剂 (TKI) 和哺乳动物雷帕霉素靶蛋白 (mTOR) 抑制剂。然而,尽管这些mRCC 靶向疗法的批准在改善临床结果方面取得了成功,但新诊断 mRCC 患者的中位总生存期 (OS) 仅为 22-29 个月,这凸显了该患者群体需要额外治疗的必要性。
21.2 PD-1及其配体在RCC中的作用
RCC 通常表现出显著的免疫细胞浸润,由多种细胞类型组成:T 细胞、自然杀伤 (NK) 细胞、树突状细胞 (DC) 和巨噬细胞。尽管有强烈的淋巴细胞浸润,但免疫功能障碍会促进 RCC 肿瘤的生长和逃逸。抗肿瘤反应受损的部分原因是肿瘤诱导的 DC 分化异常, 相关基因诱导的T 细胞耗竭。
越来越多的证据表明,新型免疫调节疗法可明显增强抗肿瘤免疫力。通常,活化的 T 细胞、B 细胞、NK 细胞、DC 和单核细胞表达 PD-1 以限制炎症状态(如感染)期间的自身免疫。许多肿瘤表达 PD-L1 ,以下调 T 细胞反应。
几项研究调查了 PD-1 和 PD-L1 表达在 RCC 中的生物学和预后作用。研究证实,PD-L1在原发性和转移性 RCC 标本中表达显著上调,但在正常肾组织中不表达 。Thompson 及其同事在196个肾切除标本中评估了PD-1和PD-L1的免疫组织化学 (IHC) 表达情况。PD-1 在 56% 的包含单核细胞浸润的患者肿瘤中表达,而不在 RCC 肿瘤细胞中表达。此外,PD-L1 表达与侵袭性肿瘤特征相关,例如较高的肿瘤淋巴结转移 (TNM) 阶段、坏死或肉瘤样分化的存在以及癌症特异性死亡率的风险增加。此外,Frigola 等人通过 ELISA 在一系列 172 名 RCC 患者中量化可溶性 PD-L1。显示较高水平的 PD-L1、侵袭性病理特征和死亡风险增加之间存在显着关联。
PD-1和PD-L1 都在CD4 + CD25 + 调节性 T 细胞 (Tregs) 上表达,但它们是否影响Tregs的功能尚不完全清楚。Tregs 浸润理论上可促进 RCC 的促血管生成表型,并与 RCC 的分期和等级相关。有趣的是,舒尼替尼和索拉非尼治疗都降低了肿瘤浸润性 Treg 的百分比,而依维莫司(一种免疫抑制剂和酪氨酸激酶抑制剂)改善了肿瘤浸润性 Treg 的百分比。正如在其他肿瘤组织学中所观察到的那样,在 RCC 患者的外周血和肿瘤浸润淋巴细胞群中可见(FOXP3 +CD4 + CD25 + )Treg 或肿瘤浸润性 PD-1 阳性淋巴细胞数量增加,并且与较差的预后结果相关 。
此外,淋巴细胞浸润中 NK 细胞的比例升高预示着 RCC 的预后较好。索拉非尼和舒尼替尼已被证明可增加肿瘤细胞对 NK 细胞杀伤 RCC 细胞的敏感性。Choueiri 等人在比较舒尼替尼和帕唑帕尼作为 mRCC 患者一线治疗的 COMPARZ 研究的子分析中,显示增加的PD-L1肿瘤表达以及肿瘤 CD8+ T 细胞计数与接受帕唑帕尼或舒尼替尼治疗的患者的 OS 较短有关。
所有这些数据都支持前瞻性试验调查的结果,验证了 PD-L1 作为 RCC TKI 治疗前后的潜在生物标志物的必要性。
21.3 RCC 中的抗 PD-1 研究
21.3.1 Ⅰ期试验
纳武利尤单抗 (Nivolumab) 是一种对 PD-1 具有特异性阻断作用的全人源单克隆 IgG4 抗体,其安全性和耐受性首次在一项针对 39 名患有mRCC、黑色素瘤、结直肠癌、去势抵抗性前列腺癌 (CRPC) 、非小细胞肺癌 (NSCLC) 患者的 I 期剂量递增研究中得到证实。不过本研究中只有一名患者患有 RCC。
在以 0.3、1、3 或 10 mg/kg 剂量递增的六名患者队列后,该研究在最大耐受剂量 (MTD) 或 10 mg/kg 的扩展队列中招募了 15 名患者。患者接受一剂纳武利尤单抗并每周监测毒性。影像学重新分期在第 8 周和第 12 周进行。没有进展性疾病 (PD) 或 3 级不良事件 (AE) 的患者在第 12 周和第 16 周接受了额外剂量(初始剂量)。没有剂量限制该试验中的毒性(DLT),因此未确定 MTD。所以,15 名患者的扩大队列以 10 mg/kg 的剂量入组。总体而言,该药物耐受性良好,最常见的 2 级或更高毒性是 CD4+ 淋巴细胞计数减少 (35.8%)、淋巴细胞减少 (25.7%)、肌肉疲劳 (15.4%) 和肌肉骨骼疼痛 (15.4%)。唯一的 3 级免疫相关不良事件是炎症性结肠炎(一名患者),并且对皮质类固醇和英夫利昔单抗治疗反应良好。总体而言,1 名患者 (2.5%) 获得 CR,2 名 (5%) 患者获得 PR,2 名 (5%) 患者出现混合反应,定义为某些病变消退而其他病变同时进展。独特的 RCC 患者在接受 10 mg/kg 的三剂后 PR 延长(超过 16 个月)。
在一项扩大的 I 期试验中进一步证明了纳武利尤单抗在 RCC 中的安全性和有效性,该试验招募了晚期 RCC、NSCLC、黑色素瘤、结直肠癌或 CRPC 的患者。计划在 8 周的周期中每 2 周 1.0、3.0 或 10.0 mg/kg 的连续给药。研究中没有使用最大耐受剂量 (MTD) 或 10 mg/kg 的扩展队列。最终纳入了 296 名患者,其中 34 名患者患有晚期 RCC,并且接受过肾切除术、免疫治疗和/或 TKI 治疗。在该试验中,纳武利尤单抗似乎具有更好的安全性:296 名患者中只有 15 名 (5%) 因 AE 停止治疗。总共有 70% 的患者表现了与治疗相关的 AE,14% 的患者表现了 3 级或 4 级事件。在至少 10% 的患者中发生的唯一与治疗相关的 AE 是肌肉疲劳 (24%)、皮疹 (12%)、腹泻 (11%) 和瘙痒 (10%)。发生不超过 1% 的 3/4 级治疗相关毒性。现实中不常见严重的免疫相关 AE ,仅在不到 1% 的接受治疗的患者中观察到。然而,在 NSCLC(2 名患者)和结直肠癌(1 名患者)组中发生了 3 例继发于肺炎的药物相关死亡。
在所有测试剂量中均观察到抗肿瘤活性。整个 RCC 队列的 ORR 为 27%。5 名在数据分析前 1 年以上开始治疗并达到客观缓解的患者具有至少 1 年的持久缓解。RCC 队列在 24 周时的 PFS 为 56%。三年后,最后一名患者在随后的报告中参加了这项扩大的 I 期研究;34 名患者 mRCC 队列报告了额外的疗效、存活率和长期安全性。在分析时,生存随访的半数生存期(中位生存期)为 45.2 个月(范围,25.9-57.9)。
总体而言,34 名患者中有 10 名(29%)出现客观反应。中位反应持续时间为 16 周(范围为 8-48 周)。40% 的响应者在第 8 周(第一次放射影像学评估)时达到了响应,大多数(70%)在 16 周时达到了响应。中位反应持续时间为 12.9 个月。十名响应者中有五名因 PD 以外的原因停止治疗。其中四名患者接受了治疗,持续反应时间为 19 至 56 周以上。除了有客观反应的 10 名 (29%) 患者外,9 名 (27%) 的患者病情稳定 (SD) 至少 24 周。在分析时,34 名患者中有 19 名(56%)死亡。中位 OS 为 22.4 个月(95% CI,12.5–NR)。3年生存率为44%。中位 PFS 为 7.3 个月(95% CI,3.6-10.9),2 年 PFS 率为 12%。
总体而言,85% (29/34) 的患者报告了任何级别的治疗相关 AE。最常见的是肌肉疲劳 (41%)、皮疹 (27%)、腹泻 (14%) 和瘙痒 (14%)。6 名 (18%) 患者报告了 3 级或 4 级治疗相关 AE,但这些 AE 是可逆的。
21.3.2 Ⅱ期试验
基于有效的毒性数据和 I 期试验中有希望的疗效,进行了一项使用纳武利尤单抗的随机 II 期试验。168 名患者随机接受每 3 周一次的纳武利尤单抗治疗,剂量为 3 种不同剂量:0.3 mg/kg(60 名患者)、2 mg/kg(54 名患者)或 10 mg/kg(54 名患者)一次。主要终点是比较不同剂量组的 PFS,以确定是否存在剂量反应关系。次要终点包括 ORR、OS、反应时间、反应持续时间和安全性。
PFS 没有剂量反应关系,中位 PFS 为 2.7 个月(80% CI,1.9-3.0)、4.0 个月(80% CI,2.8-4.2)和 4.2 个月(80% CI,2.8-5.5)分别为 0.3、2 和 10 mg/kg 组(p 值 0.9)。0.3 mg/kg 组的 ORR 为 20%,2 mg/kg 组为 22%,10 mg/kg 组为 20%(p 值 1.0)。所有组的反应时间相似,中位数为 2.8-3.0 个月,范围为 1.3-10 个月。0.3 mg/kg 和 2 mg/kg 组未达到缓解持续时间 (NR),但 10 mg/kg 组为 22.3 个月 (80% CI, 4.8–NR)。0.3 mg/kg 组的中位 OS 为 18.2 个月 (80% CI, 16.2–24.0),2 mg/kg 组为 25.5 个月 (80% CI, 19.8–28.8),以及 24.7 (80% CI, 15.3– 26.0) 在 10 mg/kg 组中。
在分析时,在35 名有客观反应的患者中有 40% 在治疗开始后至少 24 个月仍有反应。73% 的患者报告了至少一种与治疗相关的 AE,19 名(11%)患者经历了 3 级或 4 级治疗相关的 AE。肌肉疲劳是最常报告的 AE(81% 的患者)。一般而言,各队列中治疗相关 AE 的发生率没有显着差异。没有 3 级或 4 级肺炎病例。治疗相关的 AE 导致 11 名患者 (7%) 停药。在 0.3、2 和 10 mg/kg 组中,分别有 1 名 (2%)、6 名 (11%) 和 4 名 (7%) 患者因治疗相关 AE 停止治疗。导致停药的治疗相关 AE 涉及心脏、内分泌、呼吸、胸部或神经系统疾病。
与 I 期试验相比,Ⅱ期没有与治疗相关的死亡。总之,随机 II 期试验表明,经过大量预处理的 mRCC 患者可以在安全范围内耐受纳武利尤单抗,ORR 为 20-22%,40% 的反应者持续反应超过 2 年。0.3、2 和 10 mg/kg 组之间没有剂量反应关系,所有组的安全性都是可控的。
基于 I 期和 II 期试验中各种给药组合的临床疗效和安全性,选择以每 2 周 3 mg/kg 的剂量进行其他研究。
21.3.3 Ⅲ期试验
CheckMate 025 研究是纳武利尤单抗与依维莫司在晚期 RCC 患者中的 III 期随机试验。821 名既往接受过至少一种(72% 的患者)但不超过 2 种 TKI 治疗的晚期 RCC 患者以 1:1 的比例随机接受 3mg/kg 的纳武利尤单抗治疗,每 2 周60分钟静脉输注,且10 mg 口服依维莫,直到疾病进展或不可接受的毒性。试验的主要目标是OS。关键的次要目标包括 ORR、研究者确定的 PFS 和缓解持续时间 (DoR)。截至 2015 年 6 月 18 日试验截止日期,当 398 例死亡(最终分析的计划事件数的 70%)发生时,进行了中期 OS 分析。
与纳武利尤单抗组患者的 OS 相比,有统计学意义的改善依维莫司组患者的中位 OS 差异为 5.4 个月(从 19.6 个月到 25.0 个月),HR 为 0.73(95% CI,0.60-0.89;p 值 0.0018)。根据研究者的评估,PFS 证实,纳武利尤单抗组和依维莫司组的 ORR 分别为 21.5% 和 3.9%,中位缓解持续时间分别为 23.0 个月和 13.7 个月。纳武利尤单抗组的 ORR 高于依维莫司组(25% vs 5%;优势比 5.98;95% CI,3.68-9.72;p 值 < 0.001)。
在纳武利尤单抗组有反应的患者中,31% 的治疗反应超过 12 个月。最后,两组反应的中位时间似乎相似。在 OS 分析时,还检查了每个研究者评估的 PFS。观察到两个治疗组之间的 PFS 没有统计学上的显着差异。纳武利尤单抗组的中位 PFS 为 4.6 个月,依维莫司组为 4.4 个月。分层 HR 为 0.88(95% CI,0.75-1.03),双边对数秩 p 值为 0.11。考虑到亚组分析,对于 MSKCC 风险较低的患者,值得注意纳武利尤单抗与依维莫司的好处(HR 0.48,95% CI 0.32–0.70)。
本研究中的副作用:接受纳武利尤单抗治疗的患者中有 79% 有治疗相关 AE,通常是肌肉疲劳、恶心和瘙痒。只有 19% 的患者出现 3 级或 4 级 AE(2% 的贫血和 1% 的疲劳、肺炎和腹泻)。16% 的纳武利尤单抗治疗患者和 19% 依维莫司治疗的患者因不良反应停止研究治疗。接受纳武利尤单抗治疗的患者中有 44% 因不良反应出现药物延迟。对于纳武利尤单抗治疗组或使用最后一剂研究药物后,30 天内的死亡率为 4.7%,而依维莫司组为 8.6%。根据本研究显示的证据,2015 年 11 月,纳武利尤单抗获 FDA 批准用于先前经过抗血管生成治疗后的晚期肾癌治疗,并于 2016 年进一步获 EMA 批准。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab