1.非抗原相关的树突状细胞疗法
Michele De Palma – 瑞士洛桑联邦理工学院 (EPFL),洛桑,瑞士
树突状细胞疫苗通常由脉冲肿瘤裂解物或肿瘤相关抗原的单核细胞来源的树突状细胞制成,但这类疫苗的临床疗效往往未能达到预期。Michele De Palma假设,这可能与抗原的不完全识别和/或使用单核细胞来源的DCs有关,这些DCs容易从单核细胞祖细胞中产生,但相比专业抗原呈递细胞(如cDC1s)交叉呈递能力较弱,cDC1s来源于共同的DC祖细胞(DCP)。
假设DCP可能是治疗性DCs的更好来源,De Palma开发了一种使用细胞因子混合物从造血干细胞和祖细胞(HSPCs)产生DCPs的方法。通过将DCPs移植到小鼠后,它们成熟为仅限于不成熟DCs、cDC1s和cDC2s,并比单核细胞来源的DCs更有效地嵌入脾脏。研究者发现,这些小鼠的总cDC1和cDC2群体(包括内源性细胞)中,多达50%的cDC1来自移植物,这表明DCPs即使在没有调节的情况下也能支持DC的再生。
为了进一步增强DC在体内的功能,De Palma及其同事将DCPs工程化,使其产生支持DC发育的FLT3L和/或有助于诱导T细胞免疫的IL-12。在移植后,可以在DC分化或死亡之前的短暂时间窗口内检测到增加的循环FLT3L和IL-12水平。在移植B16F10黑色素瘤细胞的小鼠中,单独表达FLT3L的DCPs未能诱导肿瘤控制,表达IL-12的DCs诱导了一定程度的肿瘤控制,而两者结合则诱导出强大的抗肿瘤控制作用,阻止了肿瘤的发展。与此一致,IL-12表达增加了CD4+和CD8+ T细胞浸润到肿瘤中,而与FLT3L表达的结合在增加T细胞浸润和IFNγ产生方面表现出明显的协同作用。
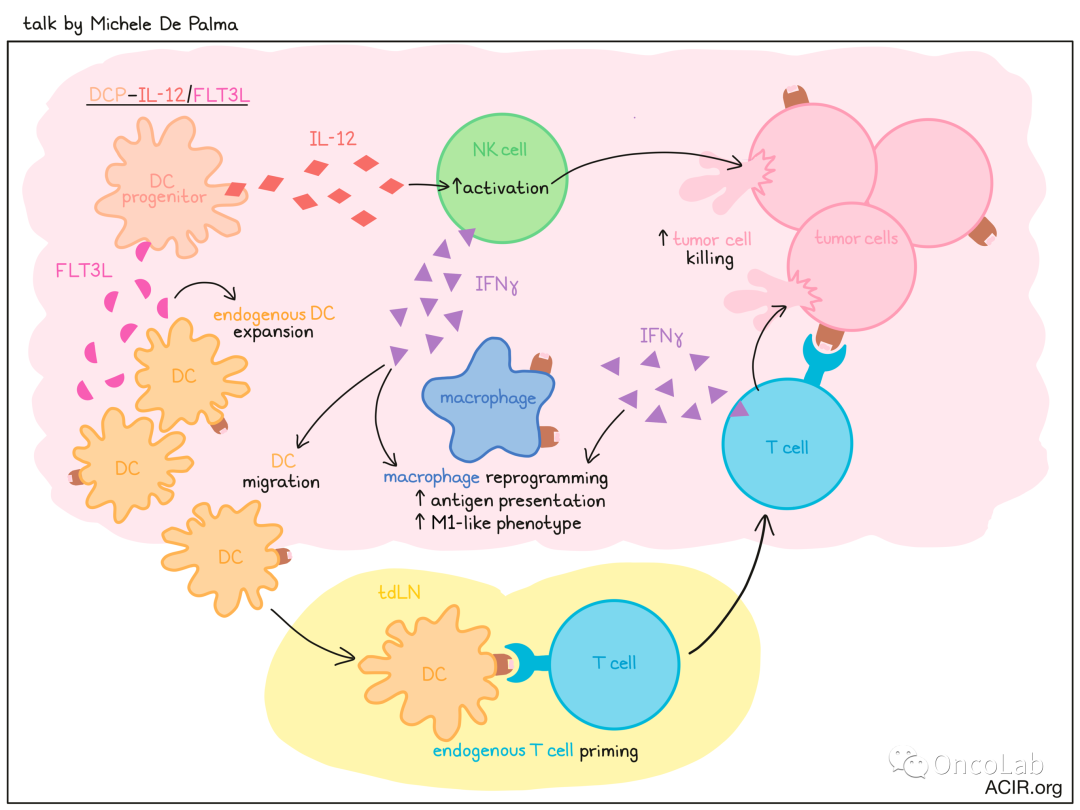
此外,单细胞RNA测序显示黑色素瘤和髓样细胞中保守的I型和II型干扰素应答,表明DCP-IL-12/FLT3L广泛激活了肿瘤微环境中的IFNγ信号传导。进一步研究这种抗原不敏感抗肿瘤作用背后的机制发现,DCP-IL-12/FLT3L通过FLT3L诱导内源性DCs的扩增,并通过IL-12激活NK细胞。被激活的NK细胞产生IFNγ,这有助于DC迁移到肿瘤引流淋巴结,在那里DC进一步扩增并引发内源性T细胞。然后,被激活的T细胞穿过到肿瘤部位,诱导抗肿瘤免疫反应,并提供额外的IFNγ,这同时可以支持巨噬细胞转变为可呈递抗原的M1样表型。工程化的单核细胞来源的DCs表达FLT3L和IL-12的效果则较差。
最后,De Palma描述了一项实验,其中将DCP-IL-12/FLT3L与GD2-CAR T细胞联合应用于携带GD2表达的胶质瘤小鼠。尽管DCP-IL-12/FLT3L细胞和GD2-CAR T细胞作为单一疗法均无效,但它们的组合诱导了强烈的抗肿瘤反应,许多小鼠经历了完全缓解和生存,即使在细胞水平的成像中也未检测到胶质瘤。凭借这些令人印象深刻的体内结果,De Palma希望这种策略能成功转化到临床应用。
2.靶向肿瘤中髓样细胞的基础和临床影响
Judith A. Varner – 加州大学圣地亚哥分校(UCSD)Moores癌症中心,La Jolla,CA
巨噬细胞与肿瘤进展和治疗耐受性有关,并且数量很多,可占肿瘤中细胞的30-60%。Judith Varner提出了两种靶向TAMs的方法:抑制骨髓来源巨噬细胞的肿瘤募集,或将巨噬细胞重新极化为促炎症M1表型。
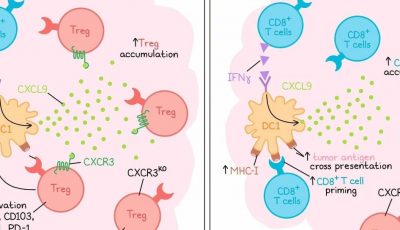
Varner及其团队鉴定出PI3Kγ,因其在髓样细胞中的主要表达和在炎症过程中髓样细胞募集和极化中的作用。抑制PI3Kγ可促使巨噬细胞向M1表型极化,与炎症和抗原呈递相关基因的增加和免疫抑制因子编码基因的表达减少有关。从机制上讲,PI3Kγ抑制改变了巨噬细胞的染色质可及性并改变了转录。在许多肿瘤模型中,治疗性抑制PI3Kγ减少了肿瘤生长和转移,但效果根据肿瘤微环境而异。炎症肿瘤反应更好,与T细胞激活、先天免疫和抗原呈递相关的基因上调,肿瘤相关巨噬细胞上MHC II类表达增强。
针对髓样细胞的T细胞非炎症Lewis肺癌的单细胞分析证实,与野生型小鼠相比,PI3Kγ敲除小鼠的MHC I类和II类分子表达更高。在一个HPV+头颈肿瘤模型中,PI3Kγ抑制与抗PD-1治疗协同作用,增加了长期生存。此外,研究人员观察到肿瘤内CD8+ T细胞、颗粒酶B、IFNγ和IL-12表达的协同增加,以及CD4+ T细胞的减少。单细胞分析揭示了髓样细胞群体向促炎表型的转变,与野生型肿瘤相比,PI3Kγ敲除肿瘤中IFNγ反应和MHC相关基因的增加。PI3Kγ抑制增加了肿瘤中活化效应和效应记忆CD8+ T细胞以及活化NK细胞的数量,促进T细胞招募,减轻耗竭并促进TCR多样性。PI3Kγ抑制的抗肿瘤作用依赖于CD8+ T细胞、IL-12和IFNγ。与检查点抑制剂结合,PI3Kγ抑制促进了长期持久的免疫记忆,治疗动物的脾脏中效应记忆T细胞增加。
在一个临床试验中,IPI-549(eganelisib),一种首创口服PI3Kγ选择性抑制剂,与nivolumab作为二线治疗联合使用,在晚期顽固性铂类耐药性膀胱癌患者中降低了42%的死亡风险。应答患者在外周血中表现出与抗原呈递、IFNγ信号和TCR信号相关的基因集富集,这与肿瘤模型中的发现一致。Varner及其同事还确定了Treg生物标志物整合素β8(ITGB8)作为一种抗性因子。在接受联合治疗的患者中,CD4+ T细胞高度表达ITGB8,抑制ITGB8和PI3Kγ在动物模型中显示出协同的抗肿瘤效果。

加入读者交流群~
(添加请备注单位姓名)

关注本号~
本篇文章来源于微信公众号:OncoLab