-
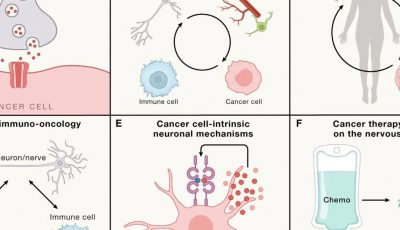
免疫炎症型(inflamed):肿瘤周围有免疫细胞浸润
-
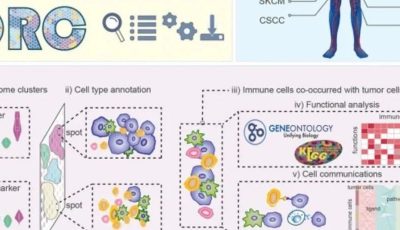
免疫排除型(Immune exclued):肿瘤微环境排除肿瘤浸润淋巴细胞TILs
-
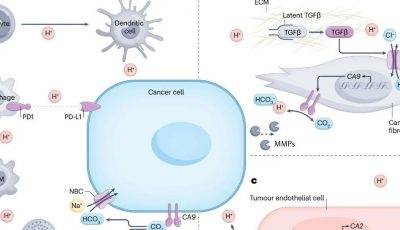
免疫沙漠型(Immune desert):免疫细胞远离肿瘤细胞,微环境基本无免疫细胞。
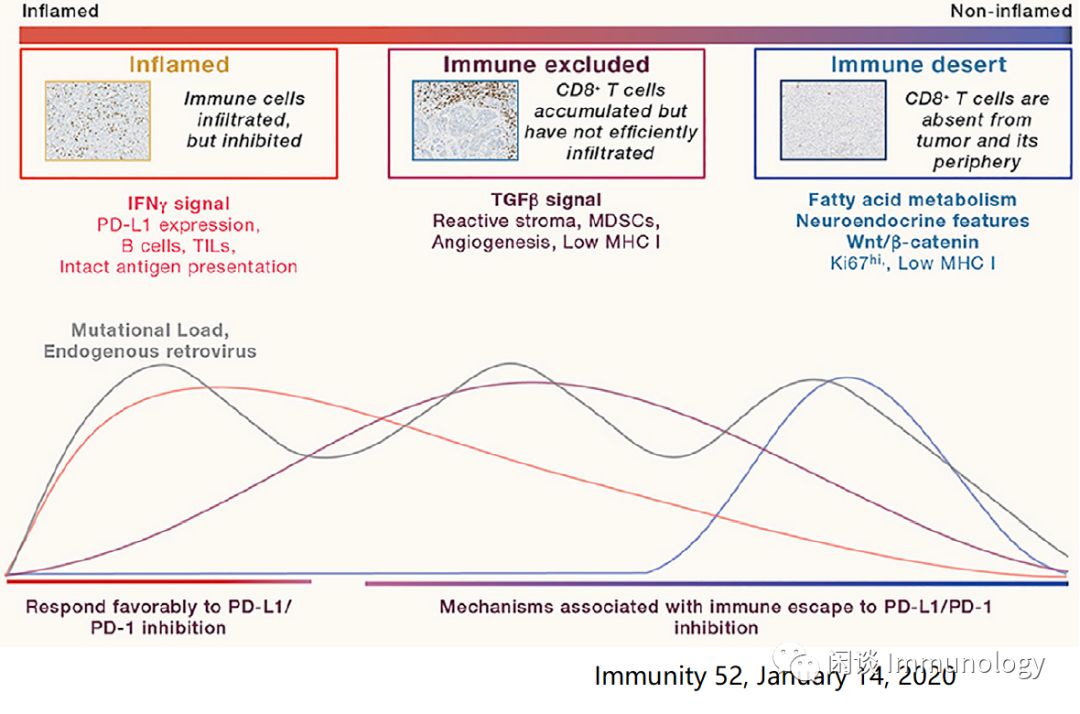
免疫排除型肿瘤
3#
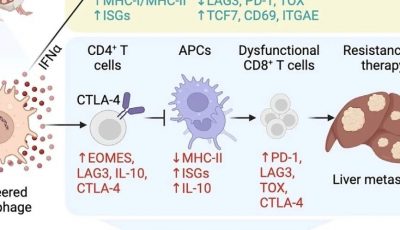
免疫沙漠型肿瘤
-
Hegde, P.S., Karanikas, V., and Evers, S. (2016). The Where, theWhen, and the How of Immune Monitoring for Cancer Immunotherapies in the Era of Checkpoint Inhibition. Clin. Cancer Res. 22, 1865–1874.
-
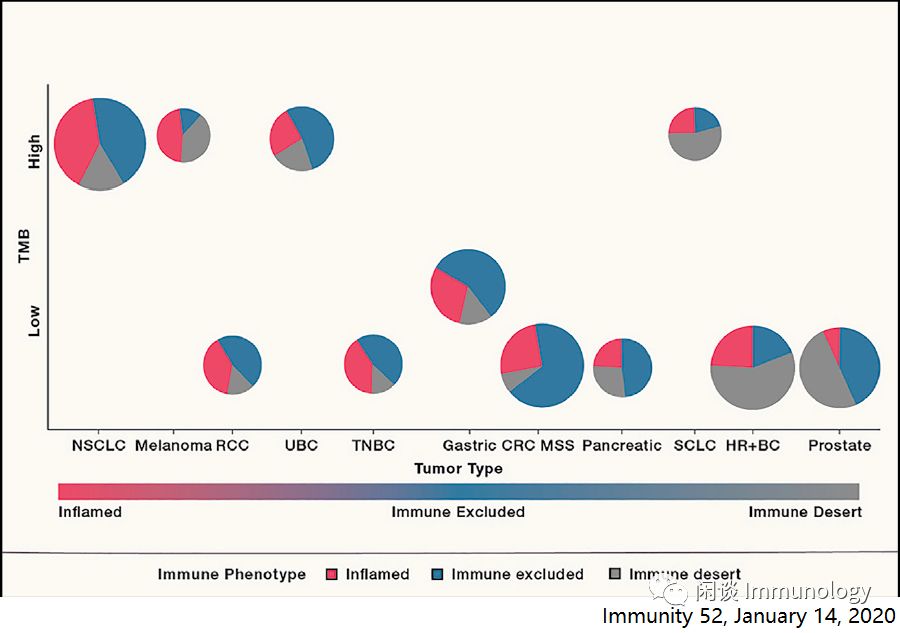
Marabelle, A., J.A., Miller, A., et al.(2019). Association of tumor mutational burden with outcomes in patients with select advanced solid tumors treated with pembrolizumab in KEYNOTE-158. ESMO 2019 Congress. Ann. Oncol. 30, v475–v532.
-
Mariathasan, S, et al. (2018). TGFb attenuates tumour response to PD-L1 blockade by contributing to exclusion of T cells. Nature 554, 544–548.
-
McDermott, D.F, et al. (2018). Clinical activity and molecular correlates of response to atezolizumab alone or in combination with bevacizumab versus sunitinib in renal cell carcinoma. Nat. Med. 24,749–757.
-
Top 10 Challenges in Cancer Immunotherapy,Priti S. Hegde and Daniel S. Chen,Immunity 52, January 14, 2020
-
McDermott, D.Fet al. (2018). Clinical activity and molecular correlates of response to atezolizumab alone or in combination with bevacizumab versus sunitinib in renal cell carcinoma. Nat. Med. 24,749–757.
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。
关注本号~

加入读者交流群~

加入知识星球~
用于OncoLab读者交流互助永久免费
本篇文章来源于微信公众号:OncoLab