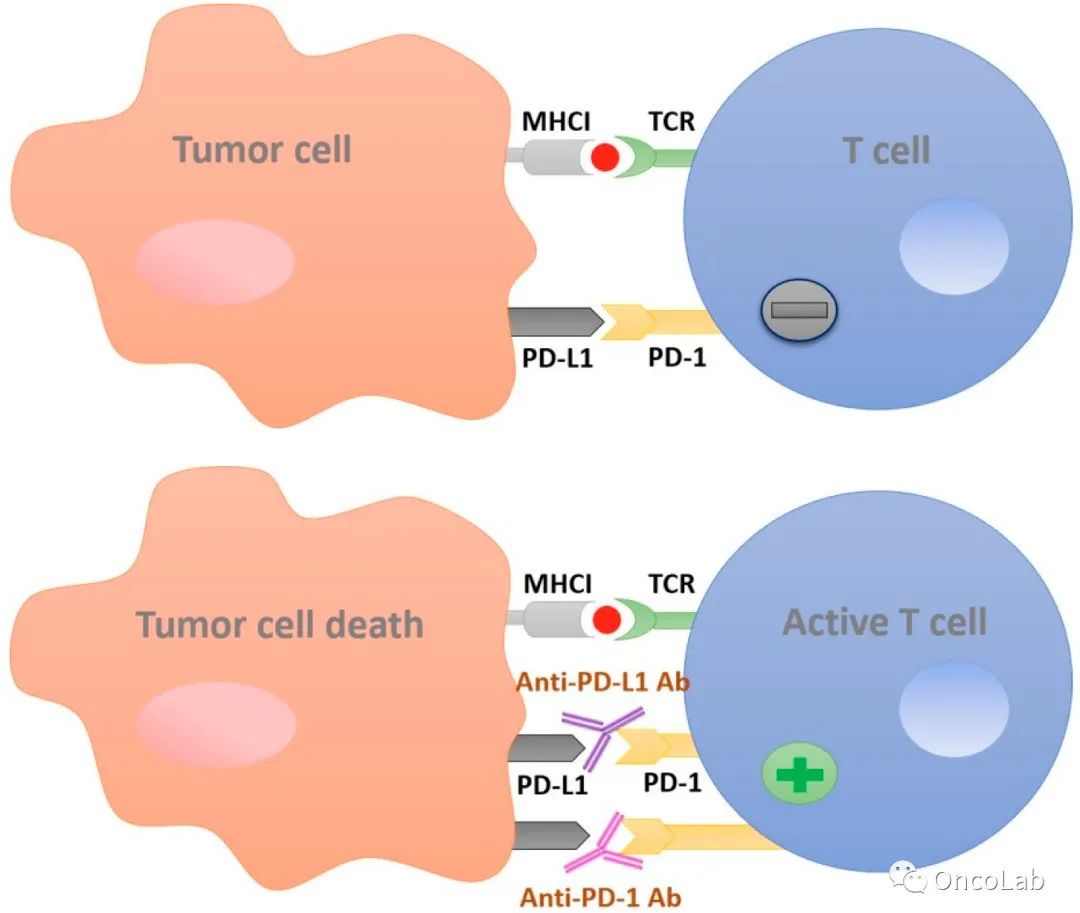
19.7 Pembrolizumab(派姆单抗)
2014年9月,FDA批准派姆单抗(以前称为MK3475或兰博利珠单抗)用于晚期黑色素瘤治疗。2015年7月,EMA以下面三项试验为依据,批准派姆单抗运用于晚期黑色素瘤治疗:一期试验KEYNOTE-001、二期试验KEYNOTE-002和三期试验KEYNOTE-006。
在KEYNOTE-001试验中,分别选取有和没有接受过系统治疗的黑色素瘤患者(共135名)接受派姆单抗治疗,三个分组剂量分别为每2周10mg/kg(体重)、每3周10mg/kg(体重)、每3周2mg/kg(体重)。所有剂量组中,全群组患者的客观缓解率(ORR)为38%,总体无进展生存期(PFS)中位数>7个月。
在随机扩大队列试验中,173例对伊匹单抗和BRAF抑制剂(针对BRAF(V600)突变型黑色素瘤)治疗无效的黑色素瘤患者接受了派姆单抗治疗,两个分组剂量为每3周2mg/kg(体重)、每3周10 mg/kg(体重)。两个剂量组的ORR、中位PFS和一年生存率没有显著差异。但是值得注意的是,这项试验表明,接受伊匹单抗预治疗的患者对纳武单抗治疗也会产生反应。
在KEYNOTE-002随机试验中,540名患者随机接受剂量为2mg/kg(体重)和10mg/kg(体重)的派姆单抗治疗或化疗治疗。参与这项研究的患者均接受过伊匹单抗和BRAF抑制剂(针对BRAF(V600)突变黑色素瘤)的预治疗。
在接受治疗的9个月后,与接受化疗的患者相比,接受派姆单抗两种剂量中任何一种剂量治疗的患者的PFS率都显著高于接受化疗治疗的患者:接受派姆单抗2mg/kg(体重)和10 mg/kg(体重)治疗的患者的PFS率分别为24%和29%,而接受化疗的患者的PFS率仅为8%。
三期随机试验Keynote-006的参试者为834名未曾接受过系统治疗的患者,它们在该试验中将接受派姆单抗或伊匹单抗治疗(Table 19.1)。
派姆单抗以10 mg/kg(体重)的剂量分别每2周和每3周给药一次,而伊匹单抗分4次给药,每3周3 mg/kg(体重)。
接受派姆单抗每2周和3周给药治疗的患者的6个月PFS率分别为47.3%和46.4%,而接受伊匹单抗治疗的患者为26.5%。
派姆单抗每2周和每3周给药组的患者1年生存率分别为74.1%和68.4%,而伊匹单抗组为58.2%。派姆单抗的有效率约为33%,而伊匹单抗则为12%。
两项研究中期分析显示,接受派姆单抗治疗的患者的总生存期(OS)增加,这项结果导致该研究提前终止,随后接受伊匹单抗的患者将使用派姆单抗进行交叉治疗。
在治疗毒性方面,与伊匹单抗(或化疗)相比,接受派姆单抗治疗的患者发生不良事件(AE)的频率和严重程度都较低。最常见的AE是乏力、腹泻、内分泌紊乱、皮疹和瘙痒。此外,10-13%的派姆单抗治疗患者(以不同的周间隔给药)和19.9%接受伊匹单抗治疗的患者发生3级或4级药物相关AE。
总而言之,派姆单抗治疗的有效率在30%到40%之间,显著高于伊匹单抗。接受过伊匹单抗预治疗的黑色素瘤患者再接受派姆单抗治疗,依然取得了良好的效果,这加速了FDA对派姆单抗临床运用的批准。
由于在各项试验中发现,派姆单抗不同剂量和时间的治疗方案并未存在显著差异,所以批准使用的剂量定为每3周给药2mg/kg(体重)。
19.8 抗PD-1/抗CTLA-4联合疗法
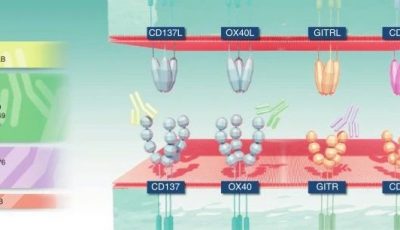
由于与PD-1和CTLA-4受体结合的配体种类不同,且配体表达在不同细胞类型上。所以,为了明确针对这两个检查点的阻断抗体是否具有协同或增效的作用,研究人员开展了联合试验。
在CHECKMate-067试验中,945名黑色素瘤患者在没有接受过治疗的情况下,接受了纳武单抗和伊匹单抗的联合治疗,或者单独接受纳武单抗或伊匹单抗治疗(随机化1:1:1)。
与单独使用纳武单抗(PFS,6.9个月;ORR,43.7%)或伊匹单抗(PFS,2.9个月;ORR,19.0%)的患者相比,接受联合治疗的患者的PFS(11.5个月)和ORR(57.6%)明显更高。
在接受纳武单抗/伊匹单抗联合治疗的患者中,11.5%的患者的症状得到了完全缓解。相比之下,在单独接受纳武单抗或伊匹单抗治疗的患者中,分别只有8.9%和2.2%的患者症状得到了完全缓解。
使用联合疗法治疗患者的死亡或肿瘤进展风险,较单独使用伊匹单抗的患者降低了58%。
联合治疗组虽然具有更好的疗效,但我们不能忽视它带来的严重毒副作用:接受联合治疗的患者中有55%的患者发生了3级和4级的AE。而单独接受纳武单抗和伊匹单抗治疗的患者中,分别只有16.3%和27.3%的患者会出现3级和4级的AE。
有趣的是,研究结果表明,对PD-L1阴性的肿瘤患者(通过免疫组织化学确定)来说,与纳武单抗单药治疗相比,纳武单抗/伊匹单抗联合治疗的有效率更高,而在PD-L1阳性肿瘤患者则没有观察到这种差异。
基于这一结果,纳武单抗/伊匹单抗联合疗法于2016年被FDA批准用于治疗患有PD-L1阴性肿瘤的晚期黑色素瘤患者。而在欧洲,不论PD-L1的表达如何,都可以被允许使用该联合疗法。
总而言之,抗PD-1和抗PD-1/CTLA-4联合疗法在特定的患者亚组中可以诱导显著的临床反应。但需要注意的是,大多数患者对免疫检查点抑制剂具有原发性的耐药性。同时在免疫检查点抑制剂使用后期,机体对药物出现的继发性耐药也是一个需要注意的问题。
19.9 与抗PD-1治疗应答相关的生物标志物
为了确定最有可能从抗PD-1治疗中受益的患者群体,研究人员对经过预处理的活检采样进行了大量筛选,以寻找可用于预测患者对抗PD-1疗法有效性的生物标志物,但是目前仍未找到。
虽然在几个临床试验中,都已经明确了可以通过免疫组化标记肿瘤标本是否是PD-L1阳性,但是由于使用的染色抗体及判定PD-L1阳性的临界值尚未统一,各试验的结果几乎不具有可比性。
此外,虽然PD-1检查点阻断疗法对PD-L1阳性肿瘤患者有效率更高,但抗-PD1疗法对PD-L1阴性肿瘤患者也有效果。
同时,与CD8+T细胞在治疗过程中被重新激活并启动临床反应的特性一致的是,目前已经明确了肿瘤实质内和病变边缘存在的浸润性淋巴细胞与机体抗PD-1治疗的应答有关,针对新抗原的特异性T细胞在其中发挥着最重要的作用。
根据这一点,我们可以知道,决定新抗原数量的黑色素瘤突变负荷与患者对抗CTLA-4治疗的应答有关,但到目前为止,这种关联尚未见于抗PD-1治疗。
为更好预测患者对抗PD-1治疗是否出现应答,我们需要联合多个生物标记物,将它们作为共同的判断指标。未来,科学家们将继续深入研究,明确更多可有效用于预测患者对抗PD-1治疗应答的生物标志物。
19.10 对治疗的耐药性
为阐明介导机体对PD-1免疫检查点阻断的耐药机制,临床医生和科学家展开了密切合作。目前发表的研究表明,这些耐药机制是多方面的。
正如最近几篇综述中总结的那样,可以大致将这些机制分为:肿瘤内在因素和肿瘤外在因素。
后者包括肿瘤微环境中不同免疫调节细胞(调节性T细胞、髓源性抑制细胞、中性粒细胞) 的活性,这些免疫调节细胞在本书的其他章节中都有介绍。
在这里,我们将重点介绍黑色素瘤的内在因素,这些因素已被确定与机体抗PD-1治疗的免疫耐受相关,包括机体的原发性耐药和继发性耐药。
黑色素瘤的遗传具有不稳定性,一方面可产生治疗相关的新抗原,另一方面也产生了可以抵抗治疗的肿瘤细胞,使其发生克隆性增生,促进黑色素瘤细胞进化以逃避免疫杀伤。
所以,我们能从一名最初对抗PD-1抗体治疗有反应,但后期出现进展性病变的患者中分离出MHC-I类分子阴性的黑色素瘤细胞,而这些肿瘤细胞通过遗传获得了B2M缺陷。
由于B2M是所有HLA I/抗原复合物的重要组成部分,所以B2M缺陷的细胞会形成不可逆的HLA I类阴性表型,逃逸T细胞攻击。
该现象在以往的黑色素瘤研究中也被报道过,这表明黑色素瘤对T细胞的完全抵抗是介导机体阻断PD-1免疫检查点的耐药机制之一。
最近的研究发现,黑色素瘤细胞阻断干扰素γ信号的突变,与机体对抗PD-1治疗的原发性耐药与继发性耐药相关。干扰素γ由通过TCR途径激活的T细胞释放,可以增强免疫疗法的疗效。
研究发现,黑色素瘤细胞上存在JAK1和JAK2基因的功能缺陷,而这两个基因是干扰素γ信号通路的组成部分。所以,该基因功能缺陷导致肿瘤细胞不再对干扰素γ的抗增殖和促凋亡的作用敏感。
有趣的是,非基因组机制似乎在机体对抗PD-1治疗的耐受中发挥了作用。研究表明,黑色素瘤细胞中的特定转录特征可以定义一种去分化的肿瘤表型,该表型会导致抗原呈递下调和T细胞浸润程度降低。这表明由于其表型的可塑性,黑色素瘤具有可逆的耐药状态。目前,关于更多与机体对抗PD-1治疗耐药性明确相关的其他机制和表型的试验仍在进行中。
19.11 前景
PD-1以及PD-1联合CTLA-4检查点阻断剂的批准使用是黑色素瘤治疗的一个里程碑,改变了黑色素瘤治疗的现状,并在晚期患者中成功获得了显著的临床效果。现在尚需后续大型临床试验的数据,以确定通过这些治疗,患者可以获得的总体的长期临床收益。
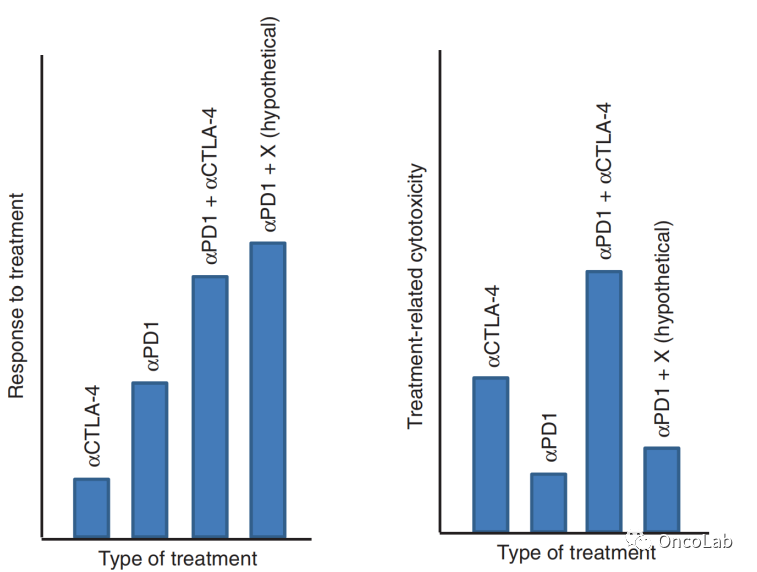
Fig. 19.3 与免疫检查点阻断相关的临床反应和细胞毒性。基于PD-1的治疗显示出最高的临床应答率。抗PD-1/抗CTLA-4联合治疗可显著增加治疗相关的细胞毒作用。在未来,PD-1检查点阻断与其他药物(X)的结合可能会在低细胞毒性的情况下实现高应答率。
预计有相当一部分患者将成为免疫疗法的长期受益者。但大多数患者仍然对PD-1和PD-1联合CTLA-4检查点阻断疗法具有原发性耐药。
此外,由于抗PD-1/CTLA-4联合治疗具有高毒副作用,所以仍需探索疗效高、毒副作用低的新联合疗法,目前研究人员正通过临床试验对新的联合疗法进行大量筛选(Fig. 19.3)。
其中,BRAF/MEK抑制剂与PD-1检查点阻断剂的联合运用取得了不错的试验结果。约50%患有BRAF(V600)突变的黑色素瘤患者接受BRAF和MEK抑制剂的联合治疗,患者对这些抑制剂的反应与包括CD8+T细胞在内的不同免疫细胞在病变部位的浸润程度相关。
这一结论为抑制剂治疗与免疫检查点阻断疗法相结合提供了理论基础。目前,研究BRAF/MEK抑制剂联合PD-1检查点阻断剂疗法的首批临床试验已经启动(https://ClinicaTrials.GOV;NCT02130466)。
除了PD-1和CTLA-4,被激活的肿瘤反应性CD8+T细胞还表达其他免疫检查点,包括LAG3、TIM3和TIGIT。
有趣的是,干扰素γ最近被证明可以促进黑色素瘤细胞上不同免疫检查点配体的表达。由于这些受体似乎在控制T细胞活性方面具有一定功能,所以目前研究人员希望通过临床试验证明它们与抗PD-1抗体联合治疗的可能性(https://ClinicaTrials.gov; NCT01968109: 抗PD-1联合抗LAG3抗体)。
还有一种联合治疗的方案是将抗PD-1治疗与瘤内注射溶瘤病毒(T-VEC)相结合,诱导专职抗原提呈细胞摄取抗原,进一步增强T细胞的激活。
除此之外,有关其他联合治疗方案的临床研究现状,可以在 https://ClinicaTrials.gov 上进行查看。一些试验可能很快就能得到初步结果,但仍需要更多时间来优化联合治疗的给药间隔和剂量。
总体来说,其中一些试验可能会对黑色素瘤的治疗产生影响,并为不同的患者亚群提供更好的治疗方案。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
本篇文章来源于微信公众号:OncoLab