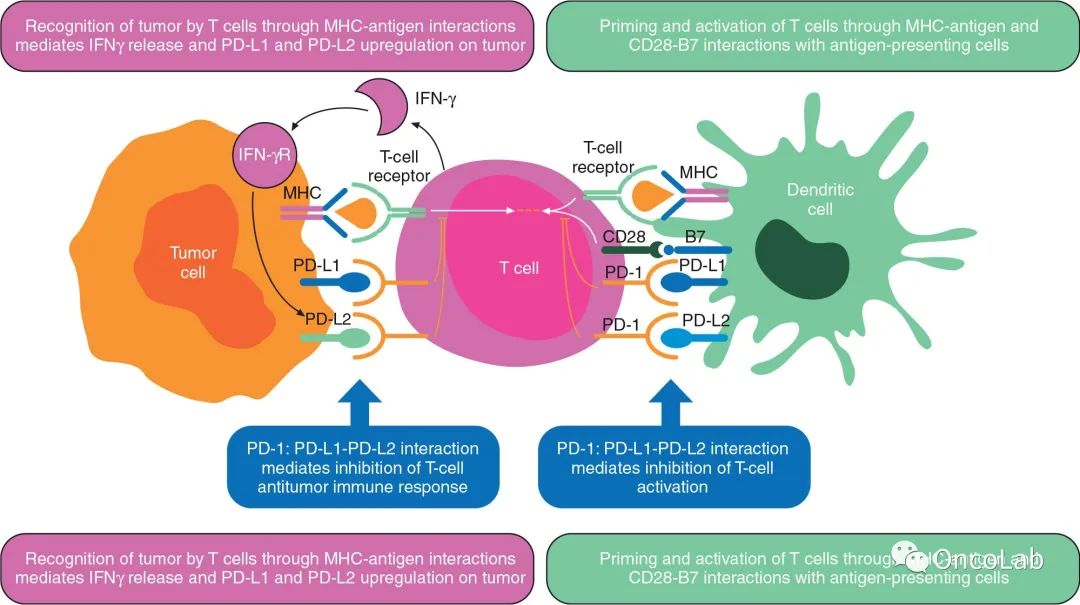
21.4 PD-L1作为预测生物标志物
由于对nivolumab的应答率约为25%,因此需要预测性生物标志物来确定哪些患者最有可能从治疗中受益。
在转移性黑色素瘤和鳞状细胞非小细胞肺癌中,PD-L1的表达与接受nivolumab或pembrolizumab治疗的患者的预后改善有关。
PD-L1生物标志物的研究已纳入肾癌临床试验。在接受nivolumab治疗的296例不同肿瘤患者的I期试验中,分析了42个肿瘤(5个肾癌)中PD-L1细胞表面的表达。免疫组织化学(IHC)染色阳性的细胞代表其PD-L1表达阳性。总体而言,这些样本中有60%的PD-L1表达阳性,这些阳性患者中有36%有客观反应。在PD-L1阴性患者中没有观察到客观反应。
在接受不同剂量nivolumab治疗的肾癌患者的随机II期试验中,使用IHC法测定PD-L1的表达。PD-L1表达阳性的截止点为5%的肿瘤细胞膜性染色。在107例(64%)肿瘤表达PD-L1的患者中,29例(27%)在5%的肿瘤细胞中表达PD-L1,78例(73%)在<5%的肿瘤细胞中表达PD-L1。PD-L1阳性患者和PD-L1阴性患者在PD-L1表达阈值为1%时的预后没有显著差异。
PD-L1的单独表达可能与接受抗PD-1治疗的患者的预后改善有关。在比较nivolumab和everolimus的III期试验中,nivolumab组的410名患者中有370名(90%)和411名evolimus患者中的386名(94%)有可量化的PD-L1表达。在PD-L1表达为1%的患者中,nivolumab组患者的mOS为21.8个月,everolimus组患者为18.8个月。然而,在PD-L1表达低于1%的患者中,nivolumab和everolimus组的中位OS分别为27.4个月和21.2个月。因此,PD-L1的高表达预示着转移性肾细胞癌患者预后较差,而不能作为预测疗效的生物标志物。
最近的两项回顾性分析研究了肾癌中PD-1表达的预后和预测作用。前一项研究显示PD-L1高表达对预后有负面影响,死亡风险增加53%(HR 1.53;95% CI 1.27-1.84;p值<0.001),而在转移性肿瘤中,原发灶PD-L1表达保留了其预后作用(HR1.45;95% CI 1.08-1.93;p值0.01)。第二项研究PD-L1表达的反应没有任何差异。
综上所述,没有证据表明PD-L1的表达可以作为接受nivolumab治疗的晚期肾癌患者的预测生物标记物。还需要使用替代抗体对PD-L1进行染色,以及对额外的细胞群(例如,浸润性免疫细胞)进行染色,以确定PD-1/PD-L1在肾癌中表达的预测价值。
21.5 PD-1在肾癌中的应用前景
由于单药nivolumab的研究取得了令人鼓舞的结果,研究PD-1阻断的试验越来越多。其他检查点抑制剂也正在积极研究中,包括pembrolizumab(抗PD-1)、atezolizumab和avelumab(两种抗PD-L1),以及PD-1/PD-L1抑制剂与其他免疫检查点抑制剂或TKI的联合策略。
与单独抑制PD-1/PD-L1通路相比,联合治疗有可能改善预后。考虑到多个免疫检查点调节的复杂性,所以支持结合免疫治疗策略以最大限度地提高临床效益是合理的。
事实上,PD-1和CTLA-4在调节获得性免疫时似乎扮演着截然不同的互补角色。CTLA-4在T细胞激活后早期上调,以抑制T细胞功能,而PD-1导致T细胞无能和衰竭。
临床前研究表明,PD-1和CTLA-4受体阻断剂联合应用可增加效应性T细胞的浸润,减少调节性T细胞的浸润,增加干扰素-ϒ的产生,从而产生更显著的抗肿瘤活性。
在I期试验中,对44例肾癌患者使用不同剂量(nivolumab 3 mg/kg+ipilimumab 1 mg/kg,每3周×4剂,nivolumab 1 mg/kg+ipilimumab 3 mg/kg,每3周×4剂,然后每2周连续服用nivolumab 3 mg/kg)的药物来评估nivolumab与抗CTLA-4的完全人源化IgG1抗体ipilimumab的联合应用。
18%的患者因治疗产生相关的不良反应,包括肺炎、腹泻、淀粉酶/脂肪酶和丙氨酸转氨酶升高而停止治疗。两个治疗组的ORR均为45%,且很高比例(80%)的患者有持续反应。这些令人鼓舞的结果引导了一项正在进行的III期试验,将这种联合疗法与sunitinib(舒尼替尼)作为mRCC的一线治疗进行比较。
血管内皮生长因子参与了髓系抑制细胞的发育和调控,而舒尼替尼通过减少髓系抑制细胞而逆转肿瘤诱导的免疫抑制。这种减少与效应器T细胞功能的改善和T细胞干扰素-γ的产生以及调节性T细胞数量的下降有关。
其他血管内皮生长因子抑制剂已经显示出通过诱导自噬和抑制肿瘤相关巨噬细胞的激活来增强免疫系统的能力,这与肾癌中的肿瘤微血管密度和血管内皮生长因子水平相关。
此外,血管内皮生长因子能够显著影响树突状细胞的功能成熟,树突状细胞是诱导初级免疫反应的最有效的APC。这些结果表明,抑制血管内皮生长因子不仅可以抑制血管生成,还可以提高抗原提呈的功能效力,从而有助于抗肿瘤细胞自身免疫的发展。
考虑到血管内皮生长因子的抑制和PD-1/PD-L1阻断相结合的临床前理论,一项I期试验研究了在转移性肾细胞癌患者中递增剂量的nivolumab(2 mg/kg剂量每3周增加到5 mg/kg)与sunitinib(每天50 mg,服用4周,停药2周;33名患者)或 pazopanib(每天800 mg,22名患者)的组合。
尽管pazopanib组的研究由于剂量限制的肝脏毒性而停止,但sunitinib联合组的剂量增加到比nivolumab更高的剂量,并将疗效扩大到未接受治疗的患者。
接受nivolumab和sunitinib治疗的患者中有82%观察到与治疗相关的3-4级不良反应,而接受nivolumab和pazopanib治疗的患者中有70%观察到与治疗相关的不良反应。总体而言,服用sunitinib的患者中有36%的患者和服用pazopanib的患者中有25%的患者因不良事件而停止治疗。
sunitinib组和pazopanib组的ORR分别为52%和45%。虽然毒性增加了,但本研究中观察到的应答率明显高于单一药物的应答率,特别是考虑到先前接受系统治疗的患者的离散数量。然而,由于毒性,这些组合没有得到进一步的推动。
此外,在Ib期研究中对atezolizumab和bevacizumab(一种直接抑制血管内皮生长因子的单抗)进行了研究(atezolizumab每3周20 mg/kg,bevacizumab每3周15 mg/kg)。10例肾癌患者经疗效评估,ORR为40%。40%的患者经历SD的时间大于或等于24周。联合用药耐受性良好,33%的患者(4/12)经历了3-4级的AEs。
在2017年泌尿生殖系癌症研讨会上提出了一项第二阶段的随机试验,即atezolizumab加bevacizumab与atezolizumab与sunitinib的比较(IMmotion 150试验)。这项试验招募了305名以前未接受治疗的肾癌患者,并随机分配到接受静脉注射atezolizumab加bevacizumab、单独接受atezolizumab或单独口服sunitinib,直到疾病进展或不可接受的毒性。
在肿瘤表达PD-L1的患者中,接受双重免疫治疗的患者的疾病进展或死亡风险比单用sunitinib的患者低36%(HR 0.64;95% CI,0.38-1.08;p值0.095);中位PFS分别为14.7个月和7.8个月。在总体人群中,与单用sunitinib相比,使用atezolizumab和bevacizumab并没有观察到PFS优势(HR,1.00;95% CI,0.69-1.45)。
正在进行的第三阶段IMMotion 151研究(ClinicalTrials.gov 标识:NCT02420821)正在招募参与者,在同一人群中对比atezolizumab联合bevacizumab与单独使用sunitinib的疗效。
其他血管内皮生长因子和PD-1/PD-L1抑制剂组合目前在几个正在进行的第三阶段临床试验中进行研究(Table 21.1)
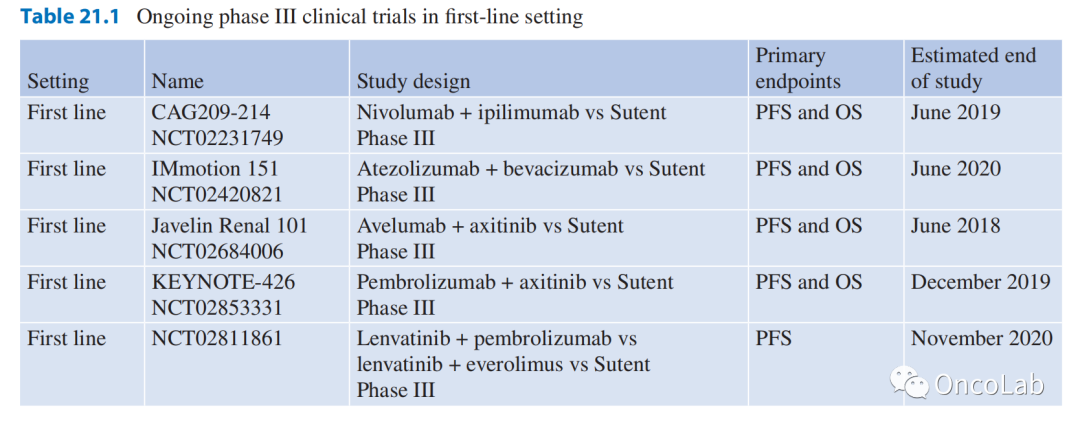
Table 21.1正在进行的第一线III期临床试验
Pembrolizumab是一种人源化的PD-1单抗,在包括肾癌在内的晚期实体肿瘤患者进行了I期试验,目前正在与血管内皮生长因子靶向药物联合进行研究。
Pembrolizumab与axitinib的联合应用是在2016年ESMO大会上公布的一项针对未接受治疗的晚期肾癌患者的Ib期研究。在ESMO上报道了52名晚期肾癌患者接受了axitinib联合Pembrolizumab的一线治疗。ORR为67.3%(35例),其中CR 2例,PR 33例。初步分析表明,联合用药耐受性好,对初治的肾癌患者有抗肿瘤活性。正在进行的这种联合治疗与sunitinib对照的第三阶段试验将试图证实这些令人鼓舞的结果。
此外,pembrolizumab和pazopanib的组合已经在一项正在进行的I/II期研究中进行了试验。初步报告了参加I期试验的20名患者的数据:联合用药引起了显著的肝毒性,65%的患者(20人中有13人)出现了3级或更高级的肝功能障碍(所有人都恢复到1级或更低)。总队列的ORR为40%(20人中有8人),pazopanib 800毫克组为60%,pazopanib 600毫克组为20%。pazopanib 800 mg组有1例完全缓解。目前正在探索新的给药方案,以pazopanib与pembrolizumab联合使用来降低肝毒性风险。
在一线晚期肾癌的Ib期试验中,对阿西替尼(Axitinib)与抗PD-L1阿维鲁单抗(avelumab)联合疗效进行了进一步的研究。在6名患者中观察到了确认的PR。
pembrolizumab和avelumab都被认为是有疗效的药物,未经治疗的晚期肾细胞癌患者 (NCT02853331和NCT02684006)的III期试验正在进行测试。
Cabozantinib是一种双重的血管内皮生长因子/MET抑制剂,最近在一项随机的III期试验中证明,在一线血管内皮生长因子靶向治疗进展后,除了改善mRCC患者的OS外,还可以改善ORR和PFS。
临床前证据表明,MET可以通过调节PD-L1促进肾癌细胞的存活。目前柯赞替尼(cabozantinib)联合尼伏卢单抗(nivolumab)或与ipilimumab联合使用治疗泌尿生殖系统肿瘤患者的临床试验目前纳入的患者数量正在增加(NCT02496208)。
Lenvatinib是血管内皮生长因子的多靶点TKI,具有抗FGFR、PDGFR、RET和KIT的活性。一项II期随机开放研究调查了150例肾细胞癌患者的二线治疗方案:lenvatinib(24 mg/d)、伊波利莫(everolimus)(10 mg/d)或联合用药(lenvatinib 18 mg/d和everolimus 5 mg/d)。
Lenvatinib与人源化PD-1单抗pembrolizumab联合使用的安全性和有效性目前正在Ib/II期研究(NCT02501096)中进行。
替伏扎尼(Tivozanib)是一种有效的、选择性的三种血管内皮生长因子受体抑制剂。在一项与nivolumab联合治疗肾癌的I/II期试验(称为TiNivo试验)中,正在评估在递增剂量下tivozanib与nivolumab的安全性,假设结果良好,试验之后将以既定的联合剂量进行扩大II期队列试验(EudraCT2016002310-44)。
在I期试验中,血管内皮生长因子抑制和PD-1/PD-L1阻断的活性汇总如表21.2所示。
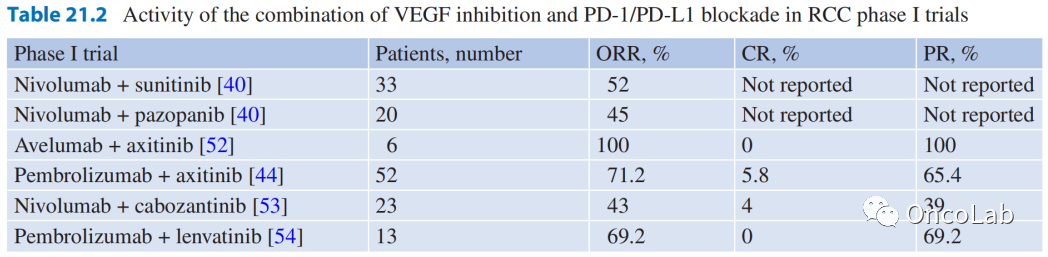
Table 21.2 血管内皮生长因子抑制和PD-1/PD-L1拮抗剂联合应用在肾癌I期试验中的活性
结论
PD-1阻断在晚期肾细胞癌中产生了令人鼓舞的应答率。特别是在CHECKMate 025试验中,与everolimus相比,nivolumab已达到了其在OS中的主要受益终点,成为一种新的治疗标准。抗PD-1/PD-L1与其他药物联合治疗肾癌的有效率高于单一药物,但毒性较高。
确定哪些患者将从这些治疗中获得临床益处仍然是一个重要的任务,也是一个正在积极研究的领域。IHC检测PD-L1表达已被广泛评估为一种预测生物标志物。许多悬而未决的问题使它的使用变得混乱:不同的抗体,确定阳性的可变IHC阈值,充分的组织准备和处理,原发灶和转移灶之间的不同表达,以及肿瘤和免疫细胞染色的评估。
免疫检查点抑制剂的有效性和毒性特征仍然存在,且有一系列悬而未决的问题。
首先,PD-1阻断在肾癌亚型中的作用是什么,例如非透明细胞肾癌患者?非透明细胞肾癌患者在很大程度上被排除在上述试验之外。最近,非透明细胞肾癌患者的PD-L1状态被证实与OS相关,提示阻断PD-1/PD-L1轴在该人群中可能显示出有益的。
第二,评估治疗反应的传统方法仍然可以预测检查点抑制剂的益处吗?在nivolumab的III期试验中,接受nivolumab治疗的患者与接受evolimus治疗的患者相比,在OS方面有显著的益处。这种对PFS的温和影响可能是假性进展的结果,假性进展可能是由于激活的免疫细胞对肿瘤的渗透而发生的,并可能导致假性进展。实体肿瘤的免疫相关反应评估标准(IRECIST)已经被提出来解决这一现象。
第三,继续免疫治疗的最佳持续时间也是未知的。一些试验在病情进展或表现出不耐受时停止了治疗。其他人则提出了一个预先定义的2年治疗停止点。虽然免疫治疗的反应模式与传统疗法不同,但一些患者在RECIST进展后也可能受益于nivolumab。
也许,对宿主免疫系统和肿瘤微环境的更好了解将更好地阐明哪些患者利用了这些有积极作用的药物。补充性PD-1途径阻断和靶向治疗或其他免疫学药物有可能减少肿瘤诱导的免疫抑制,改善转移性肾细胞癌患者的临床预后。鉴于目前PD-1/PD-L1抑制剂令人鼓舞的临床活性和安全性,联合应用很可能成为关键。
探索新的药物、组合以及反应的生物标记物的研究目前正在进行中,可能会为未来转移性肾细胞癌患者的治疗提供指导。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
作者 | Annette Paschen and Dirk Schadendorf
初稿翻译 | 陈晓意 郑梦怡 章震
编辑排版 | 吕思贤
审核修改 | 王坤 胡珊
(转载请保留此部分内容)
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab