本公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!
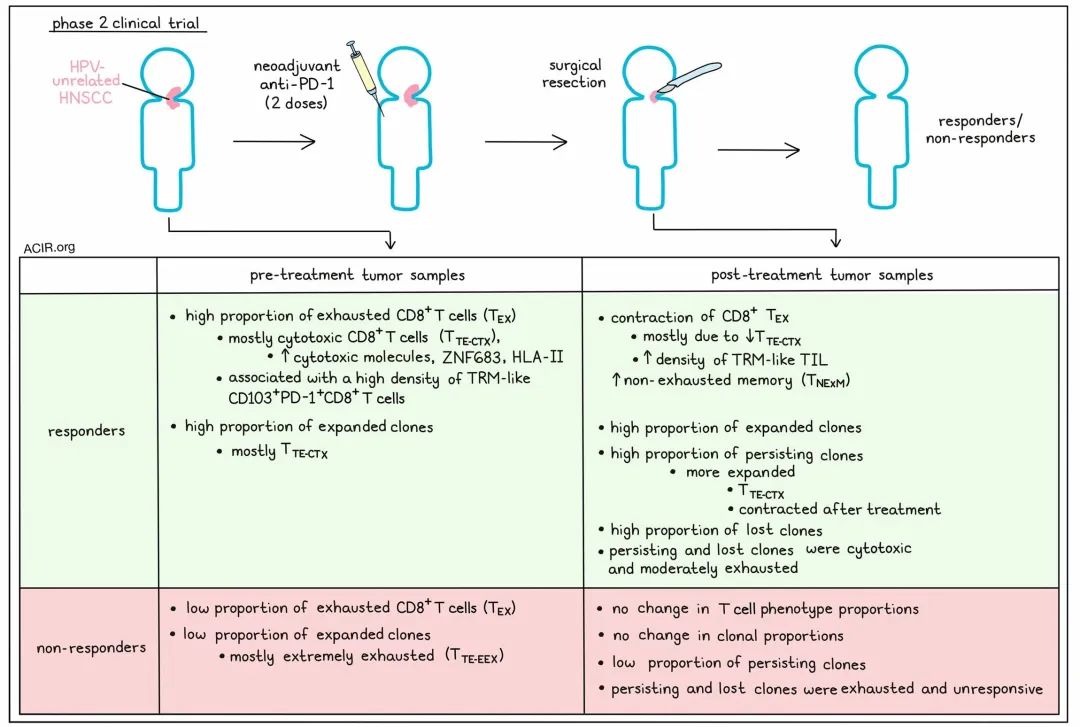
靶向PD-1的免疫检查点阻断(ICB)日益被用作新辅助疗法。然而,决定ICB反应的机制和细胞类型仍然知之甚少。Oliveira,Egloff,Afeyan等人比较了头颈鳞状细胞癌(HNSCC)患者在派姆单抗治疗下的T细胞激活状态和动态,并分别对应答者和非应答者进行了比较,最近他们在《Science Immunology》上发表了他们的数据。
这项研究的样本来自30位参加二期试验的HPV无关HNSCC患者,他们在手术前接受了两剂派姆单抗治疗。在15位患者(52%)中检测到病理性肿瘤反应。
为了确定肿瘤微环境(TME)中的T细胞动态如何与对派姆单抗的反应相关,研究人员对来自14个肿瘤活检样本的CD3+ TIL进行了单细胞RNA测序和TCR测序,这些样本在派姆单抗治疗前和/或后收集。分析了七位接受了两剂治疗和一位接受了一剂治疗的患者的样本;其中四位患者是应答者。来自6位患者(3位应答者和3位非应答者)的抗PD-1前后活检样本都可用。
有12个簇的CD8+ TIL,最丰富的终末耗竭(TTE)细胞亚群可以被细分为两个亚簇。一个亚簇被鉴定为极度耗竭(TTE-EEX),其差异表达的基因与耗竭和肿瘤抗原的识别相关。第二个亚簇具有细胞毒性特性(TTE-CTX)并且表现出较轻的耗竭程度。两个亚簇都高度表达组织驻留基因,但在转录因子方面存在差异。TTE-CTX最高表达细胞毒性分子(穿孔素、干扰素和颗粒酶)和ZNF683转录因子 – 这与组织驻留记忆(TRM)程序的维持有关。TTE-CTX还上调HLA-II基因,这与效应激活特征一致。
为了研究这些亚群如何与抗原识别相关,研究人员将TCR克隆与CD8+ TIL的表型联系起来。CD8+ TCR克隆家族大多数聚集在非耗竭记忆型(TNExM)或耗竭型(TEX)簇中。TNExM簇富含与病毒抗原特异性相关的标志,而TEX具有之前与肿瘤反应TIL相关的特征。这些可能的肿瘤反应性TIL类似于终末分化的TIL,并包括少量具有耗竭型祖细胞特征的TIL。
为了将T细胞动态与治疗反应相关联,研究人员比较了应答者和非应答者在治疗前后的TME。应答者在治疗前的样本中,CD8+ TEX TIL的频率更高,其中大部分是TTE-CTX。通过比较六名患者治疗前后的配对活检样本,研究者发现治疗开始后五周,三名应答者的CD8+ TEX细胞数量减少,TNExM细胞群体增加,而非应答者并未显示明显差异。应答者CD8+ TEX细胞数量的大部分减少是由于CD8+ TTE-CTX的减少。
在治疗前,应答者的CD8+ TEX TIL中具有细胞毒性潜能的比例更高,这与免疫荧光法检测到的治疗前样本中组织驻留记忆样(TRM-like) CD103+PD-1+CD8+ TIL的更高密度有关,而这种效应在反应更好的患者中更强。这些TRM-like TIL的密度在治疗后略有增加,但在应答者中仍然比在非应答者中高。
研究者使用独立的队列验证了数据。从参与先前单剂量派姆单抗试验的26名患者中获得的组织样本的RNA测序分析显示,应答者的CD8+浸润更多,且ZNF683和CTX基因(与TTE-CTX相关)的基线表达更丰富。另一份包含11名患者接受三剂纳武单抗治疗的肿瘤整体RNA测序数据的外部数据集也确认了ZNF683和CTX特征在治疗前的应答者中更丰富。这些数据表明,对ICB的反应依赖于预存在的高水平的耗竭/细胞毒性TIL。
研究者然后确定了治疗前后单个TCR克隆型的动态。在反应良好者中,大多数治疗前的CD8+ TEX TILs是高度扩增的克隆型,具有TTE-CTX表型,而反应不良者的扩增的CD8+ TEX TCR克隆型较少,主要是TTE-EEX。为了检查是否有预存在的TCR克隆型持续存在,或者有新的T细胞流入,TCR克隆型被分类为只在治疗前的样本中出现(丢失),只在治疗后的样本中出现(新的),或者在治疗前后的样本中都出现(持续存在)。治疗后有许多新的TCR克隆型,但大多数并未扩大,可能对治疗后的抗肿瘤反应在反应良好者和反应不良者的差异中的贡献很小。许多在基线检测到的克隆型在治疗后持续存在(占所有CD8+ TIL的60-70%),反应良好者的持续克隆型比例更大,且在治疗后更多地扩张。在反应良好者中,持续的并且扩张的CD8+ TEX克隆型在治疗后收缩;因此,反应良好者在治疗后丢失的克隆型比例更高,而反应不良者的TEX克隆比例没有变化。
在CD4+ T细胞群体中,检测到了TNExM、TEX、GZMK+ T和Tregs。TEX和TGZMK富含经过验证的肿瘤特异性TCR的特征。在反应良好者中,CD4+细胞群体中的耗竭细胞富集情况与CD8+细胞群体类似,而反应不良者的CD4+ TNExM频率更高。Tregs的比例在反应良好者和反应不良者中相似。
在所有丢失的、新的和持续的TNExM和TEX TCR克隆型中,假定的肿瘤反应性TEX TCR克隆型显示出最多的治疗诱导差异。在反应良好者中,持续或丢失的TCR克隆型的细胞表达最高水平的反应相关转录物,如细胞毒性基因,并且这些TIL也具有最高的细胞毒性评分和中等水平的耗竭。另一方面,反应不良者中持续存在的TEX克隆型高度富含与反应缺乏相关的转录物(耗竭基因),并且这些患者中扩大的克隆型具有最高的耗竭水平。在假定的肿瘤反应性CD8+ TEX克隆型中,耗竭水平在反应良好者和反应不良者中都没有减少,这些细胞也没有获得记忆表型。追踪与反应相关的克隆型显示,这些细胞在治疗前样本中约占CD8+ TEX的55%和所有CD8+ TIL的32%。高度扩张的克隆型表达ZNF683和CTX基因,而在反应不良者中,这一群体只占所有CD8+ TIL的大约4%。在反应良好者中,表达ZNF683和CTX基因的群体在治疗后最多地降低,这是通过这些克隆型的收缩实现的。反应不良者则主要是在极度耗竭状态的预存在TEX TCR克隆型,这在治疗后并未改变。
这些数据显示,对HNSCC中的抗PD-1治疗的反应可能是由在治疗前存在于HNSCC TME中的CD8+ TEX TIL引起的,这些细胞具有强烈的细胞毒性和驻留记忆特征。这个新发现与其他疾病的机制研究不同,后者识别出肿瘤内部耗竭程度较轻的细胞(克隆复活)和新的克隆型(克隆替换)的扩张。这项研究的结果可以帮助确定哪些患者可能最能从ICB治疗中受益,并提供一些关于为何一部分患者没有应答的线索。
作者面对面
本本周,共同第一作者Alex Afeyan回答了我们的问题。

共同第一作者Alex Afeyan
这项研究中最令你惊讶的发现是什么?
最令我惊讶的发现是,在我们分析的患者中,对免疫疗法的反应似乎由肿瘤浸润T细胞的状态预先决定。事实上,在我们研究的时间范围内,PD-1阻断反应的主要驱动因素似乎是恢复治疗前存在的肿瘤浸润CD8+ T细胞克隆的细胞毒活性。以前的研究强调了抗PD-1反应的两种机制,要么是招募新的抗肿瘤T细胞克隆到肿瘤(克隆替代),要么是使耗竭的T细胞克隆恢复到较少耗竭的祖先状态(克隆复活)。然而,在头颈癌中,我们看到应答者富含维持组织驻留、细胞毒性表型的预存在的T细胞克隆的扩增,并且经历了“细胞毒复活”,在应答治疗的患者中释放他们的抗肿瘤潜能。
前景如何?
通过比较应答者和非应答者的研究,我们确定了一个表达细胞毒潜能和组织驻留标记(ZNF683+ CTX+ TILs)的肿瘤浸润CD8+ T细胞群体,这个群体显著预测并似乎驱动了头颈鳞状细胞癌的反应。我们相信,我们对这个群体的单细胞转录组特征的分析在未来可以用来通过将患者按照对抗PD-1疗法的反应可能性进行分层来指导治疗。此外,我们对外部数据集的分析表明,细胞毒复活的机制可能也在其他肿瘤类型中活跃。需要进一步的研究来确定是什么肿瘤特性驱动了反应机制,以及为什么非应答者患者的肿瘤微环境无法支持ZNF683+ CTX+ TILs的扩增,而是更倾向于支持严重耗竭和功能失调的T细胞。
在工作之外,你最近学到的最酷的事情是什么?
作为一名波士顿体育迷,我在过去的几年里从一些小小的失落中学习到了坚韧和逆袭的力量,以及我们如何能够振作并支持我们心爱的队伍。我一直陪着各种球队赢得超级碗、世界系列赛、NBA总决赛和斯坦利杯。尽管过去几年我们在季后赛中经历了许多次失利,这让新英格兰地区以外的人感到欣喜,但我们的队伍总能重新振作起来,团结一心,坚持斗争,这给了我们地区的许多粉丝希望。让我们为凯尔特人、爱国者、熊和红袜队加油!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab