杂志名称:Nat Cancer.
发表日期:2024.01.10
DOI:10.1038/s43018-023-00691-z.
PubMed:https://pubmed.ncbi.nlm.nih.gov/38200243/
影响因子:22.7
内容简介
肿瘤中的免疫抑制性髓系细胞阻碍了免疫治疗的效果,但具体机制尚未明确。通过对结直肠癌组织进行单细胞RNA测序,我们发现与正常组织相比,肿瘤相关的巨噬细胞和粒细胞性髓系来源的抑制细胞数量增加最多,并且在所有免疫细胞中展示了最高的免疫抑制特征。这些细胞显著增加了包括SIRPA在内的含免疫受体酪氨酸抑制基序受体的表达。值得注意的是,Sirpa-/-小鼠比野生型小鼠对肿瘤进展更具抵抗力。此外,Sirpα缺失通过扩增显示强烈抗肿瘤活性的TAM_Ccl8hi和gMDSC_H2-Q10hi亚群重编程了肿瘤微环境。Sirpa-/-巨噬细胞展现出强烈的吞噬作用和抗原呈递能力,以增强T细胞的激活和增殖。此外,Sirpa-/-巨噬细胞通过Syk/Btk依赖的Ccl8分泌促进了T细胞的招募。因此,Sirpα缺失增强了先天和适应性免疫激活,独立于CD47的表达,而Sirpα阻断可能是提高癌症免疫治疗效果的有希望的策略。
创新性及研究意义
这篇文章的核心创新性在于揭示了肿瘤相关髓系细胞上的Sirpα在结直肠癌中抑制抗肿瘤免疫的新机制,这一过程独立于其与CD47的相互作用。研究通过单细胞RNA测序技术,发现与正常组织相比,结直肠癌组织中的肿瘤相关巨噬细胞和粒细胞性髓系来源抑制细胞显著增多,表现出强烈的免疫抑制特征,并具有高表达含免疫受体酪氨酸抑制基序的受体,包括SIRPA。
该研究进一步证明了Sirpa基因敲除(Sirpa-/-)小鼠相比于野生型小鼠对肿瘤进展更具抵抗力。重要的是,Sirpα缺失不仅重新编程了肿瘤微环境,通过扩增具有强烈抗肿瘤活性的细胞亚群,还增强了巨噬细胞的吞噬作用和抗原呈递能力,进而增强T细胞的激活和增殖。此外,Sirpα缺失巨噬细胞还能通过特定的分泌途径促进T细胞的招募,从而增强了先天和适应性免疫反应。
研究意义在于,这些发现为结直肠癌的免疫治疗提供了新的靶点,即通过阻断Sirpα来增强抗肿瘤免疫反应,为癌症治疗提供了潜在的新策略。这一发现不仅有助于深化我们对肿瘤免疫环境的理解,也为开发新的免疫治疗方法提供了科学依据。
数据图
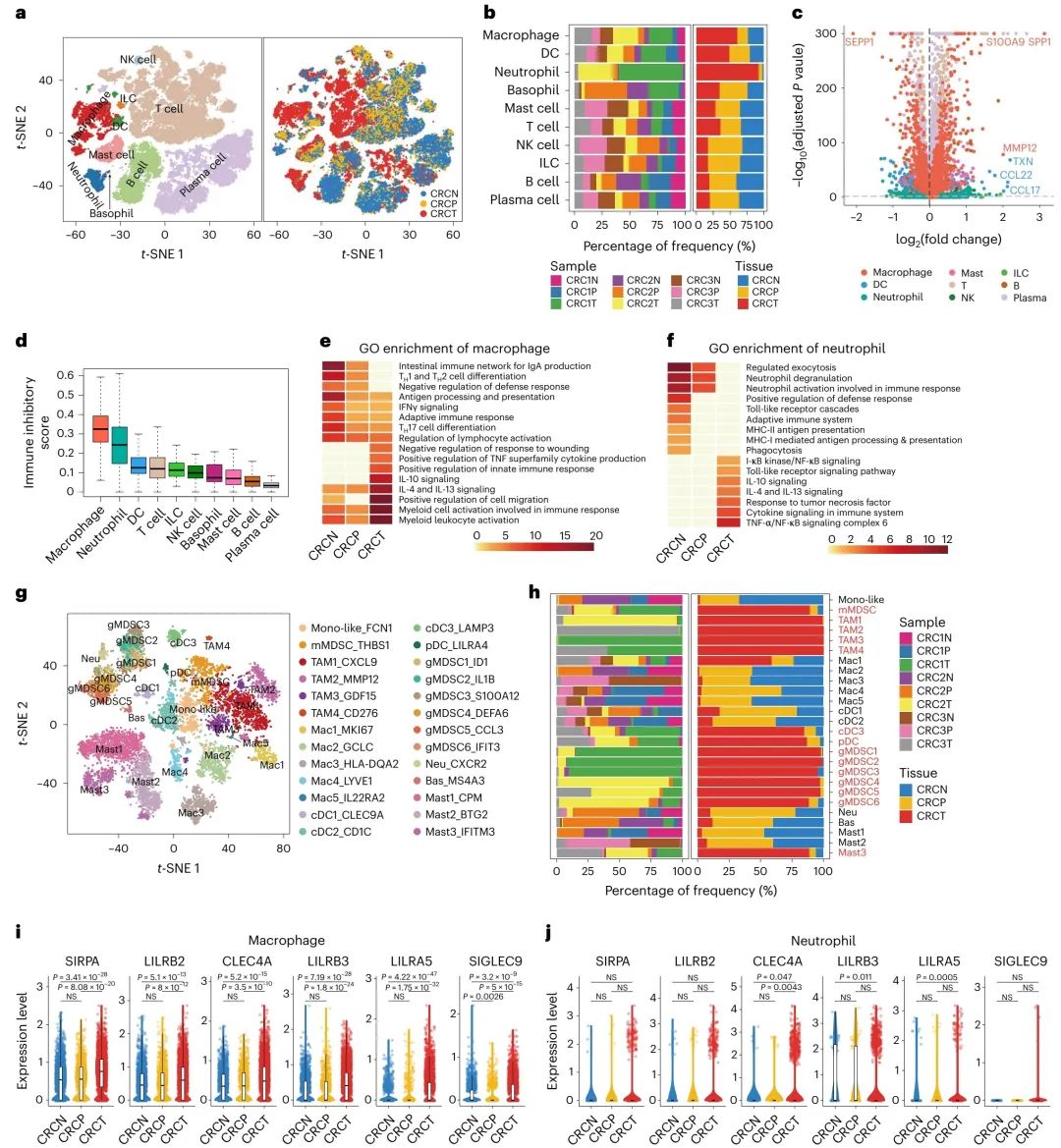
图 1 | 肿瘤中富集的髓系细胞展现出最高的免疫抑制特征。
a,来自三位结直肠癌(CRC)患者的62,288个免疫细胞的t-SNE投影,根据细胞类型(左侧)和组织类型(右侧)进行着色。
b,每种细胞类型中各个样本和组织的百分比。CRC1、CRC2和CRC3代表三位结直肠癌患者。
c,肿瘤组织与正常/癌旁组织间每种细胞类型的差异表达基因的火山图(Wilcoxon检验,双侧)。采用Bonferroni方法进行多重比较校正。
d,肿瘤浸润免疫细胞(TIICs)中每种细胞类型的免疫抑制评分。
e,f,巨噬细胞(e)和中性粒细胞(f)在CRCN、CRCP和CRCT组织中显著富集的特征。颜色深度代表-log10(q值)。TH细胞,辅助性T细胞。
g,来自三位结直肠癌患者的10,245个髓系细胞的t-SNE可视化,根据推断的细胞亚群进行着色。
h,每个髓系细胞亚群中各个样本和组织的比例。
i,j,不同组织中巨噬细胞(i)和中性粒细胞(j)中免疫抑制基因的表达(Wilcoxon检验,双侧)。箱线图中标记了最小值、最大值、中心、边界以及百分位数。
NS,不显著。CRCT,结直肠癌患者的肿瘤组织;CRCN,结直肠癌患者的正常组织;CRCP,结直肠癌患者的癌旁组织。
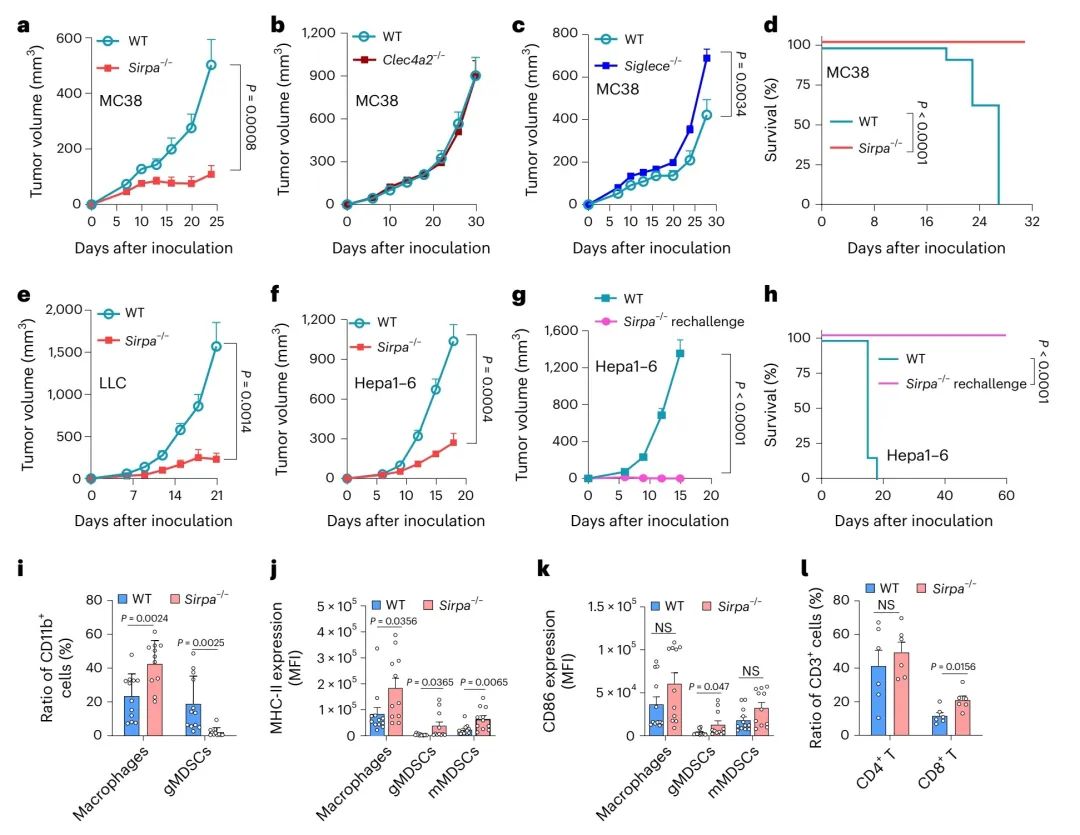
图 2 | Sirpα基因的缺失抑制实体肿瘤的发展。
a,野生型小鼠(WT,n = 12只)和Sirpa−/−小鼠(n = 11只)体内皮下MC38肿瘤的生长情况。
b,野生型小鼠(WT,n = 6只)和Clec4a2−/−小鼠(n = 6只)体内皮下MC38肿瘤的生长情况。
c,野生型小鼠(WT,n = 6只)和Siglece−/−小鼠(n = 13只)体内皮下MC38肿瘤的生长情况。
d,携带皮下MC38肿瘤的野生型小鼠(WT,n = 14只)和Sirpa−/−小鼠(n = 9只)的生存分析。
e,野生型小鼠(WT,n = 6只)和Sirpa−/−小鼠(n = 6只)体内皮下Lewis肺癌(LLC)肿瘤的生长情况。
f,野生型小鼠(WT,n = 9只)和Sirpa−/−小鼠(n = 6只)体内皮下Hepa1-6肿瘤的生长情况。
g,h,在消除初次接种的Hepa1-6肿瘤45天后,再次接种三倍Hepa1-6细胞的野生型小鼠(WT,n = 6只)或无肿瘤的Sirpa−/−小鼠(n = 17只)的肿瘤生长(g)和生存分析(h)。
i,在野生型小鼠(WT,n = 12个样本)或Sirpa−/−小鼠(n = 11个样本)体内皮下MC38肿瘤中,巨噬细胞和gMDSCs的百分比。
j,k,通过流式细胞术计算得出野生型小鼠(WT,n = 12个样本)和Sirpa−/−小鼠(n = 11个样本)体内皮下MC38肿瘤中的巨噬细胞、gMDSCs和mMDSCs中的MHC-II表达(j)或CD86表达(k)。
l,通过流式细胞术计算得出,野生型小鼠(WT,n = 6个样本)和Sirpa−/−小鼠(n = 6个样本)体内皮下MC38肿瘤中CD4+ T细胞和CD8+ T细胞的百分比。所有样本均来自独立的小鼠。结果(a,d,i–l)汇总自两个独立实验。结果(b,c,g,h)代表两个独立实验之一。结果(e,f)代表五个独立实验之一。误差条表示均值 ± 标准误差。采用未配对的学生t检验(双尾)(a–c,e–g,i–l)和对数秩检验(d,h)进行统计分析。
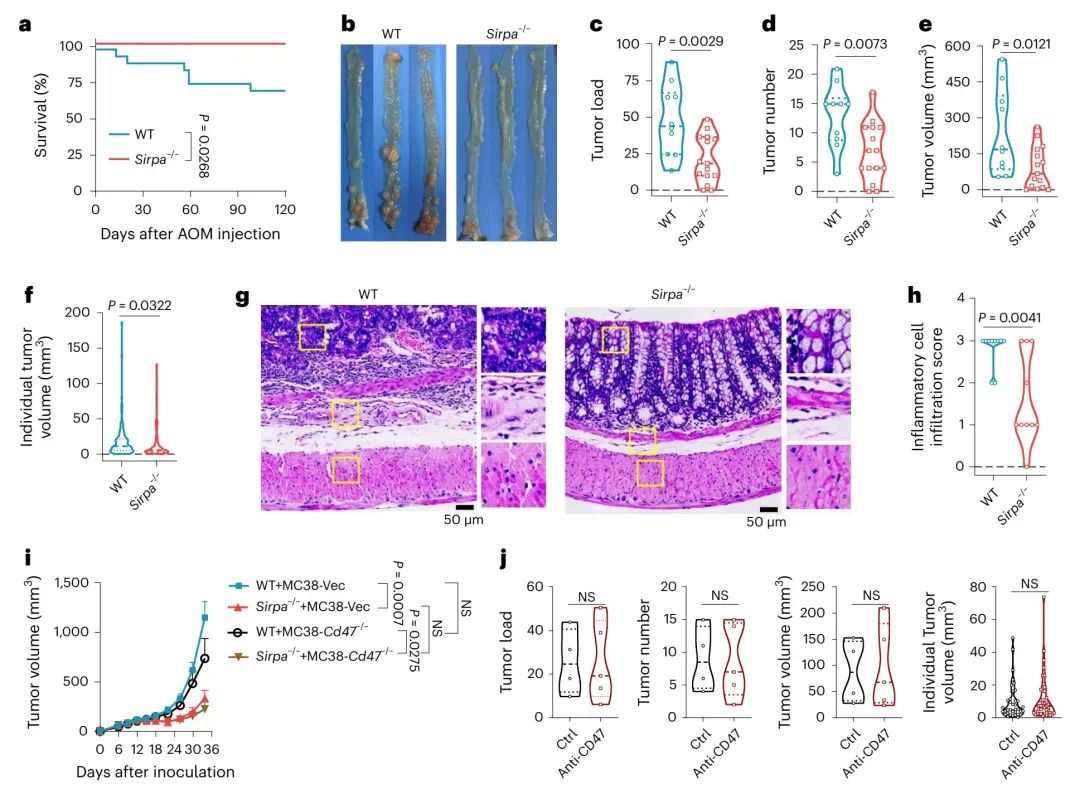
图 3 | Sirpα缺失阻止自发性结肠癌的发展。
a,AOM/DSS诱导的自发性结直肠癌(CRC)模型中,野生型小鼠(WT,n = 21只)和Sirpa−/−小鼠(n = 15只)的生存分析。
b,AOM/DSS诱导的CRC中大肠肿瘤的代表性图片。
c-f,在AOM/DSS诱导的CRC模型中,测量野生型小鼠(n = 10只)和Sirpa−/−小鼠(n = 15只)的肿瘤负荷(c),肿瘤数量(d),总肿瘤体积(e)和单个肿瘤体积(f)。
g,用苏木精-伊红(H&E)染色对野生型小鼠(有肿瘤)和Sirpa−/−小鼠(无肿瘤)的结肠组织进行的组织学分析的代表性图片。比例尺,50微米。
h,在AOM/DSS诱导的CRC模型中,野生型小鼠(n = 10只)和Sirpa−/−小鼠(n = 10只)的结肠组织中炎症细胞浸润的评分。
i,在WT小鼠和Sirpa−/−小鼠体内接种MC38-vector或MC38-Cd47−/−细胞后,皮下肿瘤的生长情况。WT + MC38-vector(n = 6只),Sirpa−/− + MC38-vector(n = 7只),WT + MC38-Cd47−/−(n = 6只),Sirpa−/− + MC38-Cd47−/−(n = 7只)。
j,使用CD47抗体治疗(anti-CD47,n = 5只)和不治疗(对照组;n = 4只)的AOM/DSS诱导的CRC中的肿瘤负荷、肿瘤数量、肿瘤体积和单个肿瘤体积。
结果(a,b,g,h)代表三个独立实验之一。结果(c-f)汇总自两个独立实验。结果(i)代表四个独立实验之一,结果(j)来自一个独立实验。数据表示为均值 ± 标准误差。使用对数秩检验(a)和未配对的学生t检验(双尾)(c-f,h-j)进行统计分析。
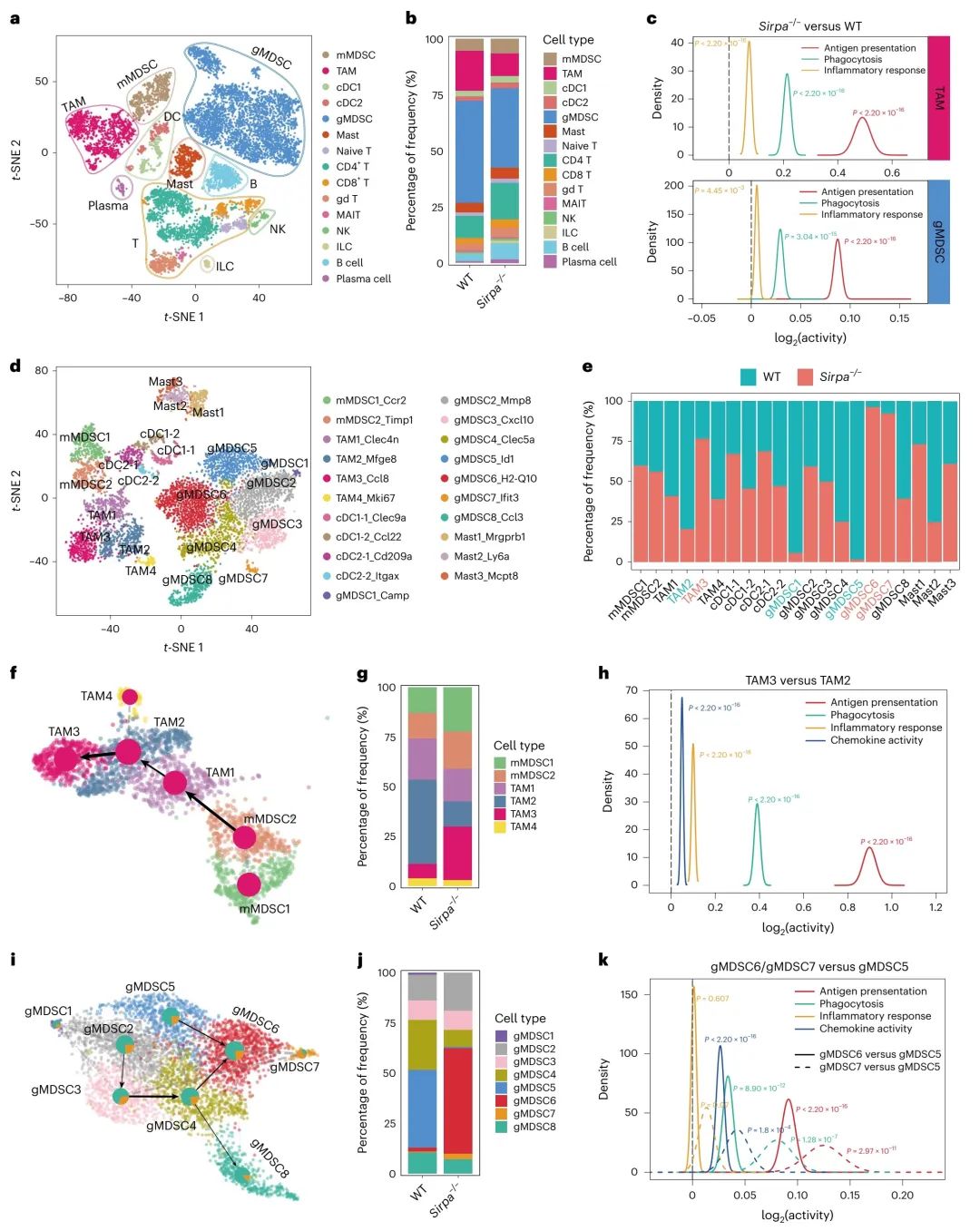
图 4 | Sirpα缺失重新编程肿瘤免疫微环境以促进抗肿瘤免疫。
a,采用t-SNE可视化方法展示了来自两只野生型小鼠和两只Sirpa−/−小鼠的AOM/DSS诱导的CRC中11,516个肿瘤浸润免疫细胞(TIICs),按细胞类型进行着色。
b,野生型小鼠和Sirpa−/−小鼠中各细胞类型的百分比。
c,使用QuSAGE比较Sirpa−/−小鼠与野生型小鼠中巨噬细胞(TAMs,上图)和肉芽肿性髓细胞(gMDSCs,下图)的抗原呈递评分、吞噬评分和炎症反应评分。x轴代表基因集评分的log2(倍数变化)。
d,采用t-SNE可视化方法展示了来自野生型小鼠和Sirpa−/−小鼠的7,842个肿瘤浸润的髓系细胞,按细胞亚群进行着色。
e,野生型小鼠和Sirpa−/−小鼠中每个髓系细胞亚群的细胞比例。
f,通过scVelo和CellRank推断的巨噬细胞谱系的发展轨迹。每个簇的饼图显示细胞群体分化为特定终端谱系的概率,箭头指示轨迹方向。
g,对应于推断谱系的野生型小鼠和Sirpa−/−小鼠中巨噬细胞亚群的百分比。
h,使用QuSAGE比较TAM3和TAM2的抗原呈递评分、吞噬评分、炎症反应评分和趋化因子活性评分。
i,通过scVelo和CellRank推断的肉芽肿性髓细胞(gMDSC)谱系的发展轨迹。识别出两个谱系。图例注释与f相同。
j,野生型小鼠和Sirpa−/−小鼠中gMDSC亚群的百分比。
k,使用QuSAGE比较gMDSC6/gMDSC7与gMDSC5的抗原呈递评分、吞噬评分、炎症反应评分和趋化因子活性评分。P值是使用QuSAGE从概率密度函数中提取的(c,h)。
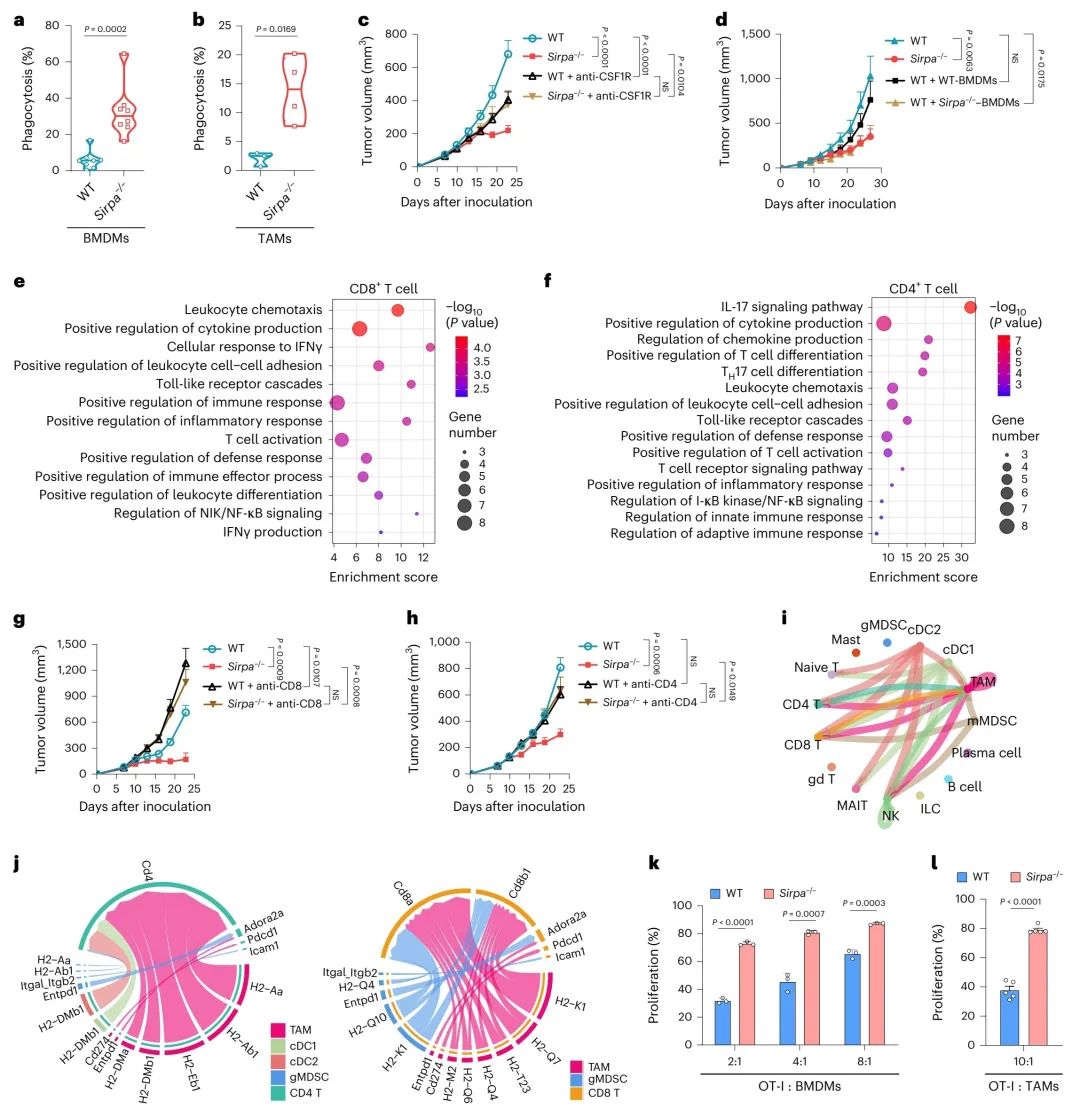
图 5 | Sirpα缺失增强了巨噬细胞功能和T细胞激活。
a,b,多糖(I:C)激活的野生型(WT,n = 8个样本)和Sirpa−/−(n = 8个样本)骨髓来源的巨噬细胞(BMDMs)(a)或肿瘤相关巨噬细胞(TAMs)WT(n = 3个样本)和Sirpa−/−(n = 4个样本)(b)对MC38细胞的吞噬作用。
c,在WT(n = 17只)、Sirpa−/−(n = 14只)、WT + 抗CSF1R(n = 13只)和Sirpa−/− + 抗CSF1R组(n = 13只)小鼠体内,皮下MC38肿瘤的生长情况。
d,在WT(n = 5只)、Sirpa−/−(n = 8只)、WT + WT BMDMs(n = 6只)和WT + Sirpa−/− BMDM组(n = 6只)小鼠体内,皮下MC38肿瘤的生长情况。
e,f,在Sirpa−/−小鼠相比于WT小鼠中,肿瘤浸润的CD8+ T细胞(e)和CD4+ T细胞(f)中显著富集的特征(Wilcoxon检验,双侧)。
g,在WT(n = 6只)、Sirpa−/−(n = 5只)、WT + 抗CD8(n = 5只)和Sirpa−/− + 抗CD8组(n = 6只)小鼠体内,皮下MC38肿瘤的生长情况。
h,在WT(n = 11只)、Sirpa−/−(n = 5只)、WT + 抗CD4(n = 6只)和Sirpa−/− + 抗CD4组(n = 5只)小鼠体内,皮下MC38肿瘤的生长情况。
i,通过CellChat计算的任意两种细胞类型间通过细胞-细胞接触信号传递的前10%显著配体-受体对(L-R对)。
j,在Sirpa−/−小鼠中,来自mMDSCs、TAMs、cDCs和gMDSCs到CD4+ T细胞(左侧)或CD8+ T细胞(右侧)的细胞-细胞接触信号传递的上调L-R对。
k,由WT BMDMs(n = 3个样本)或Sirpa−/− BMDMs(n = 3个样本)预处理OVA肽后引发的OT-I T细胞增殖,以不同比例进行。
l,由WT TAMs(n = 5个样本)或Sirpa−/− TAMs(n = 5个样本)预处理OVA肽后引发的OT-I T细胞增殖,以10:1的比例进行。
所有样本均来自独立小鼠。数据表示为均值 ± 标准误差,汇总自八个独立实验(a)和两个独立实验(b,c),或代表三个独立实验之一(d,g),两个独立实验之一(h,k),以及一个独立实验(l)。使用未配对的学生t检验(双尾)计算P值(a–d,g,h,k,l)。
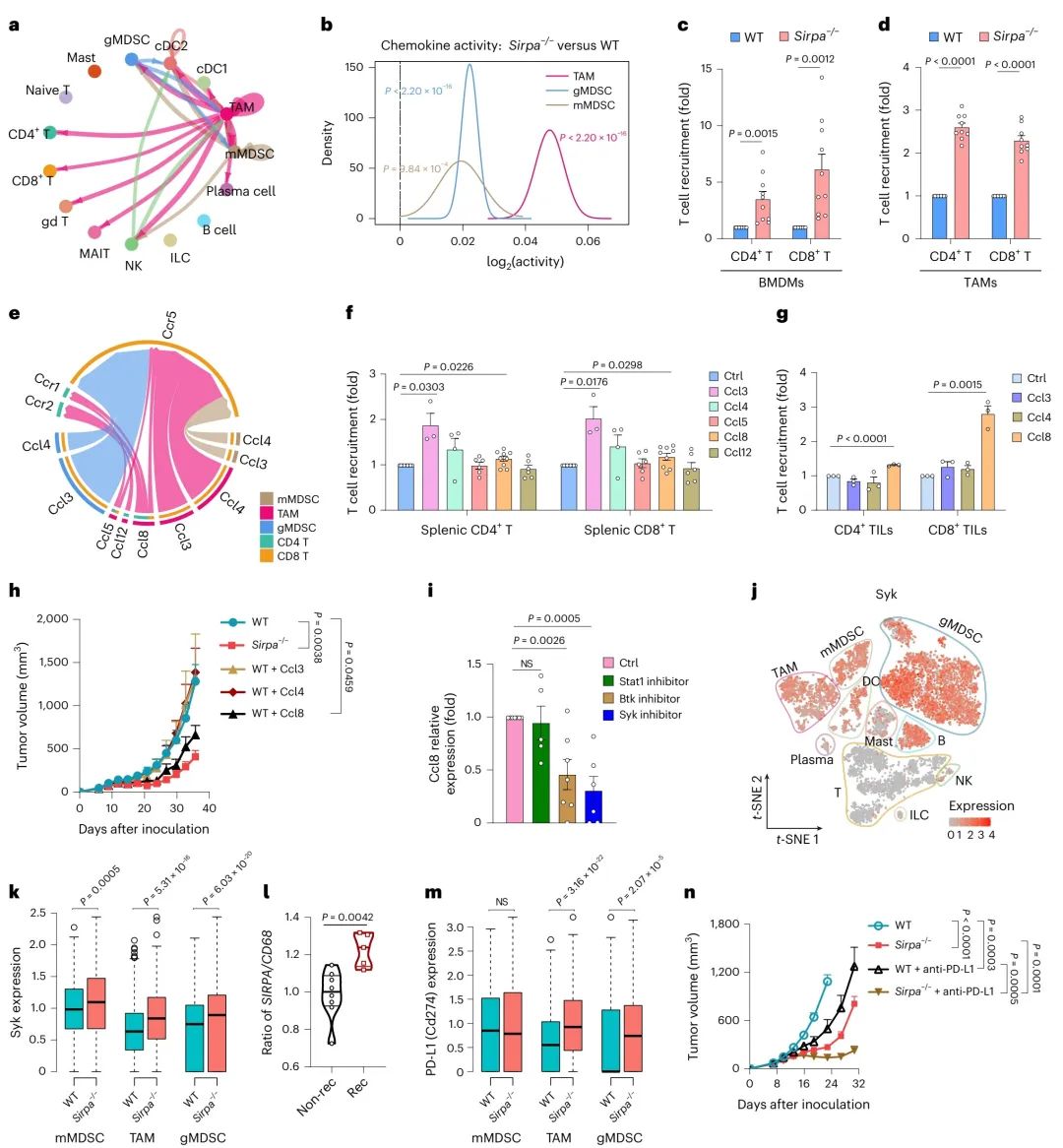
图 6 | Sirpα缺失的巨噬细胞通过依赖Syk/Btk的Ccl8分泌增强T细胞招募。
a,细胞类型对之间分泌信号传递的前10%显著配体-受体对(L–R对)。
b,使用QuSAGE比较野生型小鼠和Sirpa−/−小鼠中mMDSC、TAM和gMDSC的趋化因子活性评分。
c,d,在骨髓来源巨噬细胞(BMDMs)WT(n = 10个样本)和Sirpa−/−(n = 10个样本)(c)或TAMs WT(n = 9个样本)和Sirpa−/−(n = 9个样本)(d)作用下,CD8+ T细胞或CD4+ T细胞的倍增变化。
e,在Sirpa−/−小鼠中,来自mMDSC、TAM和gMDSC到CD4/CD8 T细胞的上调分泌信号传递的L–R对。
f,Ccl3(n = 3个样本)、Ccl4(n = 4个样本)、Ccl5(n = 6个样本)、Ccl8(n = 9个样本)或Ccl12(n = 6个样本)招募的脾脏CD4+或CD8+ T细胞的倍增变化。
g,Ccl3、Ccl4或Ccl8(n = 3个样本)招募的CD4+或CD8+肿瘤浸润淋巴细胞(TILs)的倍增变化。
h,在WT(n = 9只)、Sirpa−/−小鼠(n = 6只)和给予Ccl3(n = 5只)、Ccl4(n = 6只)或Ccl8(n = 5只)的WT小鼠体内,皮下MC38肿瘤的生长情况。
i,使用反转录qPCR测试Sirpa−/− BMDMs在无抑制剂(对照)或加入Stat1(n = 5个样本)、Btk(n = 7个样本)或Syk(n = 6个样本)抑制剂情况下的Ccl8表达。
j,WT小鼠中Syk表达水平的t-SNE可视化。
k,在AOM/DSS诱导的CRC中,WT和Sirpa−/−小鼠的mMDSCs、TAMs和gMDSCs中Syk的表达水平(Wilcoxon检验,双侧)。
l,在接受新辅助抗PD-1治疗的黑色素瘤患者中,SIRPA/CD68的比率。非复发(n = 8名患者)和复发(n = 5名患者)。rec,复发。
m,在AOM/DSS诱导的CRC中,WT和Sirpa−/−小鼠的mMDSCs、TAMs和gMDSCs中PD-L1(Cd274)的表达水平(Wilcoxon检验,双侧)。
n,在WT(n = 15只)、Sirpa−/−(n = 8只)、WT + 抗PD-L1(n = 12只)和Sirpa−/− + 抗PD-L1组(n = 11只)小鼠体内,皮下MC38肿瘤的生长情况。
所有样本均来自独立小鼠。数据(均值 ± 标准误差)来自四个独立实验(c)、六个独立实验(f)、七个独立实验(i)、两个独立实验(d、n)、1个独立实验(h)和1个独立实验(g)。P值采用双尾Student ‘s t检验(c,d,f – i,n)计算。
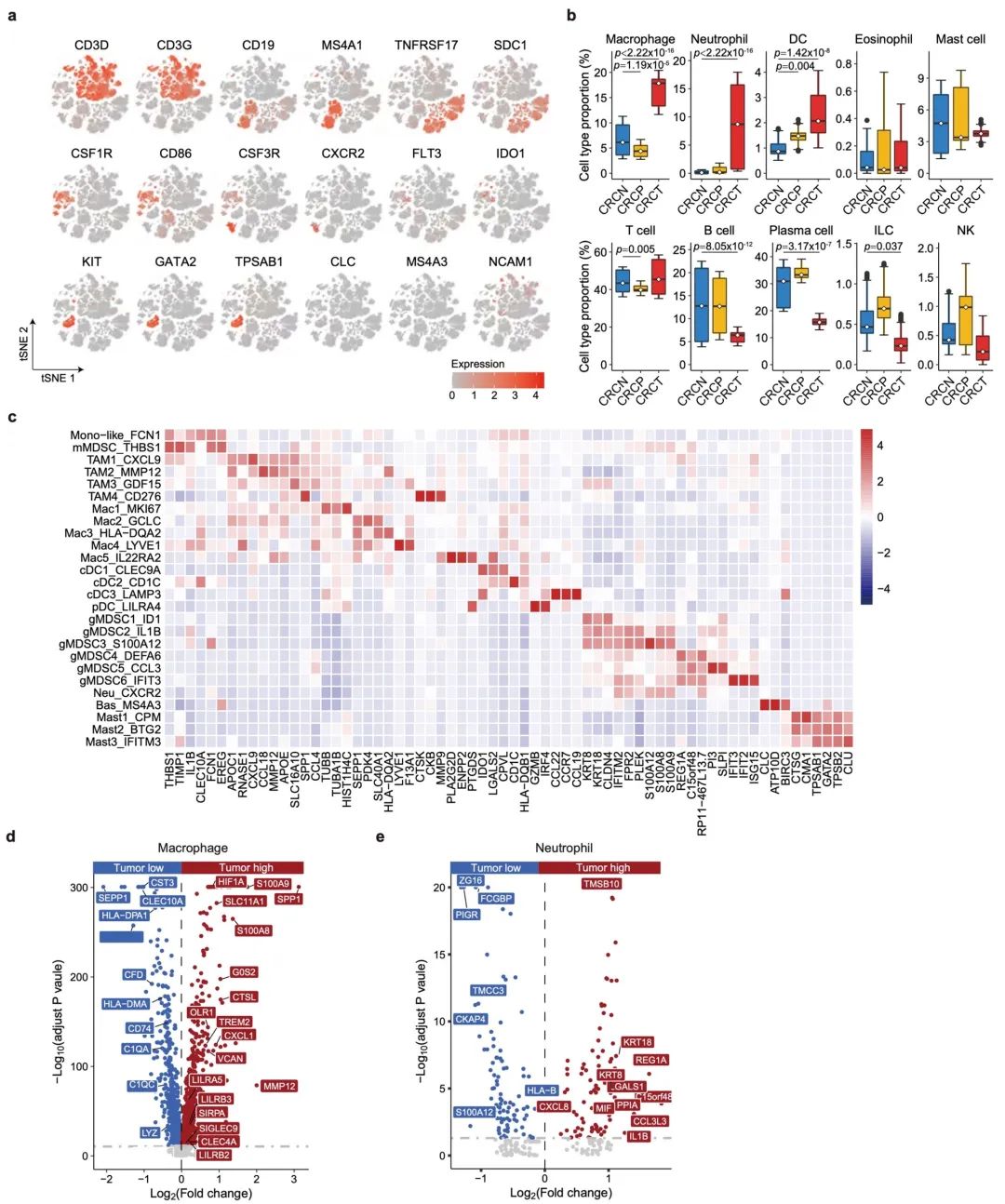
扩展数据 图 1 | 结直肠癌患者肿瘤组织中的髓系细胞展现出促进肿瘤的特征。
a. 通过表达水平着色的细胞类型特异性基因的t-SNE可视化。
b. 通过scDC计算得出CRCN、CRCP和CRCT组织中每种细胞类型的比例。通过scDC中的GLM模型进行自助重采样来计算p值。
c. 每个髓系细胞簇中前3个差异表达基因的热图。颜色代表每个簇中基因平均表达的标准化值。
d, e. 宏观观测巨噬细胞(d)和中性粒细胞(e)在肿瘤组织与正常/癌旁组织之间差异表达基因的火山图(Wilcoxon检验,双侧)。红点和蓝点分别代表在肿瘤组织和正常/癌旁组织中高表达的基因。使用Bonferroni方法对多重比较进行校正。
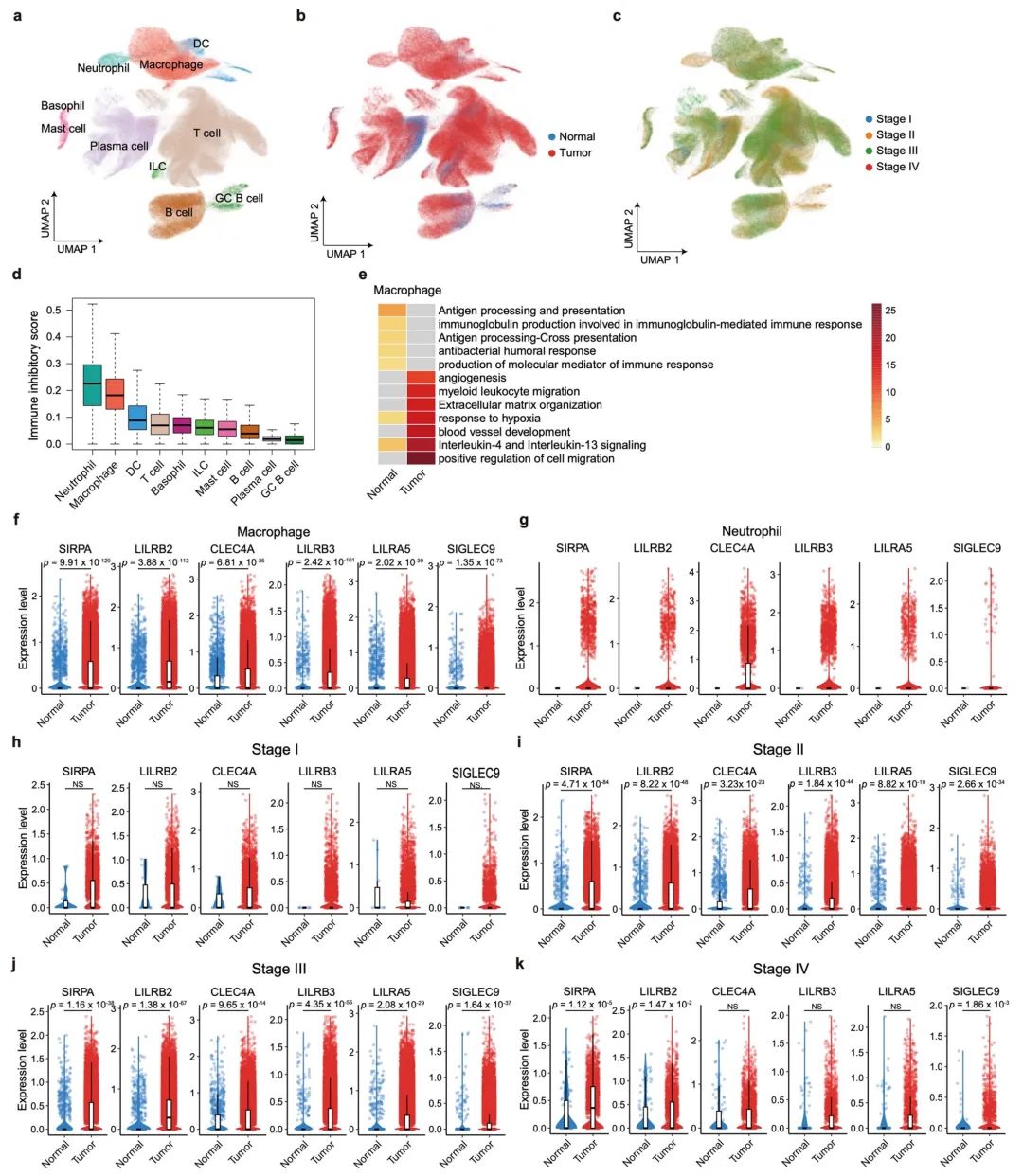
扩展数据图 2 | 在大数据中,肿瘤浸润的髓系细胞展示出最高的免疫抑制特征。
a–c. 从syn26844071、GSE188711和GSE178341中,131位结直肠癌(CRC)患者的455,959个免疫细胞的UMAP投影,按细胞类型(a)、组织(b)和TNM分期(c)着色。
d. 肿瘤组织中每种细胞类型的免疫抑制评分。
e. 肿瘤相关巨噬细胞(TAM)特异基因显著富集的特征。颜色深度代表-Log10 (p值)。
f-k. 来自所有131位CRC患者的巨噬细胞(f)和中性粒细胞(g),以及I期(h)、II期(i)、III期(j)和IV期(k)巨噬细胞在肿瘤和正常组织中的免疫抑制基因表达(Wilcoxon检验,双侧)。
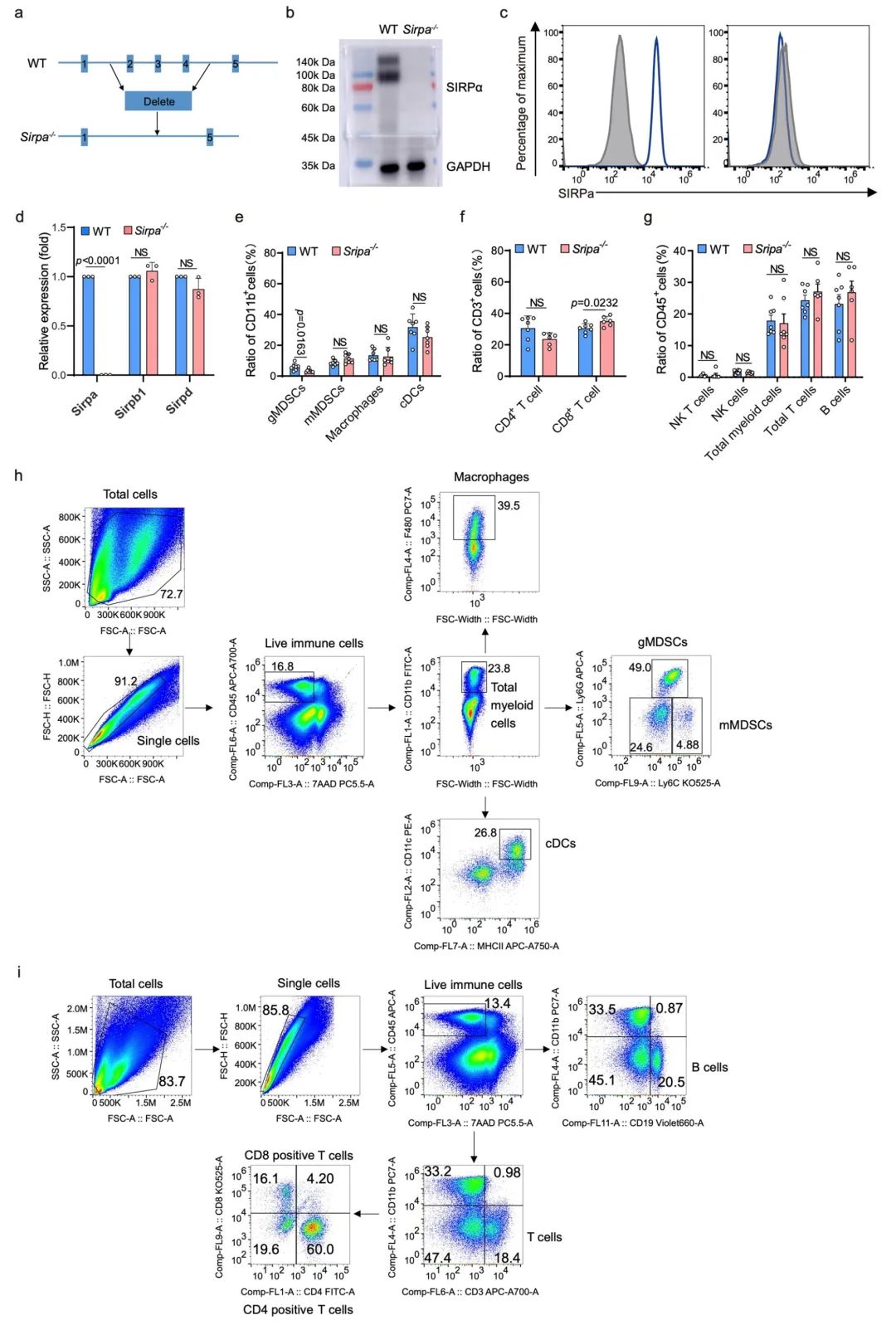
扩展数据图 3 | Sirpα基因敲除小鼠的基本信息及其基线免疫特征。
a. Sirpa−/−小鼠的生成方案。
b, c. 通过免疫印迹(Western blot)(b)和流式细胞术(FACS)(c)检测野生型(WT)和Sirpa−/−小鼠骨髓来源巨噬细胞(BMDMs)中的Sirpα蛋白。
d. 通过RT-qPCR测量WT BMDMs(n = 3个样本)和Sirpa−/− BMDMs(n = 3个样本)中Sirpa、Sirpb1和Sirpd的表达水平。
e. 比较WT小鼠(n = 7个样本)和Sirpa−/−小鼠(n = 7个样本)肠道中的髓系细胞亚群。
f. 比较WT小鼠(n = 7个样本)和Sirpa−/−小鼠(n = 6个样本)肠道中的T细胞亚群。
g. 比较WT小鼠(n = 7个样本)和Sirpa−/−小鼠(n = 7或6个样本)中所有肠道免疫细胞中NKT细胞、NK细胞、总髓系细胞、总T细胞和B细胞的比例。
h-i. 髓系细胞(h)或淋巴细胞(i)的门控策略。
所有样本均来源于独立的小鼠。结果(b, c)代表三个独立实验中的一个。结果(d-g)来自一个独立实验。误差条表示均值 ± 标准误差。对d-g使用了未配对的学生t检验。
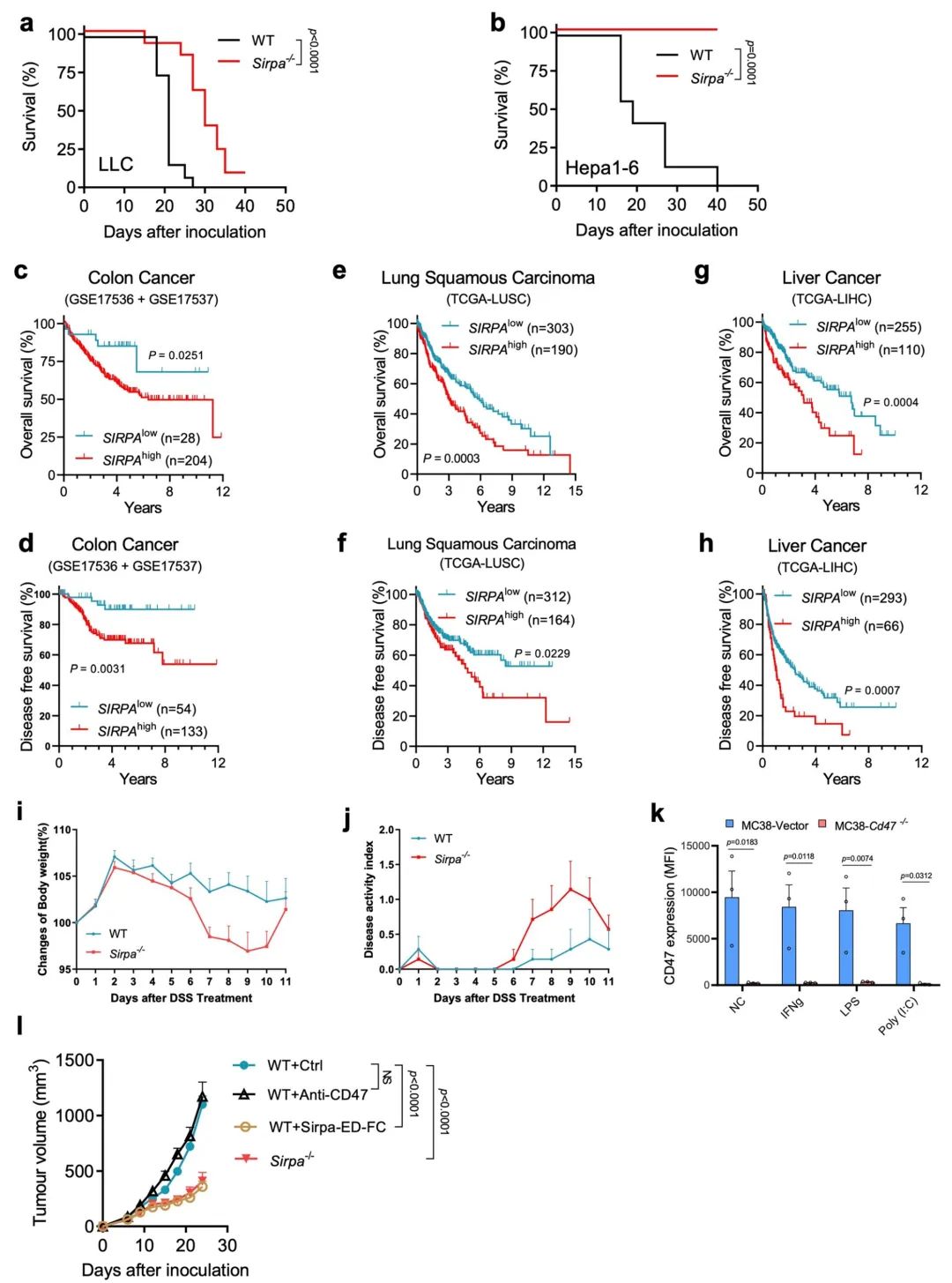
扩展数据图 4 | Sirpα缺失抑制肿瘤生长,且Sirpα与患者预后不良相关。
a. 携带皮下LLC肿瘤的WT小鼠(n = 12只)和Sirpa−/−小鼠(n = 13只)的生存分析。
b. 携带皮下Hepa1-6肿瘤的WT小鼠(n = 7只)和Sirpa−/−小鼠(n = 7只)的生存分析。
c, e, g. 结肠癌(GSE17536和GSE17537,n = 232)(c)、肺鳞状细胞癌(TCGA-LUSC,n = 493)(e)和肝癌(TCGA-LIHC,n = 365)(g)中SIRPA高表达和低表达患者的总生存率。
d, f, h. 结肠癌(GSE17536和GSE17537,n = 187)(d)、肺鳞状细胞癌(TCGA-LUSC,n = 476)(f)和肝癌(TCGA-LIHC,n = 359)(h)中SIRPA高表达和低表达患者的无病生存率。
i-j. DSS诱导过程中WT小鼠(n = 7只)和Sirpa-/-小鼠(n = 7只)的体重变化(i)和结肠炎病情活动指数(j)。病情活动指数通过总结体重损失分数计算得出。
k. MC38-Vector和MC38-CD47−/−细胞在基础和炎症条件下CD47的表达水平(n = 3个独立实验)。
l. 未经治疗的WT小鼠(对照组;n = 6只)、接受抗CD47治疗的WT小鼠(n = 6只)、接受Sirpa-ED-FC蛋白治疗的WT小鼠(n = 6只)和未经治疗的Sirpa−/−小鼠(n = 9只)中MC38肿瘤的生长情况。
数据汇总自2个独立实验(a)、3个独立实验(k)或来自5个独立实验中的一个代表(b),以及一个独立实验(i, j, l)。生存分析的P值(a-h)通过对数秩检验获得。体重和病情活动指数的P值(i, j, l)通过未配对的学生t检验(双尾)获得,k的P值通过比例配对的学生t检验(双尾)获得。误差条表示均值 ± 标准误差。

扩展数据图 5 | Sirpα缺失重塑肿瘤浸润免疫细胞(TIICs)的细胞构成和免疫功能。
a. 所有免疫细胞的t-SNE可视化,按野生型小鼠和Sirpa−/−小鼠的来源着色。
b. 所有免疫细胞中每种细胞类型的前五个差异表达基因的平均表达量。
c. 通过单细胞解卷积(scDC)计算的WT小鼠和Sirpa−/−小鼠中AOM/DSS诱导的肿瘤内每种细胞类型的比例。P值通过scDC中的GLM模型的自助重采样计算得出。
d. 通过流式细胞术分析的WT小鼠(n = 9-12个样本)或Sirpa−/−小鼠(n = 6-9个样本)中AOM/DSS诱导的自发性结直肠肿瘤中的免疫细胞百分比。
e. WT小鼠与其Sirpa−/−小鼠对应物之间AOM/DSS诱导的CRC中每种细胞类型的差异表达基因数量。
f. 使用QuSAGE比较Sirpa−/−小鼠和WT小鼠中AOM/DSS诱导的CRC中mMDSC的抗原呈递评分、吞噬评分和炎症反应评分。X轴代表基因集评分的log2(倍数变化)。
g-i. 在Sirpa−/−小鼠相比WT小鼠中,AOM/DSS诱导的CRC中ILCs(g)、B细胞(h)和浆细胞(i)的显著富集特征(Wilcoxon检验,双侧)。
所有样本均来自独立的小鼠。数据(d)表示为来自4个独立实验的均值 ± 标准误差,并使用未配对的学生t检验(双尾)进行分析。
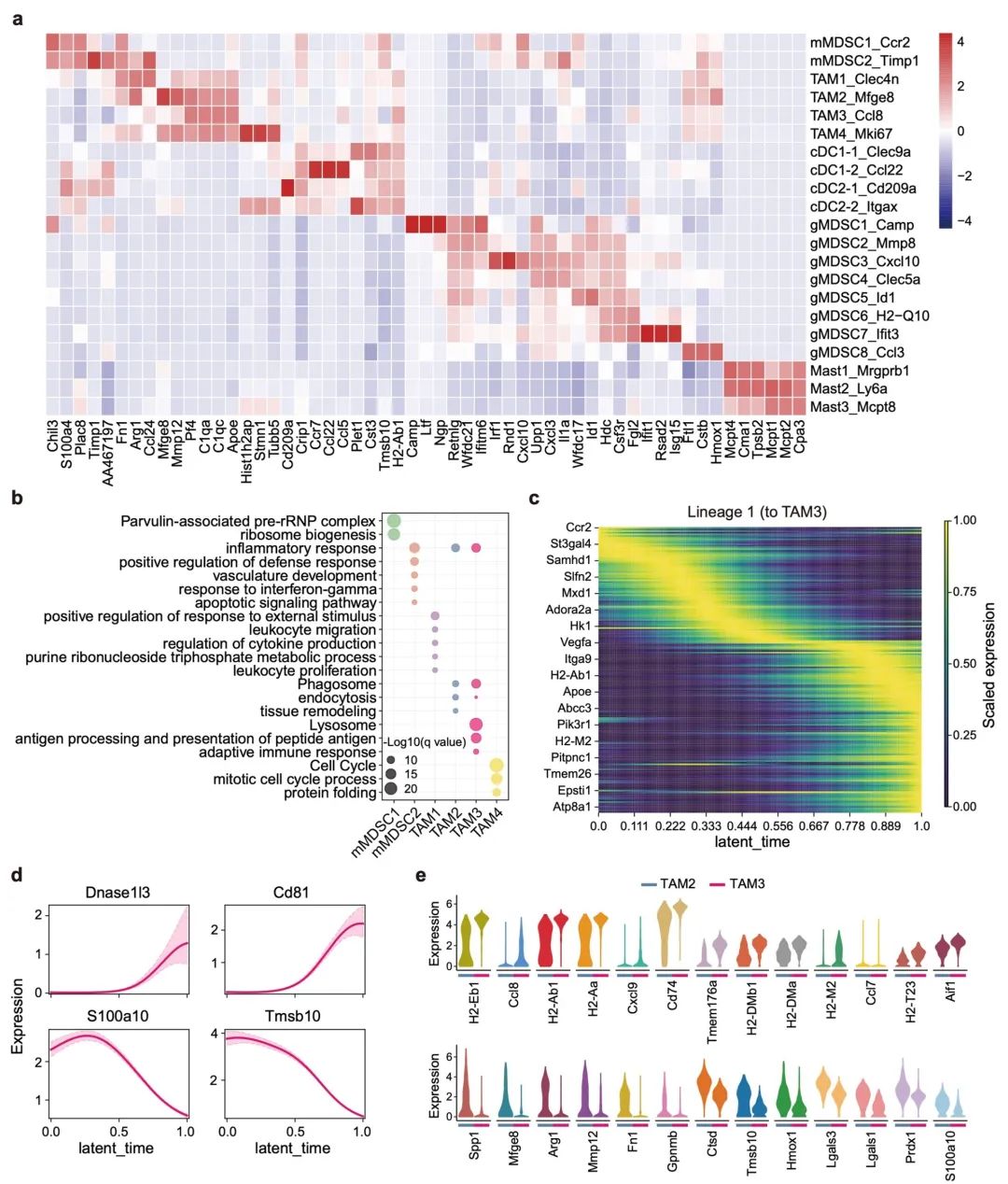
扩展数据图 6 | Sirpα缺失重编程了肿瘤中的巨噬细胞亚群和谱系。
a. 所有髓系细胞亚群中每个亚群的前三个特异性基因的表达水平。
b. mMDSC1-2和TAM1-4簇富集的最显著特征。
c. 在拟时序分析中,根据在伪时间中的峰值排序,表达值与谱系1(至TAM3)命运概率最佳相关的前100个基因的平滑化表达趋势。并非所有基因名称都显示出来。
d. 伪时间中与谱系1(至TAM3)相关的基因Dnase1l3、Cd81、S100a10和Tmsb10的平滑化表达趋势(95%置信区间)。
e. 与TAM2相比,在TAM3中表达上调的基因(顶部)和表达下调的基因(底部)。所有基因在TAM3和TAM2亚群间显示出显著的统计差异(Wilcoxon检验,双侧,p < 0.05)。
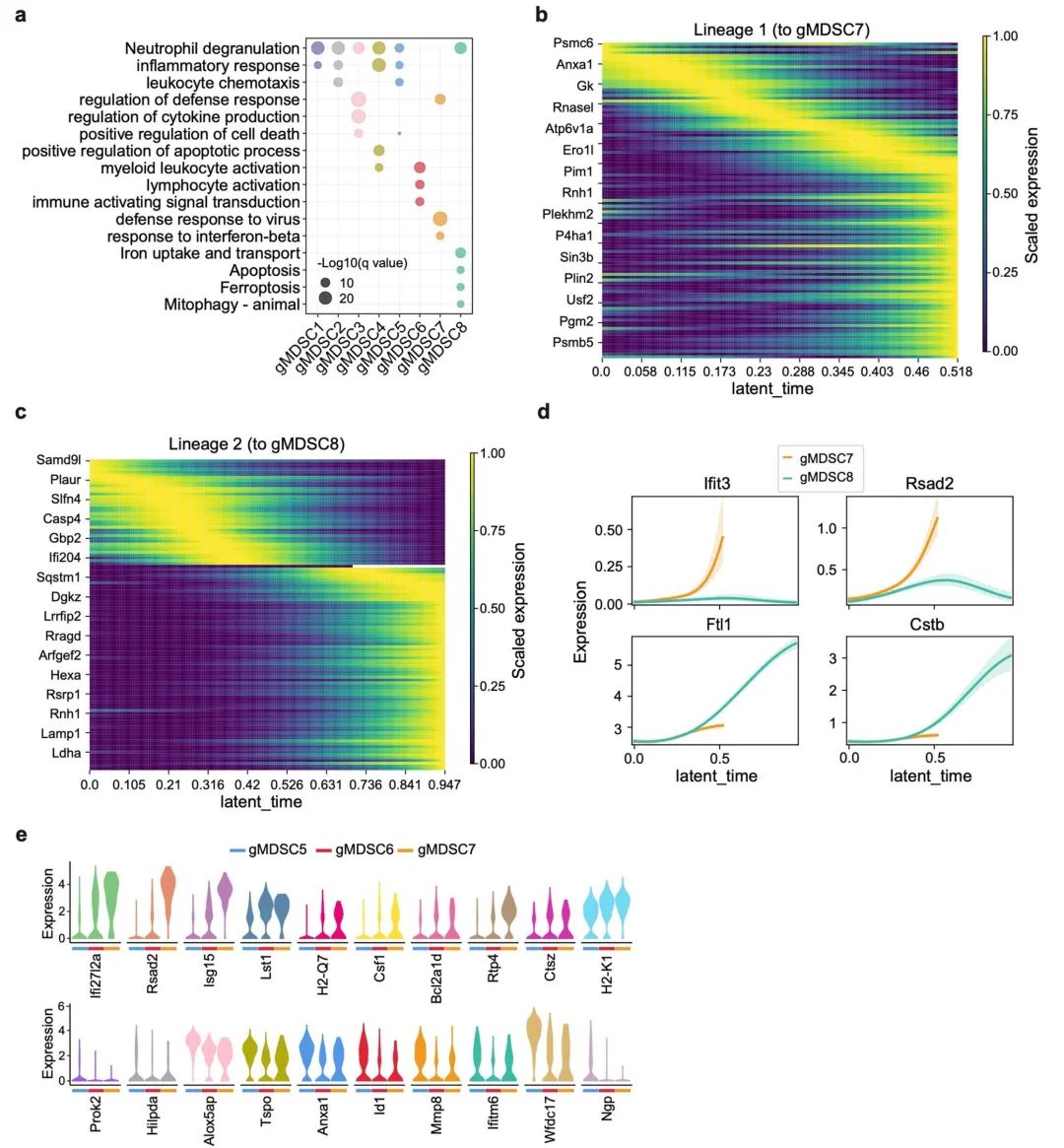
扩展数据图 7 | Sirpα缺失在肿瘤中重编程了gMDSC亚群和谱系。
a. gMDSC1-gMDSC8簇的显著富集特征。
b, c. 在拟时序分析中,根据在伪时间中的峰值排序,表达值与谱系1(至gMDSC7)(b)或谱系2(至gMDSC8)(c)命运概率最佳相关的前100个基因的平滑化表达趋势。并非所有基因名称都显示出来。
d. 拟时序分析中与谱系1(至gMDSC7)和谱系2(至gMDSC8)相关的基因Ifit3、Rsad2、Ftl1和Cstb的平滑化表达趋势(95%置信区间)。
e. 在gMDSC6/gMDSC7与gMDSC5比较中,表达上调的基因(顶部)和表达下调的基因(底部)。所有基因在gMDSC6/gMDSC7和gMDSC5亚群间显示出显著的统计差异(Wilcoxon检验,双侧,p < 0.05)。
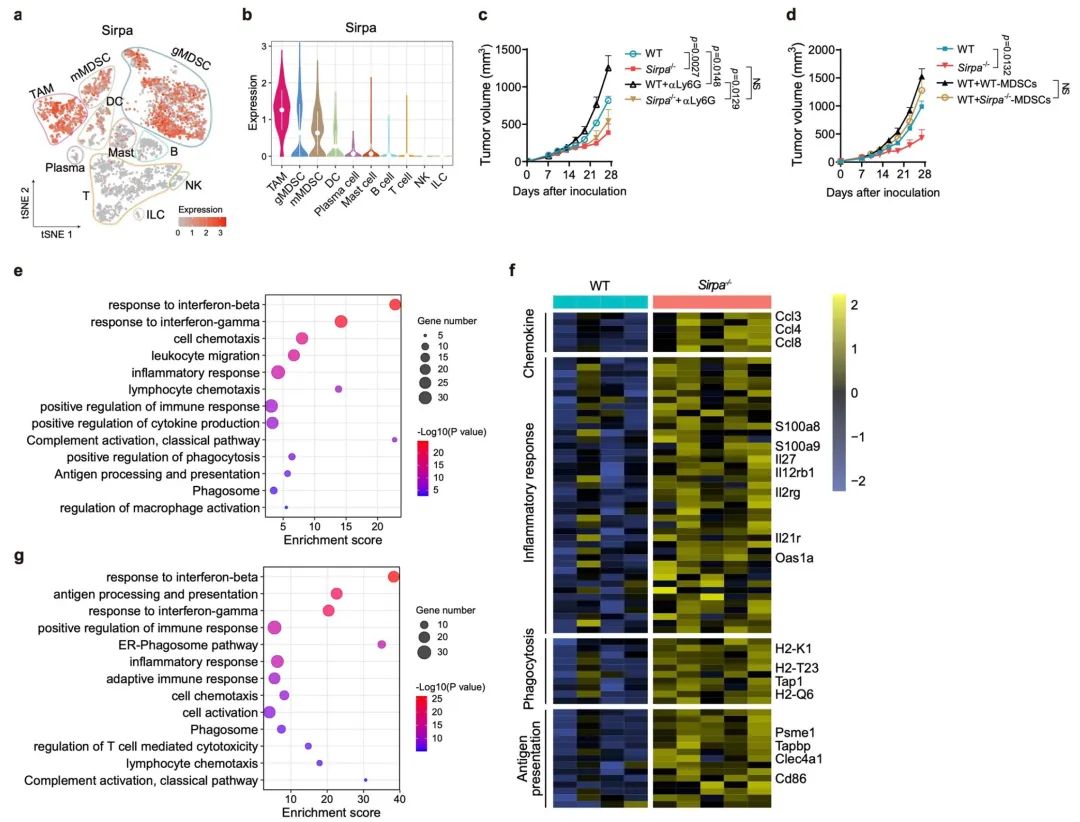
扩展数据图 8 | Sirpα-/- gMDSCs在抗肿瘤免疫和TAMs中的作用较弱。
a. WT小鼠中TIICs的Sirpa的t-SNE可视化,根据表达水平着色。
b. 小鼠肿瘤微环境中每种免疫细胞类型中Sirpa的表达。中间的白点和线代表中位数和四分位数值。
c. WT小鼠(n = 9只)、Sirpa−/−小鼠(n = 6只)、WT + αLy6G小鼠(n = 7只)和Sirpa−/− + αLy6G小鼠组(n = 5只)体内皮下MC38肿瘤的生长。
d. WT小鼠(n = 5只)、Sirpa−/−小鼠(n = 5只)、WT + WT-MDSCs小鼠(n = 6只)和WT + Sirpa−/−MDSCs小鼠组(n = 7只)体内皮下MC38肿瘤的生长。
e. 在MC38模型中,Sirpa−/−小鼠和WT小鼠之间TAMs的差异表达基因的富集特征(批量RNA测序数据)(Wilcoxon检验,双侧)。
f. 在MC38模型中,Sirpa−/−小鼠和WT小鼠之间TAMs的差异表达基因的热图,主要显示了与趋化因子、炎症反应、吞噬作用和抗原呈递相关的基因(批量RNA测序数据)。
g. 在MC38模型(批量RNA测序数据)和AOM/DSS模型(单细胞RNA测序数据)中,Sirpa−/−小鼠高表达基因在TAMs中的富集特征(Wilcoxon检验,双侧)。
结果(c)代表三个独立实验中的一个。结果(d)来自一个独立实验。误差条显示均值 ± 标准误差。对于c和d,使用了未配对的学生t检验(双尾)。
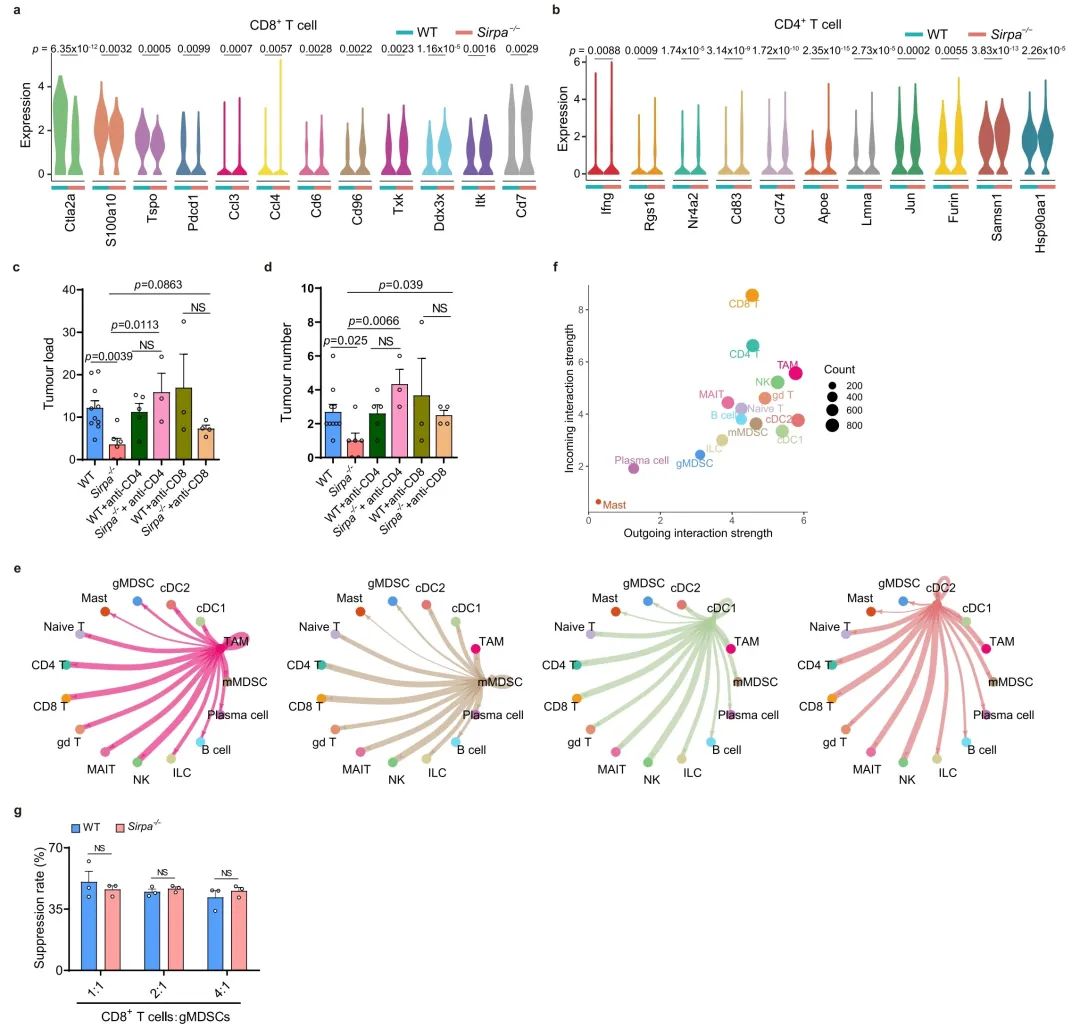
扩展数据图 9 | Sirpa-/-髓系细胞增强了T淋巴细胞的激活。
a, b. 在AOM/DSS诱导的CRC中,WT小鼠与Sirpa-/-小鼠之间CD8+ T细胞(a)或CD4+ T细胞(b)差异表达基因的表达(Wilcoxon检验,双侧)。
c-d. 在AOM/DSS诱导的WT小鼠和Sirpa-/-小鼠中,经CD4+或CD8+抗体处理后测量的肿瘤负荷(c)和肿瘤数量(d),WT(n = 9只小鼠),Sirpa-/-(n = 6只小鼠),WT + αCD4(n = 5只小鼠),Sirpa-/- + αCD4(n = 3只小鼠),WT + αCD8(n = 3只小鼠),Sirpa-/- + αCD8(n = 4只小鼠)。
e. 通过CellChat计算的AOM/DSS处理的WT小鼠和Sirpa-/-小鼠中TAM、mMDSC、cDC1和cDC2(发送者)到其他细胞类型(接收者)的细胞-细胞接触信号传递的L–R对。线宽表示信号强度,线颜色与信号发送者相同。
f. 通过CellChat计算的细胞-细胞接触信号网络中的主要发送者和接收者细胞类型。计数代表L–R对的数量。
g. 不同比例下,WT(n = 3个样本)或Sirpa-/-(n = 3个样本)gMDSCs抑制的CD8+ T细胞增殖。所有样本均来源于独立小鼠。结果(c, d, g)来自一个独立实验。误差条表示均值 ± 标准误差。对c, d, g使用了未配对的学生t检验(双尾)。
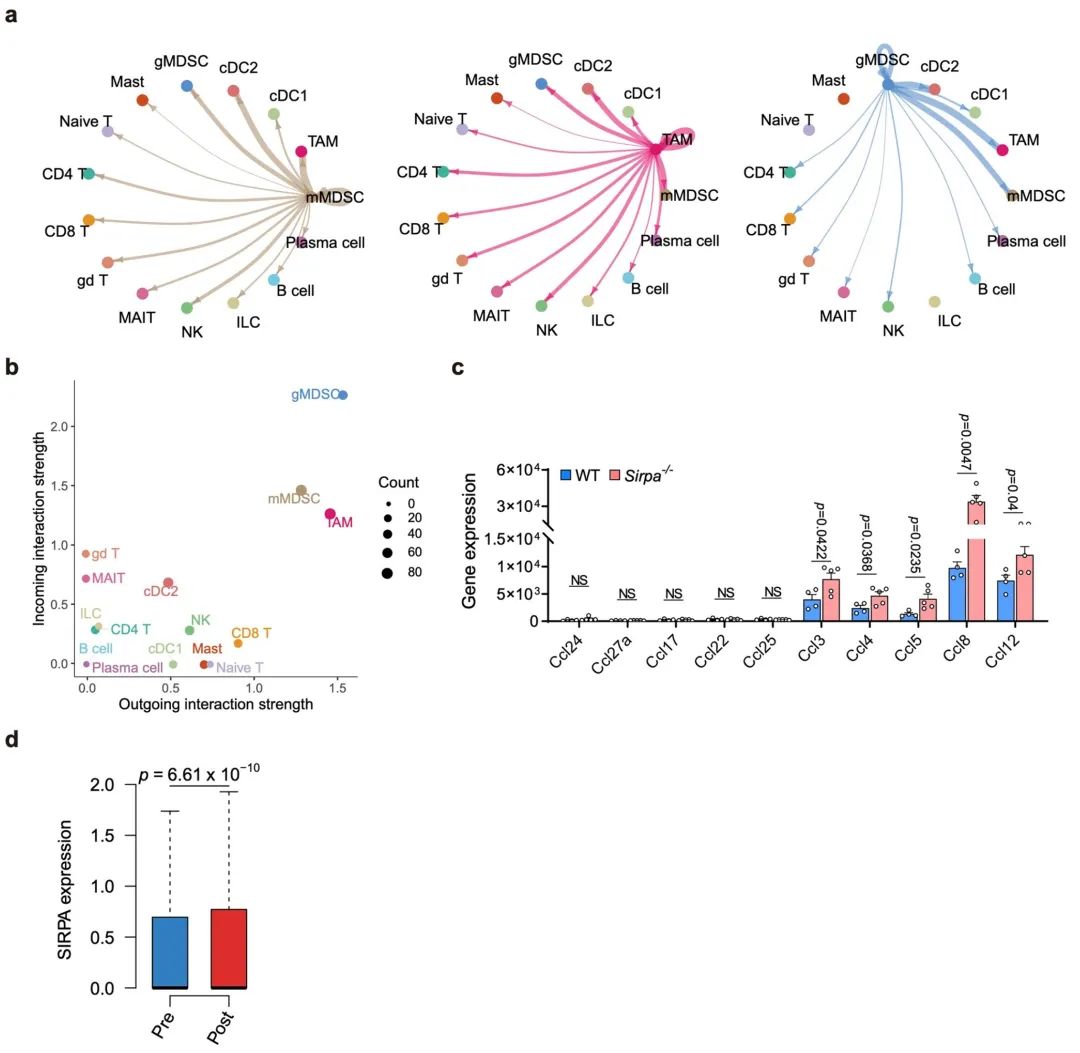
扩展数据图 10 | Sirpa-/-髓系细胞增强了T淋巴细胞的招募。
a. 通过CellChat计算的AOM/DSS处理的WT小鼠和Sirpa-/-小鼠中mMDSC、TAM和gMDSC(发送者)到其他细胞类型(接收者)的分泌信号传递的L–R对。线宽表示信号强度,线颜色与信号发送者相同。
b. 通过CellChat计算的趋化因子信号通路(CCL和CXCL通路)中的主要发送者和接收者细胞类型。计数代表L–R对的数量。
c. WT小鼠(n = 4个样本)和Sirpa-/-小鼠(n = 5个样本)MC38肿瘤中TAMs的各种趋化因子基因表达水平。
d. 盒形图显示复发性胶质母细胞瘤(GBM)患者在新辅助PD-1阻断治疗前后巨噬细胞上SIRPA的表达。
所有样本均来源于独立小鼠。使用双侧未配对t检验计算P值。结果(c)来自一个独立实验。误差条表示均值 ± 标准误差。对c使用了未配对的学生t检验(双尾)。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab