前期精彩内容:
Nature Cancer:肿瘤相关髓系细胞上的Sirpα在结直肠癌中独立于其与CD47相互作用抑制抗肿瘤免疫

杂志名称:Nature
发表日期:2022.11.02
DOI:10.1038/s41586-022-05374-w.
PubMed:https://pubmed.ncbi.nlm.nih.gov/36323780/
影响因子:64.8
内容简介
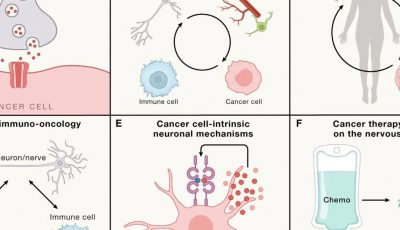
实体肿瘤受到自主神经和周围感觉神经系统中神经纤维的支配。目前尚不明确痛觉感受神经元(伤害感受器)对肿瘤新生神经内化及其对癌症免疫监视的影响。本研究揭示了黑色素瘤细胞与痛觉神经元之间的相互作用,这一互动促进了神经突起的生长、增加了对有害配体的响应性以及神经肽的释放。特别地,痛觉神经元产生的神经肽——降钙素基因相关肽(CGRP)——直接导致了细胞毒性CD8+ T细胞的耗竭,减弱了它们清除黑色素瘤的能力。TRPV1谱系的基因删除、痛觉神经元的局部药理抑制以及CGRP受体RAMP1的阻断,都能减轻肿瘤浸润的淋巴细胞耗竭并降低肿瘤生长,显著提高了接种B16F10黑色素瘤细胞小鼠的生存率。相反,当使用局部重组CGRP治疗去除痛觉神经元的小鼠时,CD8+ T细胞的耗竭问题再次出现。在Rag1缺陷小鼠中,与野生型CD8+ T细胞相比,Ramp1-/- CD8+ T细胞在共移植肿瘤时显示出更好的耐受性。黑色素瘤患者活检组织的单细胞RNA测序结果表明,表达RAMP1的CD8+ T细胞比不表达RAMP1的细胞更易耗竭,RAMP1的高表达与较差的临床预后相关。总而言之,我们的研究表明,减少肿瘤神经支配中痛觉神经元释放的CGRP,可能是通过消除其对细胞毒性CD8+ T细胞免疫调节作用的一种改善抗肿瘤免疫反应的策略。
创新性及研究意义
这篇文章的核心创新性在于揭示了伤害感受神经元如何通过与黑色素瘤细胞的相互作用,影响肿瘤的免疫监视机制。研究发现伤害感受神经元释放的神经肽—钙基因相关肽(CGRP)—直接导致细胞毒性CD8+ T细胞功能耗竭,减弱了它们清除肿瘤的能力。通过基因消融、药理学沉默和受体拮抗实验,研究证明抑制伤害感受神经元或其产生的CGRP可以显著降低肿瘤生长,提高携带肿瘤小鼠的生存率。
研究的意义在于为癌症免疫治疗提供了新的视角和潜在策略。通过针对伤害感受神经元及其产生的CGRP,可能开发出新的治疗方法,用以增强细胞毒性T细胞的功能,提高肿瘤的免疫清除能力。此外,单细胞RNA测序揭示了RAMP1表达与CD8+ T细胞耗竭及患者预后之间的相关性,为临床预测和治疗提供了新的分子标志物。总体而言,这项研究不仅增进了我们对肿瘤微环境中神经免疫相互作用的理解,也为癌症治疗提供了新的目标和策略。
数据图
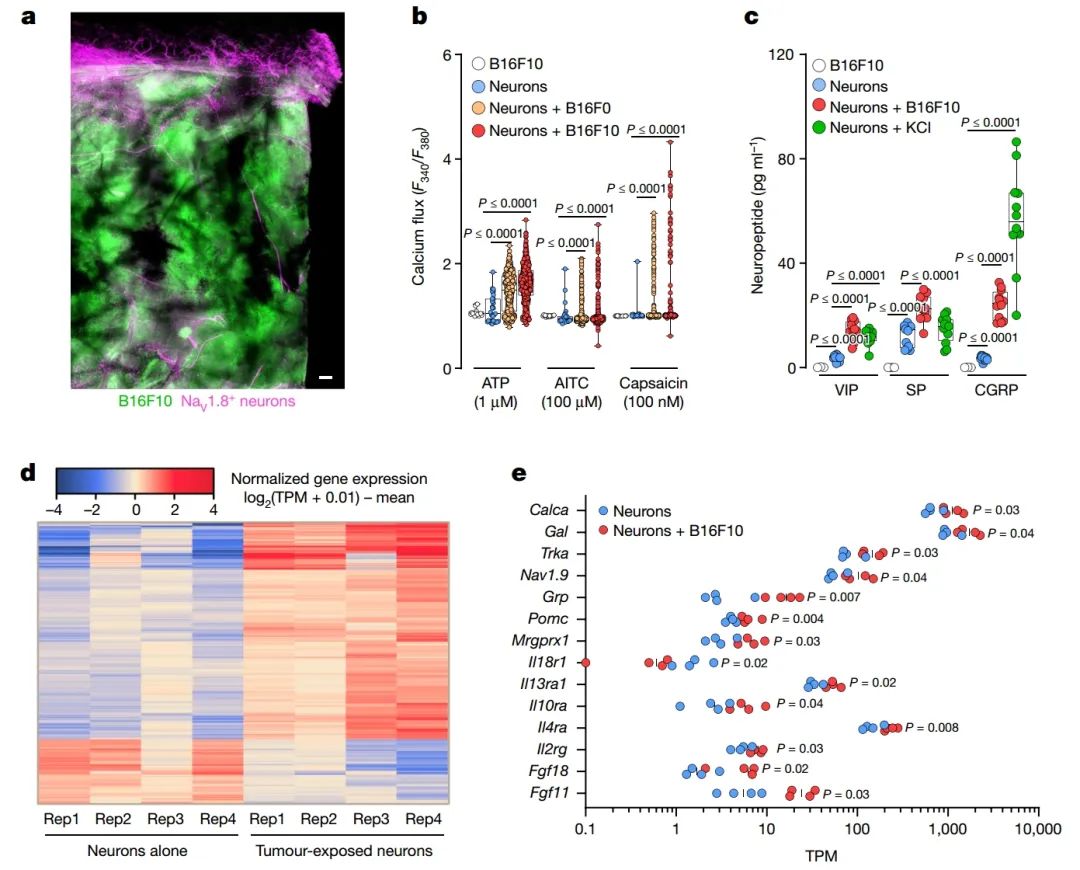
图 1 | 黑色素瘤细胞使伤害感受神经元敏感化
a、伤害感受器(Nav1.8cre::tdTomatofl/WT;洋红色)报告小鼠的后爪接种了B16F10-eGFP癌细胞(皮内注射,2×105个细胞;绿色)。显示B16F10-eGFP接种小鼠皮肤中与NaV1.8+神经纤维(洋红色)有神经连接的代表性图像,观察时间为22天。标尺,200μm。
b、在共培养中,B16F0或B16F10细胞使伤害感受器对辣椒素(100 nM)、异硫氰酸烯丙酯(AITC,100 μM)和ATP(1 μM)的反应敏感化,通过钙离子通量测量。低浓度的配体在对照神经元中引起最小的反应,而B16F10细胞对ATP的敏感性较小。
c、背根神经节(DRG)神经元与B16F10细胞共培养(96小时),释放物质P(SP)、血管活性肠肽(VIP)和CGRP。单独的B16F10细胞不释放神经肽。用KCl(40 mM;30分钟)刺激培养的神经元可显著释放神经肽。
d、e、原始DRG神经元(Trpv1cre::-CheRiff-eGFPfl/WT)单独培养或与B16F10-mCherry-OVA细胞组合培养。48小时后,收集细胞,进行FACS纯化和RNA测序。通过对排序的神经元的DEG进行层次聚类,显示了在暴露于癌细胞的TRPV1+神经元中富集的不同转录本组(d),包括Calca(编码CGRP的基因;e)。
数据显示为代表性图像(a),为盒须图(从最小到最大值;盒子从第25到第75百分位数,中间线表示中位数),给出了个体数据点(b、c),为显示归一化基因表达的热图(log2(0.01+每百万读数(TPM))-均值(d))或具有中位数的散点图(e)。
实验独立重复了两次(a)或三次(b、c),结果相似。RNA测序实验没有重复(d、e)。
n如下:a:n = 4;b:神经元(来自10只小鼠的29个神经元)、B16F10(来自10个培养皿的16个细胞)、神经元 + B16F0(来自12只小鼠的387个神经元)、神经元 + B16F10(来自12只小鼠的409个神经元);c:神经元(n = 12)、神经元 + B16F10(n = 12)、神经元 + KCl(n = 12)、B16F10(n = 3);d、e:每组n = 4。
P值由一元方差分析后进行Bonferroni(b、c)或双侧未配对的Student’s t检验(e)确定。
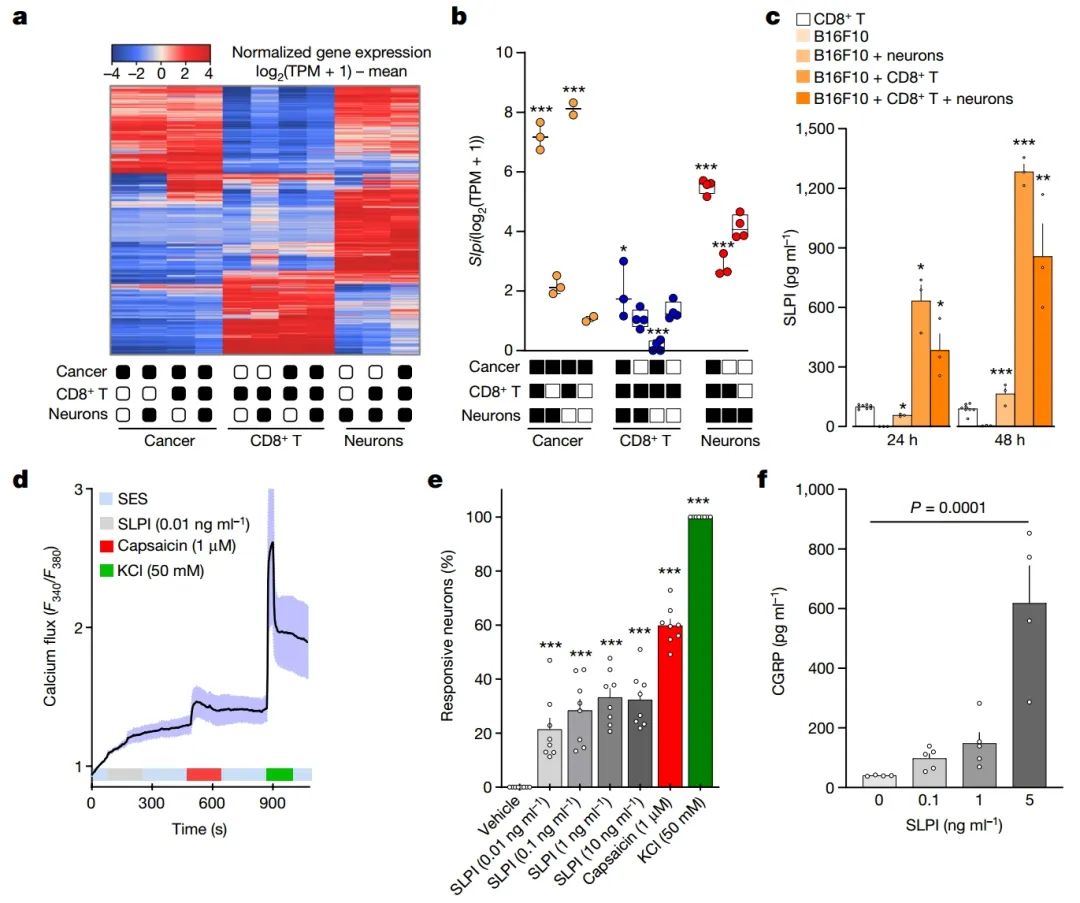
图 2 | 癌细胞分泌的SLPI驱动伤害感受器神经元释放CGRP
a-c, 未经处理的背根神经节(DRG)神经元(Trpv1cre::-CheRiff-eGFPfl/WT)、B16F10-mCherry-OVA细胞和OVA特异性细胞毒性CD8+ T细胞单独或组合培养。48小时后,收集细胞,通过流式细胞排序纯化并进行RNA测序。
a, 分选神经元分子轮廓的层次聚类描绘了每个组中富集的不同转录本群组。
b, 计算差异表达基因(DEGs),发现当与OVA特异性细胞毒性CD8+ T细胞、DRG神经元或两种细胞共培养时,癌细胞中Slpi过表达。
c, 当B16F10-mCherry-OVA细胞与未经处理的DRG神经元和OVA特异性细胞毒性CD8+ T细胞共培养(24小时或48小时)时,会分泌SLPI,48小时后效果最大。
d-f, 使用钙显微镜技术发现,SLPI(10 pg ml−1 – 10 ng ml−1)激活了约20%的培养未经处理DRG神经元(d,e)。用SLPI(3小时)激活的培养神经元也会显著释放CGRP(f)。
数据以热图显示标准化基因表达(log2(1 + TPM)− 平均值(a),箱形图(定义见图 1b,c)(b)或平均值 ± 标准误(c–f)显示。
样本数量如下:a,b: 每组n = 2–4;c: 所有组n = 3,除了CD8+ T细胞(n = 8);d: n = 17;e: 每组n = 8;f: 0 ng ml−1(n = 4),0.1 ng ml−1(n = 5),1 ng ml−1(n = 5),5 ng ml−1(n = 4)。
c-f中的实验独立重复三次,结果相似。测序实验未重复(a,b)。
P值通过单因素方差分析配合事后Bonferroni校正(b,e,f)或双侧未配对学生t检验确定(c)。*P ≤ 0.05, **P ≤ 0.01, ***P ≤ 0.001。
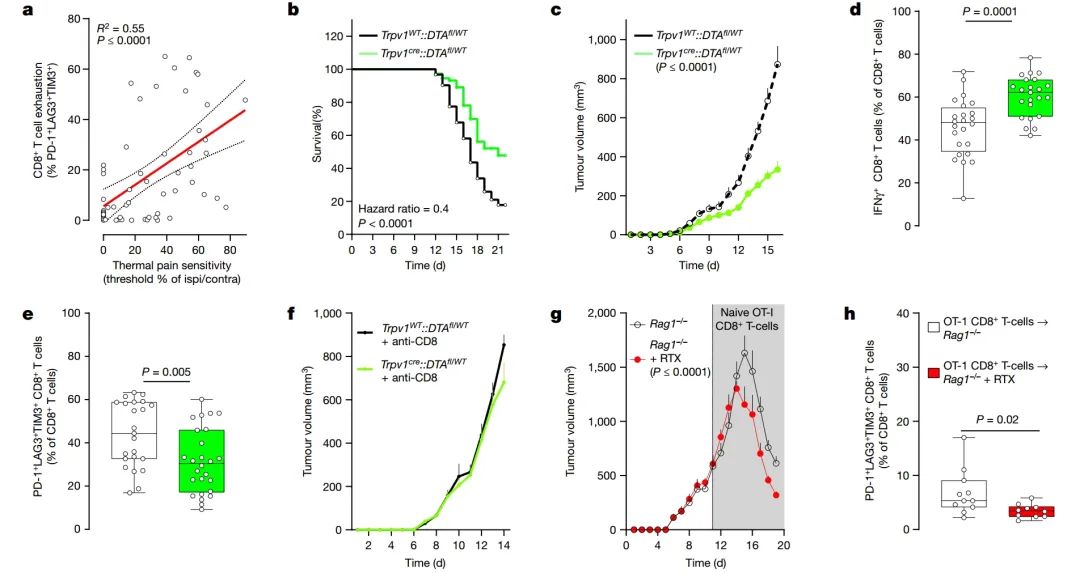
图 3 | 伤害感受器的遗传消除保护抗肿瘤免疫力
a, 向野生型小鼠的左后爪内侧注射正位点B16F10-mCherry-OVA细胞(2 × 105个细胞,i.d.)。根据肿瘤接种后第13天的测量,肿瘤内CD8+ T细胞的耗竭与热超敏感性正相关(R2 = 0.55, P ≤ 0.0001)。热痛超敏反映了同侧爪(接种肿瘤的)与对侧爪的撤回延迟期比值。
b, 将正位点B16F10-mCherry-OVA(5 × 105个细胞,i.d.)接种到保留有感觉神经元(Trpv1WT::DTAfl/WT)或经消除的(Trpv1cre::DTAfl/WT)八周大雄性和雌性小鼠的胁侧。在接种后22天内测量,伤害感受器消除的小鼠中位生存时间增加了约250%。
c-f, 肿瘤接种后16天,感觉神经元消除的小鼠显示出减少的肿瘤生长(c)和增加的肿瘤内IFNγ+ CD8+ T细胞浸润(d),同时PD-1+ LAG3+ TIM3+ CD8+ T细胞的比例降低(e)。在伤害感受器消除的小鼠中,B16F10-mCherry-OVA(5 × 105个细胞,i.d.)肿瘤体积的减少在全身消耗CD8+ T细胞的小鼠中未见(f;评估至第14天;抗CD8,每只小鼠200微克,腹腔注射,每3天一次)。
g,h, 为化学消除其伤害感受器神经元,Rag1−/−小鼠被注射RTX。28天后,小鼠被接种B16F10-mCherry-OVA(5 × 105个细胞,i.d.)。接受RTX注射且被动转移OVA特异性CD8+ T细胞(i.v.,1 × 106细胞,当肿瘤达到约500 mm3时)的小鼠显示出比暴露于载体的Rag1−/−小鼠更少的肿瘤生长(g;评估至第19天)和耗竭(h)。
数据以线性回归分析 ± s.e.(a)、Mantel–Cox回归(b)、平均值 ± s.e.m.(c,f,g)或箱形图(如图 1b,c定义),并给出单独数据点(d,e,h)显示。
样本数量如下:a: n = 60;b: 完整(n = 62),消除(n = 73);c: 完整(n = 20),消除(n = 25);d: 完整(n = 24),消除(n = 23);e: 完整(n = 23),消除(n = 26);f: 完整 + 抗CD8(n = 10),消除 + 抗CD8(n = 8);g: 载体(n = 12),RTX(n = 10);h: 载体(n = 11),RTX(n = 10)。
实验分别重复两次(a,f–h)或六次(b–e)得到相似结果。P值通过简单线性回归分析(a)、Mantel–Cox回归(b)、双因素方差分析配合事后Bonferroni校正(c,f,g)或双侧未配对学生t检验(d,e,h)确定。
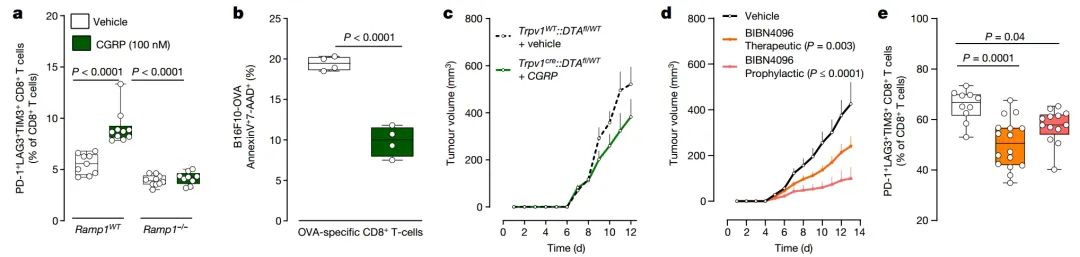
图 4 | CGRP调节CD8+ T细胞的活化
a,b, 来自野生型(a)、Ramp1−/−(a)或未经处理的OT-I(b)小鼠的脾细胞CD8+ T细胞在Tc1刺激条件下(通过CD3和CD28、IL-12和抗IL4外源性激活)培养48小时,以产生细胞毒性CD8+ T细胞。在IL-2(10 ng ml−1)存在下,用CGRP(100 nM;每两天挑战一次)刺激细胞96小时。野生型细胞毒性CD8+ T细胞显示PD-1+ LAG3+ TIM3+细胞比例增加;当处理来自Ramp1−/−小鼠的细胞毒性CD8+ T细胞时,这种效应不存在(a)。在共培养中(48小时),CGRP(100 nM;每天一次)还降低了OT-I细胞毒性CD8+ T细胞(4 × 105个细胞)清除B16F10-mCherry-OVA癌细胞的能力(b)。
c, 将正位点B16F10-mCherry-OVA细胞(5 × 105个细胞,i.d.)接种入八周大的雌性小鼠,这些小鼠的感觉神经元保持完整或被消除。在伤害感受器被消除的小鼠中,肿瘤周围注射重组CGRP(100 nM,i.d.,每天一次)可以恢复B16F10的生长(评估至第12天)。
d,e, 将正位点B16F10-mCherry-OVA细胞(5 × 105个细胞,i.d.)接种入八周大的雄性和雌性小鼠。从接种后第一天开始(定义为预防性),系统性给予RAMP1拮抗剂BIBN4096(5 mg kg−1),每两天一次(i.p.)。在另一组小鼠中,当肿瘤体积达到约200 mm3时,开始BIBN4096(5 mg kg−1,i.p.,每两天一次)注射(定义为治疗性)。预防性或治疗性BIBN4096治疗减少了肿瘤生长(d)并降低了肿瘤内PD-1+ LAG3+ TIM3+ CD8+ T细胞的比例(e;评估至第13天)。
数据以箱形图(如图 1b, c定义),并给出单独数据点(a,b,e),或以平均值 ± s.e.m.(c,d)显示。
样本数量如下:a: Ramp1WT CD8 + 溶剂对照(n = 9),Ramp1WT CD8 + CGRP(n = 10),Ramp1−/− CD8 + 溶剂对照(n = 10),Ramp1−/− CD8 + CGRP(n = 9);b: 每组n = 4;c: 完整 + 溶剂对照(n = 15),消除 + CGRP(n = 11);d: 溶剂对照(n = 13),BIBN预防(n = 16),BIBN治疗(n = 18);e: 溶剂对照(n = 10),BIBN预防(n = 13),BIBN治疗(n = 16)。
实验独立重复三次,结果相似。P值通过单因素方差分析配合事后Bonferroni校正(a,e)、双侧未配对学生t检验(b)或双因素方差分析配合事后Bonferroni校正(c,d)确定。
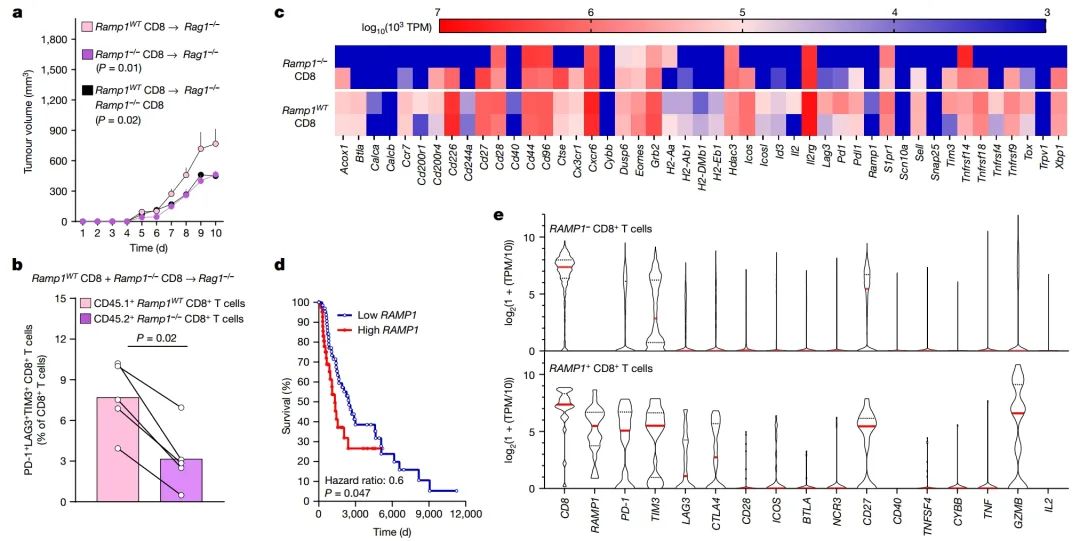
图 5 | CGRP减弱RAMP1+ CD8+ T细胞的抗肿瘤免疫力
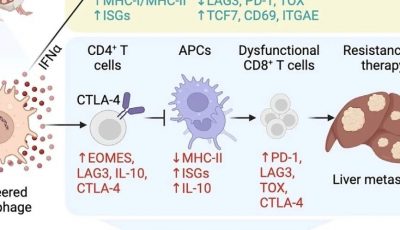
a–c, 从Ramp1WT(CD45.1+)或Ramp1−/−(CD45.2+)小鼠中纯化分离脾脏CD8+ T细胞,体外扩增并刺激(CD3和CD28 + IL-2)。将激活的Ramp1−/−或Ramp1WT CD8+ T细胞或Ramp1−/−与Ramp1WT CD8+ T细胞1:1混合物(每只2.5 × 106细胞)通过静脉移植至八周大的雌性Rag1−/−小鼠。移植后一周,小鼠被接种B16F10-mCherry-OVA细胞(5 × 105细胞,i.d.)。在B16F10接种后十天,我们观察到在Ramp1WT移植的小鼠中肿瘤生长更快(a)。肿瘤内的Ramp1−/−(CD45.2+)和Ramp1WT(CD45.1+)CD8+ T细胞被流式细胞术纯化、免疫表型鉴定(b)并进行RNA测序(c)。Ramp1−/− CD8+ T细胞显示出较低比例的PD-1+ LAG3+ TIM3+ CD8+ T细胞(b),以及减少的耗竭标记物转录本表达(c)。
d, 利用癌症基因组图谱(TCGA)数据的体内分析40用来相关联459名黑色素瘤患者的生存率与RAMP1表达水平(原始活检大规模RNA测序)。与RAMP1表达低的患者相比,更高的RAMP1水平与患者生存率下降相关。
e, 人类黑色素瘤的单细胞RNA测序的体内分析揭示,与Ramp1阴性CD8+ T细胞相比,肿瘤内RAMP1表达的CD8+ T细胞强烈过表达数个免疫检查点受体(PD-1(也称为PDCD1)、TIM3、LAG3、CTLA4)。
数据以平均值 ± s.e.m.(a)、坡度图(b)、热图显示标准化基因表达(log10(103 × TPM))(c)、Mantel–Cox回归(d)或小提琴图(e)显示。
实验独立重复两次(a,b)得到相似结果。测序实验未重复(c)。
P值通过双因素方差分析配合事后Bonferroni校正(a)、双侧未配对学生t检验(b)或Mantel–Cox回归(d)确定。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab