前期精彩内容:
Nature Cancer:肿瘤相关髓系细胞上的Sirpα在结直肠癌中独立于其与CD47相互作用抑制抗肿瘤免疫
杂志名称:Cancer Cell
发表日期:2024.03.01
DOI:10.1016/j.ccell.2024.02.013.
PubMed:https://pubmed.ncbi.nlm.nih.gov/38490213/
影响因子:50.3
内容简介
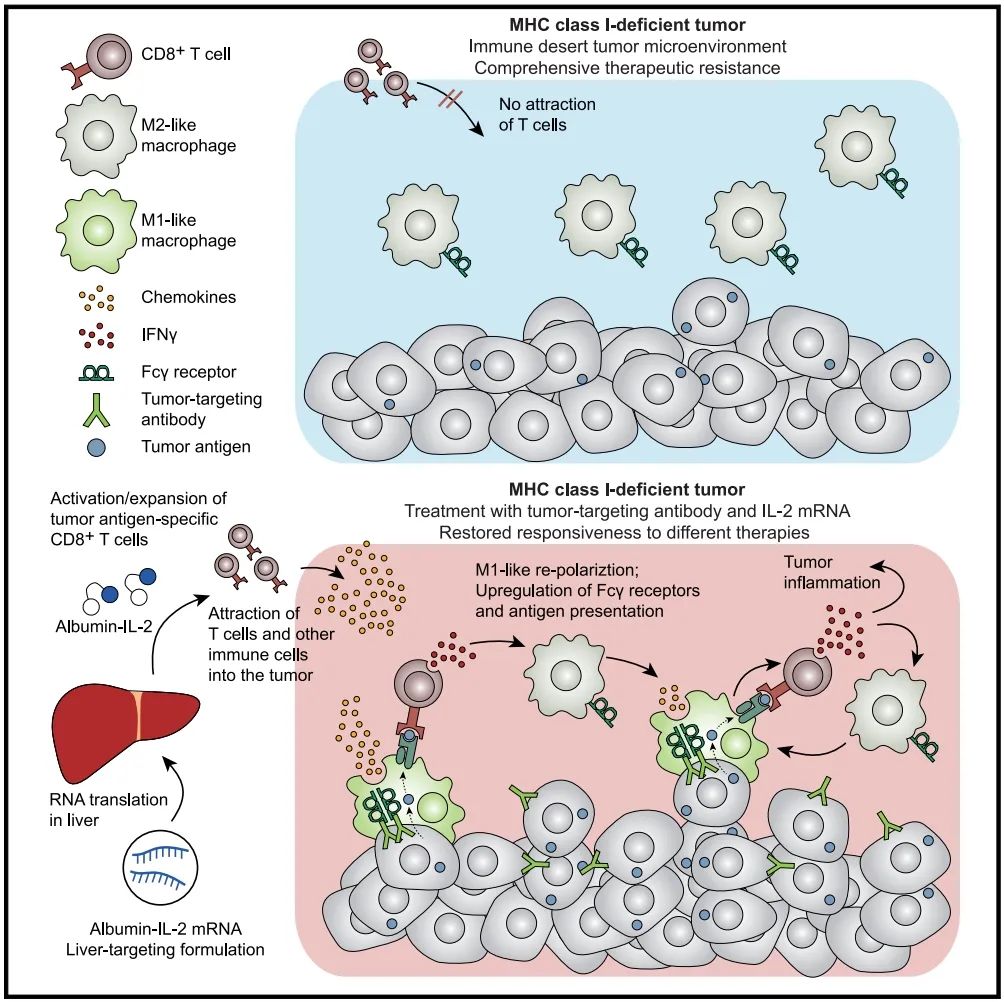
主要组织相容性复合体(MHC)I类抗原呈递缺陷是癌症免疫逃逸的常见机制,但对其机制和解决这一挑战的潜在策略仍然了解不足。通过β2-微球蛋白(B2M)缺陷的小鼠肿瘤模型,研究者发现MHC I类缺失导致肿瘤微环境(TME)的大量免疫荒漠化以及对免疫、化疗和放疗的广泛抵抗。该研究还展示了通过mRNA技术编码持久性IL-2进行治疗可以恢复免疫细胞浸润、IFNγ促进的高度炎症的TME特征,并且当与针对肿瘤的单克隆抗体(mAB)联合使用时,可以克服治疗抗性。意外的是,这种治疗的有效性是由释放IFNγ的CD8+ T细胞驱动的,这些细胞识别由TME中活化的巨噬细胞交叉呈递的新抗原。在IL-2治疗下,这些巨噬细胞获得了增强的抗原呈递能力和其他M1表型相关特征。该研究的发现强调了在治疗MHC I类缺陷癌症中恢复新抗原特异性免疫应答的重要性。
创新性及研究意义
这篇文章的核心创新性在于揭示了一种新的癌症治疗策略,即通过mRNA技术编码的长效IL-2来恢复MHC I类分子缺陷癌症中针对新抗原的CD8+ T细胞免疫反应。文章研究了β2-微球蛋白(B2M)缺失的小鼠肿瘤模型,发现MHC I类分子的缺失导致肿瘤微环境(TME)的免疫荒漠化和对免疫、化疗和放疗的广泛抵抗。
文章展示了长效mRNA编码的IL-2治疗能够恢复TME中的免疫细胞浸润、促进IFNγ驱动的高度炎症反应,并且当与针对肿瘤的单克隆抗体联合使用时,能够克服治疗抵抗。意外的发现是,这种治疗的有效性由能够识别由TME内活化的巨噬细胞跨呈递的新抗原的IFNγ释放CD8+ T细胞驱动。这些巨噬细胞在IL-2治疗下获得了增强的抗原呈递能力和其他M1表型相关的特征。
研究的意义在于强调了在治疗MHC I类缺陷癌症时,恢复针对新抗原的特异性免疫应答的重要性。这为克服癌症免疫逃逸机制提供了新的策略,并可能为MHC I类分子缺陷癌症的治疗开辟新的途径。
数据图
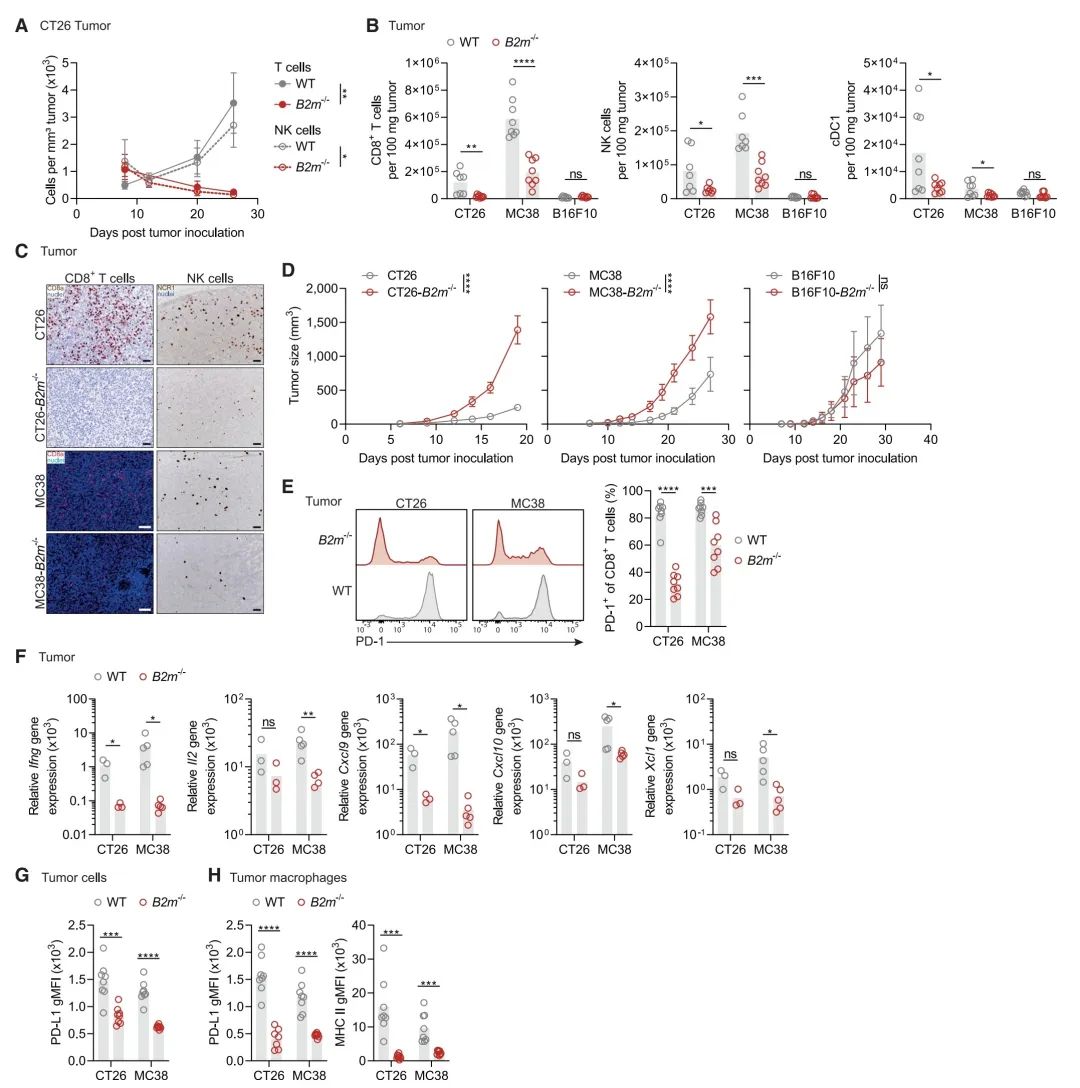
图1:MHC I类缺失肿瘤的免疫荒漠化
(A) 通过流式细胞术确定CT26或CT26-B2m-/-肿瘤中T细胞和NK细胞渗透的时间动态(每个时间点n = 4-5)。
(B) 通过流式细胞术,在接种后20天内确定CT26、MC38或B16F10野生型(WT)和B2m-/-肿瘤中免疫细胞的渗透情况(n = 8)。
(C) 通过αCD8免疫组化(IHC)或免疫荧光(IF)染色以及Ncr1原位杂交(ISH),在接种19天后确定CT26或MC38 WT和B2m-/-肿瘤中CD8+ T细胞和NK细胞的渗透(展示了代表性示例;每行代表一个单独的肿瘤)。比例尺=100 mm(IF)或50 mm(IHC, Ncr1 ISH)。
(D) CT26、MC38或B16F10 WT和B2m-/-细胞在体内的生长(n = 5)。
(E) 通过流式细胞术,在接种后20天内确定渗透CT26或MC38 WT和B2m-/-肿瘤组织中CD8+ T细胞的PD-1表达(n = 8)。
(F) 通过定量实时PCR(qRT-PCR),在接种后19天内确定CT26(n = 3)或MC38(n = 5)WT和B2m-/-肿瘤组织中所示基因的表达。
(G) 通过流式细胞术,在接种后20天内确定CT26或MC38 WT和B2m-/-肿瘤细胞中PD-L1的表达(n = 8)。
(H) 通过流式细胞术,在接种后20天内确定渗透CT26或MC38 WT和B2m-/-肿瘤的巨噬细胞中PD-L1和MHC II类的表达(n = 8)。
以均值作为汇总统计。误差条表示均值的标准误差(SEM)。通过Grubb’s检验移除了单个异常值(B)。通过两种方式ANOVA与Sidak’s事后检验(A, D)或学生的双尾非配对t检验(B, E, F, G, H)确定统计显著性。ns,不显著;*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S1。
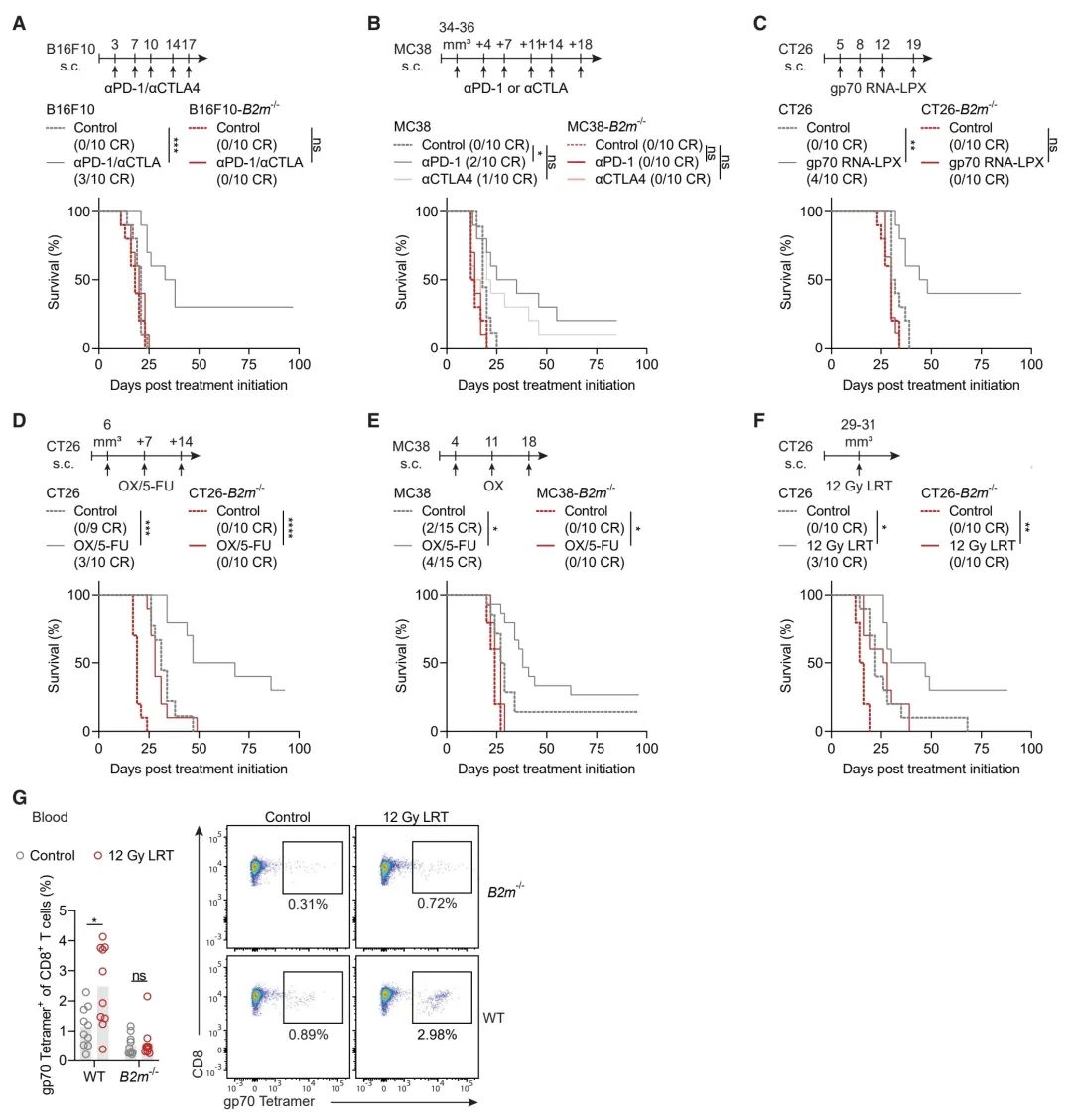
图2:MHC I类缺失肿瘤的治疗抵抗性
(A–F) 在接受以下治疗后,携带所示亲本或B2m-/-肿瘤变异体的小鼠的存活情况:αPD-1/αCTLA4组合治疗或同种型对照(A;n = 10)、αPD-1、αCTLA4或不相关对照单克隆抗体(B;n = 10)、编码gp70的mRNA-LPX疫苗或空载体mRNA-LPX作为对照(C;n = 10)、奥沙利铂(OX)/氟尿嘧啶(5-FU)双药治疗或车辆对照(D;n = 9–10)、OX或车辆对照(E;n = 10–15)、局部放疗(LRT),剂量为12 Gy或0 Gy作为对照(F;n = 10)。CR表示完全缓解。
(G) 在局部放疗(LRT)后9天,通过流式细胞术确定血液中gp70特异性CD8+ T细胞的数量(n = 10)。
以均值作为汇总统计。通过对数秩检验(A–F)或学生的双尾非配对t检验(G)确定统计显著性。ns表示不显著;*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S1。
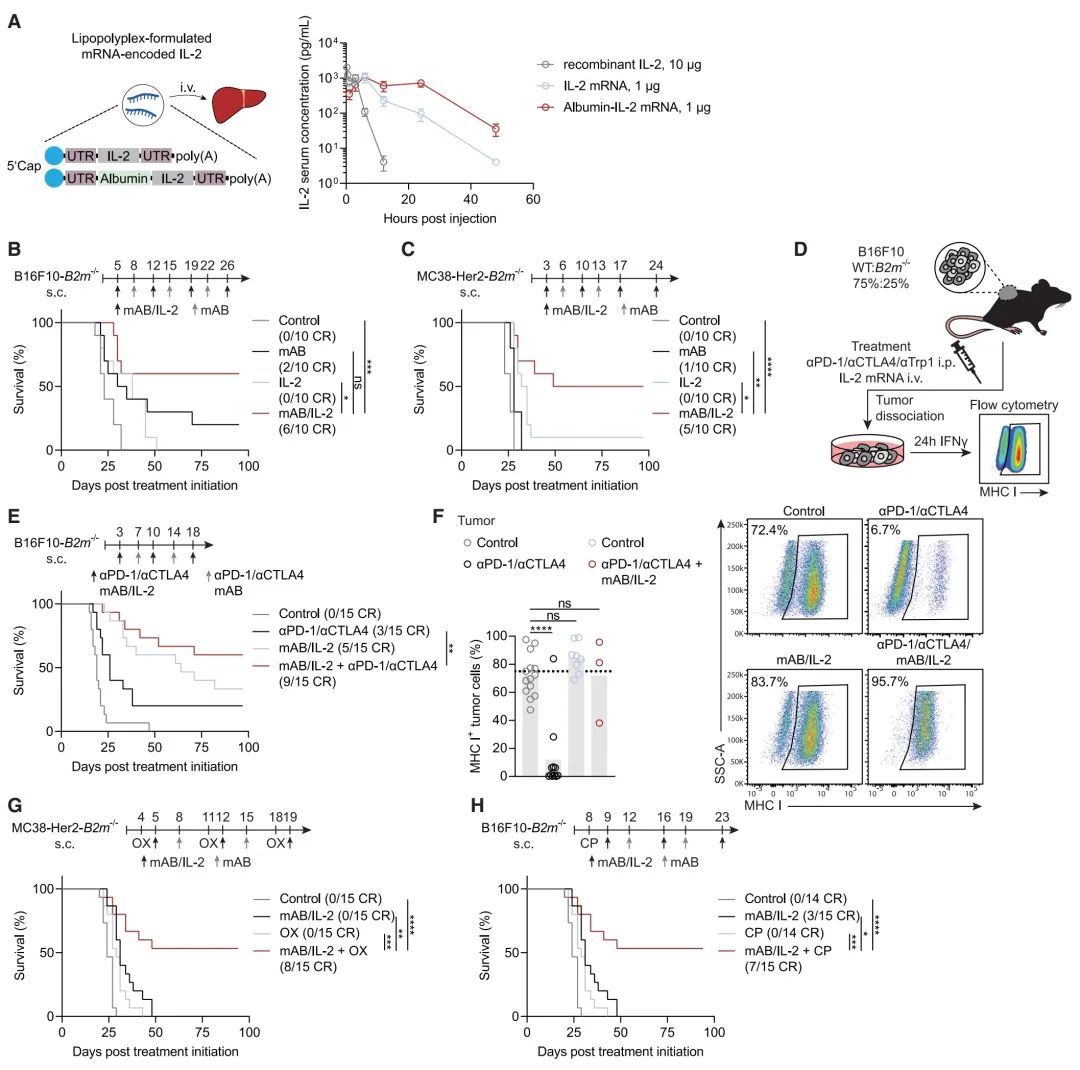
图3:通过mAB/IL-2治疗逆转MHC I类缺失肿瘤对多种治疗方式的抗性
(A) IL-2及其与白蛋白结合的IL-2 mRNA的示意图,包括5’端帽子结构、5’和3’非翻译区(UTR)、开放阅读框架两侧以及多腺苷酸尾巴(左图),以及与重组蛋白相比,通过mRNA传递的长效IL-2的药代动力学(右图;n = 3)。
(B 和 C) 经αTrp1(B)或αHer2(C)单克隆抗体和IL-2治疗的B16F10-B2m-/-(B)或MC38-Her2-B2m-/-(C)肿瘤小鼠的生存情况,或者分别使用这两种化合物(n = 10)。CR表示完全缓解。
(D) 异质性B16F10:B16F10-B2m-/-肿瘤模型的治疗和分析方案。
(E) 接种异质性B16F10:B16F10-B2m-/-肿瘤并接受αTrp1单克隆抗体/IL-2、αPD-1/αCTLA4组合治疗或四联治疗的小鼠的生存情况(n = 15)。
(F) 通过流式细胞术,在IFNγ体外刺激24小时后,确定达到终点标准的小鼠异质肿瘤中MHC I类+ B16F10细胞的数量(n = 3–14)。虚线代表接种时MHC I类+细胞的比例。
(G 和 H) 经αHer2单克隆抗体/IL-2、奥沙利铂(OX)或三联组合(G;n = 15)治疗的MC38-Her2-B2m-/-肿瘤小鼠的生存情况,或经αTrp1单克隆抗体/IL-2、环磷酰胺(CP)或三联组合(H;n = 14–15)治疗的B16F10-B2m-/-肿瘤小鼠的生存情况。所有实验中使用编码白蛋白的mRNA和同种型单克隆抗体作为对照。
均值作为汇总统计数据。误差条代表SEM。统计显著性通过对数秩检验(B, C, E, G, H)或单向ANOVA配合Dunnett’s事后检验(F)确定。ns表示不显著;*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S2和S3。
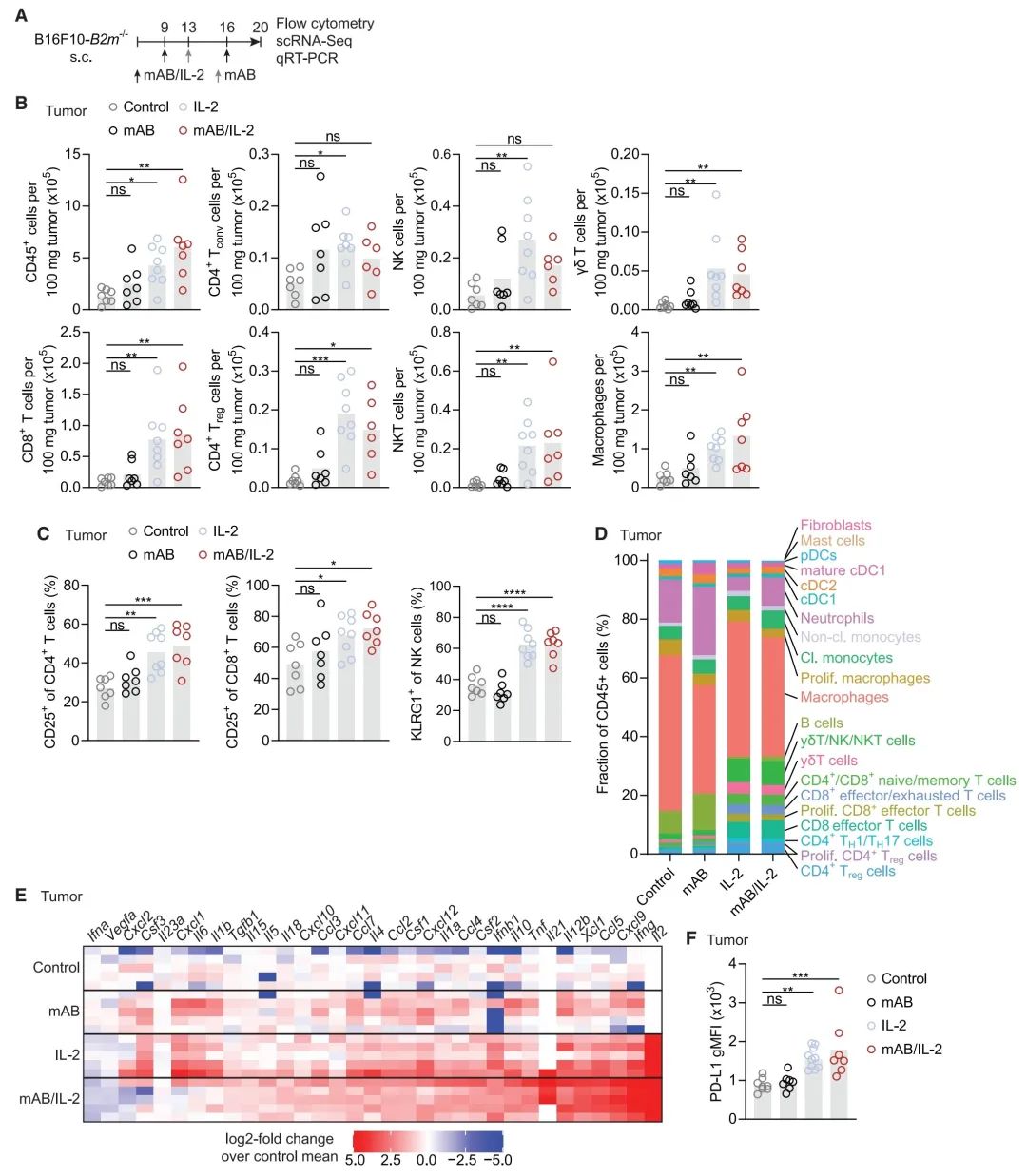
图4:IL-2在肿瘤微环境中引发与IFN相关的炎症特征标志
(A) 实验示意图,分析经αTrp1单克隆抗体和IL-2或其中任一治疗后的B16F10-B2m-/-肿瘤。
(B 和 C) 通过流式细胞术确定的指定肿瘤浸润免疫细胞亚群中免疫细胞浸润(B)和激活标志物上调(C)(n = 7–8)。
(D) 通过单细胞RNA测序(scRNA-seq)确定的不同治疗组中细胞类型簇的比例(每组n = 3汇总)。
(E) 通过定量实时PCR(qRT-PCR)确定的整个肿瘤组织中细胞因子和趋化因子表达的log2倍变化(n = 5;每行代表一个独立的肿瘤)。
(F) 通过流式细胞术确定的B16F10-B2m-/-肿瘤细胞中PD-L1表达(n = 7–8)。
所有实验中均使用编码白蛋白的mRNA和同种型单克隆抗体作为对照。
均值作为汇总统计数据。通过Grubb’s检验移除单个异常值(B)。统计显著性通过Kruskal-Wallis检验与Dunn’s事后检验(B)或单向ANOVA与Dunnett’s事后检验(C, F)确定。ns表示不显著;*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S4。
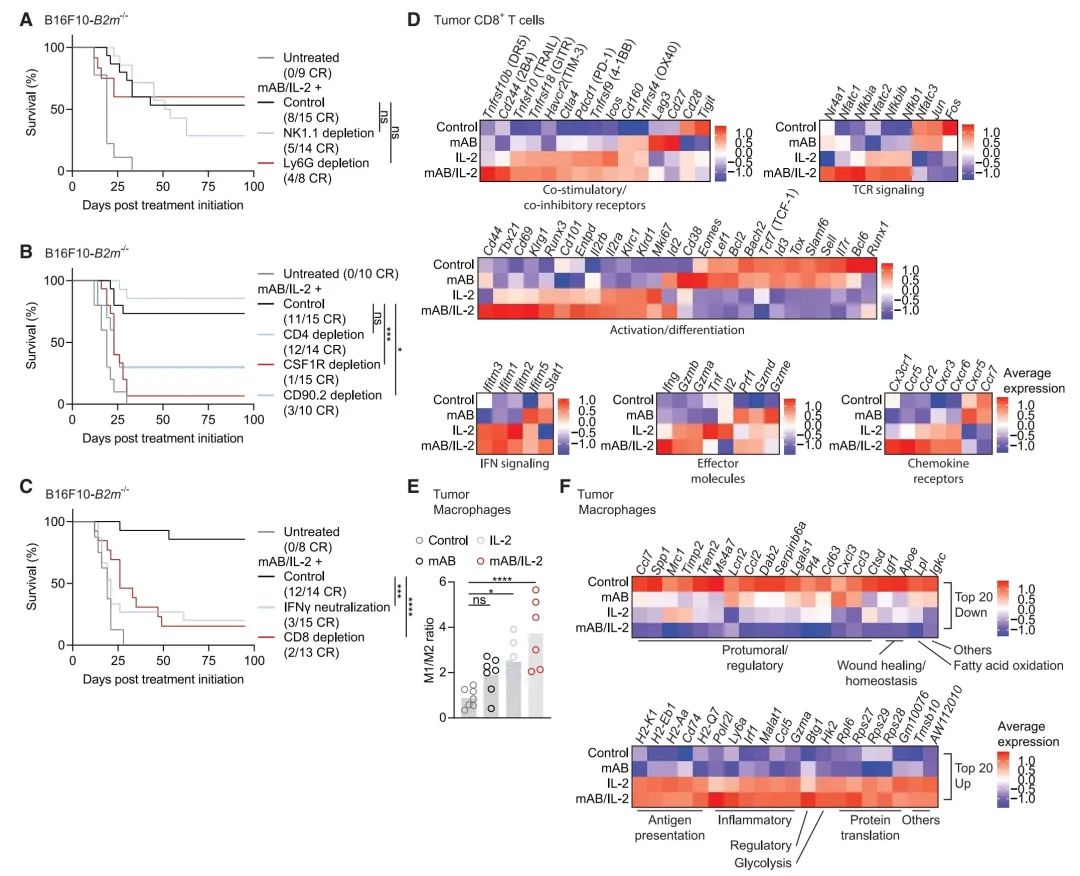
图5:CD8+ T细胞和巨噬细胞在mAB/IL-2处理的小鼠中排斥MHC I类缺失肿瘤中发挥核心作用
(A–C) 用αTrp1单克隆抗体和IL-2治疗携带B16F10-B2m-/-肿瘤的小鼠,并消耗特定免疫细胞亚群后的存活情况。对NK1.1和Ly6G(A;n = 8–15)、CD4、CSF1R和CD90.2(B;n = 10–15)或IFNα和CD8(C;n = 8–15)进行了消耗/中和单克隆抗体注射。对照组注射了无关的单克隆抗体。CR表示完全缓解。
(D) 经αTrp1单克隆抗体和IL-2联合治疗或其中任一治疗后,从B16F10-B2m-/-肿瘤中分离出的CD8+ TILs中选定基因的表达情况,通过单细胞RNA测序(scRNA-seq)确定(每组n = 3汇总)。治疗于接种后9天开始,分析于接种后第20天进行。
(E) 用流式细胞术测量,治疗后B16F10-B2m-/-肿瘤中渗透的巨噬细胞的M1/M2比例,治疗包括αTrp1单克隆抗体和IL-2联合或其中任一治疗处理。治疗于接种后9天开始,分析于接种后第20天进行。
(F) 热图显示了接种后第20天,通过单细胞RNA测序(scRNA-seq)测量的B16F10-B2m-/-肿瘤中巨噬细胞中前20上调和前20下调基因的表达(每组n = 3汇总)。治疗于接种后9天开始,包括αTrp1单克隆抗体和IL-2 mRNA或其中任一单一化合物。
所有实验中均使用编码白蛋白的mRNA和同种型单克隆抗体作为对照。
均值作为汇总统计数据。通过Grubb’s检验移除单个异常值(E)。统计显著性通过对数秩检验(A至C)或单向ANOVA配合Dunnett’s事后检验(E)确定。ns表示不显著;*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S5和S6。
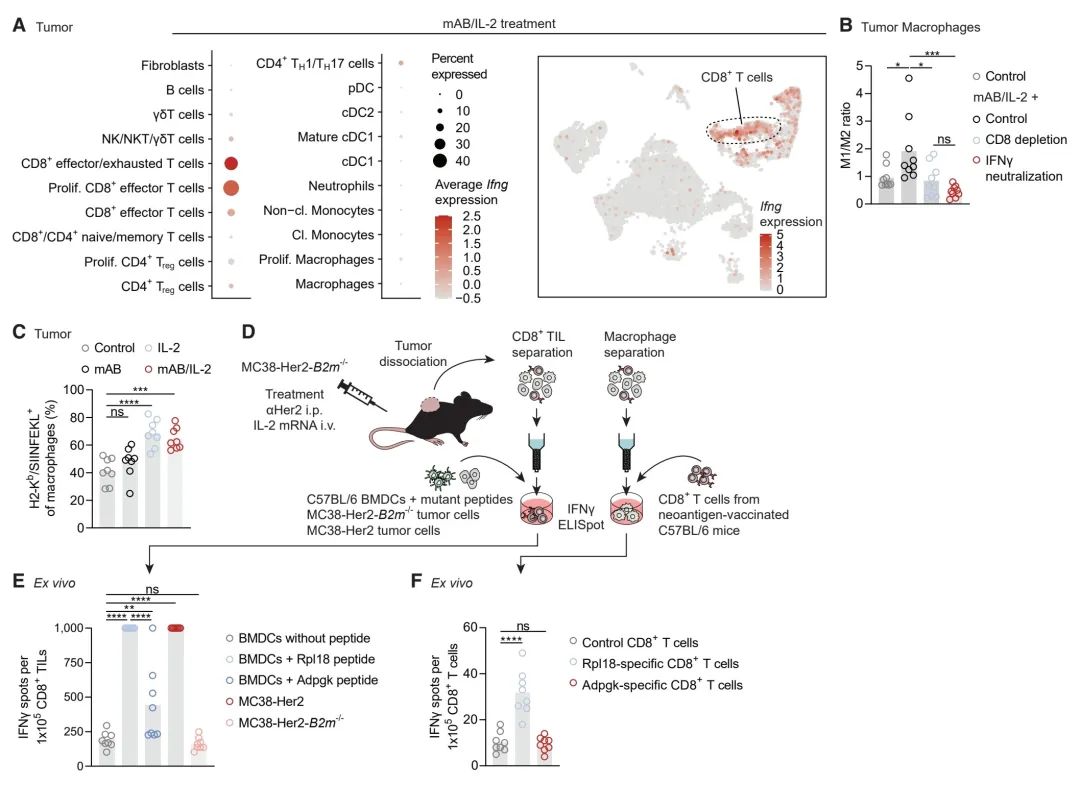
图6:IL-2激活的CD8+ T细胞和呈递肿瘤新抗原的巨噬细胞进行特异性交流
(A) 点图(左)和特征图(右)展示了mAB/IL-2处理的B16F10-B2m-/-肿瘤浸润免疫细胞的所有细胞簇中Ifng表达情况,这是通过单细胞RNA测序(scRNA-seq)确定的(每组n = 3汇总)。治疗在接种后9天开始,分析在接种后第20天进行。
(B) 通过流式细胞术测量,在接种后9天开始治疗并在接种后第18天进行分析的mAB/IL-2处理小鼠中,注射针对CD8或IFNγ或无关对照单克隆抗体后,B16F10-B2m-/-肿瘤浸润巨噬细胞的M1/M2比例(n = 9–10)。
(C) 在接种后第15天进行单次αTrp1单克隆抗体和IL-2或其中任一治疗3天后,通过流式细胞术量化测定浸润B16F10-Ova-B2m-/-肿瘤的巨噬细胞上H2-Kb/SIINFEKL复合物的数量(n = 8)。编码白蛋白的mRNA和同种型单克隆抗体作为对照。
(D) 实验示意图,分析从携带MC38-Her2-B2m-/-肿瘤的小鼠中分离出的巨噬细胞呈递新抗原的能力,这些小鼠在接种后第20天被分析。治疗在接种后第9天开始,使用αHer2单克隆抗体和IL-2联合或其中任一种进行处理。
(E) CD8+ TILs与BMDCs单独共培养或在新抗原肽段或指定肿瘤细胞系存在下共培养的IFNγ ELISpot检测(n = 8)。
(F) 从肿瘤组织中分离出的巨噬细胞与接种空载体、Rpl18-或Adpgk编码RNA-LPX的小鼠的CD8+ T细胞共培养的IFNγ ELISpot检测(n = 8)。
均值作为汇总统计数据。通过Grubb’s检验移除单个异常值(B)。统计显著性通过单向ANOVA配合Dunnett’s事后检验确定。ns表示不显著;*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S6。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab