40.1 治疗恶性疾病的T细胞疗法
细胞毒性CD8 T细胞不仅在抵御多种传染病中发挥关键作用,近年来的研究表明,它们同样可以有效清除肿瘤细胞。癌症免疫反应的核心在于表达肿瘤特异性T细胞受体(TCR)的T细胞,这些T细胞能够精准识别并摧毁恶性细胞。免疫疗法的目标是高度特异性地激活机体的免疫细胞,与肿瘤细胞展开战斗。
近年来,这种策略在癌症治疗中取得了显著的临床成功,几种基于T细胞的疗法被成功应用于患者。首先,主动免疫(或治疗性疫苗)旨在诱导和增强免疫反应,通过破坏肿瘤细胞并阻止肿瘤进展来实现治疗效果。这类策略依赖于对特定癌症表达的肿瘤相关抗原的理解,通常通过肽、蛋白质疫苗或病毒载体与基因载体的方式来递送抗原。
其次,被动免疫(或过继性细胞转移)通过从癌症患者体内分离自体外周血单个核细胞(PBMCs)或肿瘤浸润淋巴细胞(TILs),在体外进行扩增和筛选肿瘤反应性细胞,然后将这些细胞回输至患者体内。在细胞回输前,基因改造T细胞,例如插入TCR或嵌合抗原受体(CARs),可以显著提高治疗效果。
最后,免疫调节可以通过靶向抑制T细胞功能的共抑制受体实现。例如,单克隆抗体Ipilimumab(Yervoy®)能够阻断T细胞表面的CTLA-4抑制性受体,在临床上显著改善了转移性黑色素瘤患者的预后。最近,抗PD-1抗体或其配体PD-L1抗体,单独或与Ipilimumab联合使用,已在黑色素瘤、肾癌和肺癌患者中显示出显著的临床益处。
总的来说,这些进展表明,T细胞在对抗恶性细胞的免疫反应中扮演了关键且持久的角色。现阶段,确定哪些T细胞特性对于实现临床疗效至关重要尤为关键。在本章中,我们将特别关注TCR与pMHC结合的相互作用,这被认为是T细胞介导保护性免疫反应的关键参数,并回顾评估这种相互作用的不同技术手段,从而帮助识别最具功能相关性的T细胞。
40.2 定义T细胞功能活性及TCR结合亲和力和亲和度
T细胞功能亲和力已多次被证明与T细胞的保护效应相关,是衡量T细胞识别同源抗原能力的关键生物学指标。通过体外定量评估,T细胞在逐渐增加的抗原肽剂量下的功能反应(如细胞毒性活性、IFN-γ产生或增殖)可以被测量,并通过诱导半数最大反应的肽浓度(EC50)来进行量化(见Fig 40.1a)。
20多年前,Speiser及其同事开创性地证明了低功能亲和力的T细胞虽然可以在体外促进增殖或细胞毒性,但在体内对病毒感染的反应中表现不足。与此相对应,目前的共识是,具有更高功能亲和力的CD8 T细胞在控制病毒复制和肿瘤生长方面比亲和力较低的T细胞更为有效。然而,T细胞功能亲和力的体外评估仍然是技术上耗时且复杂的过程。此外,由于生物/功能指标的固有变异性,它也不适合标准化,因此在体外,通常仅限于使用固定刺激剂量进行检测,且缺乏对T细胞评估的通用标准。
基于这些考虑,改善对T细胞功能与临床疗效的不同贡献的理解,并识别额外的基于T细胞的参数,以克服功能检测的局限性,已成为当务之急。
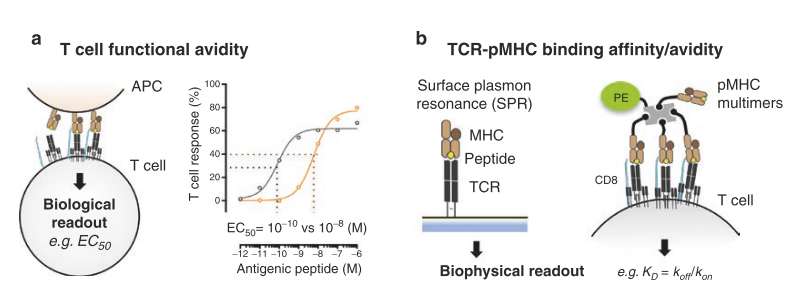
Fig. 40.1 定义和评估T细胞功能亲和力及TCR-pMHC结合亲和力/亲合度
(a) T细胞功能亲和力是反映T细胞对抗原特异性刺激的反应性的生物学指标,评估方式是通过定量暴露于滴定剂量的抗原肽下的T细胞反应(如细胞毒性活性、IFN-γ产生或增殖)。其中,EC50是定义为产生半数最大反应的肽浓度。
(b) TCR-pMHC结合亲和力与亲合度则是描述TCR与抗原之间的单体或多聚体结合强度的生物物理学指标,通常通过表面等离子体共振(SPR)或pMHC多价结合试剂来测量。
CD8 T细胞的功能亲和力主要由TCR与MHC-I类分子所呈递的抗原肽(即pMHC)的结合强度及其动力学相互作用决定。值得注意的是,这种相互作用的结合强度和动力学属性是影响T细胞生物学几乎所有方面的关键参数,包括胸腺选择和功能有效性。这些属性可能为评估T细胞反应质量提供更有价值的指标。
然而,由于技术限制,目前很少能在研究或患者的免疫监测中确定TCR-pMHC结合亲和力或动力学,即使在选择用于过继性细胞治疗的肿瘤浸润T细胞时,这一参数也常被忽视。TCR-pMHC的结合相互作用可以通过亲和力或亲和度来测量(见Fig 40.1b),这两者都能直接影响T细胞的整体功能反应。
TCR结合亲和力是指单个TCR与单个pMHC复合物结合的物理强度,通常通过表面等离子共振(SPR)来测量。相反,在细胞环境中评估时,TCR亲和度则描述了TCR-pMHC相互作用的结合强度,包含了共受体(如CD8)的贡献,通常使用重组可溶性pMHC多聚体进行估计。
TCR-pMHC结合的亲和力/亲和度与解离平衡常数KD成反比,KD定义为在平衡状态下,解离速率(koff)与结合速率(kon)的比值。
40.3 低结合亲和力/亲和度的TCR介导的肿瘤特异性T细胞反应
外周T细胞库的多样性通过胸腺发育期间TCRα和β链的随机体细胞基因片段重排来实现。随后,T细胞库通过胸腺内的正选择事件得以塑造,从而生成能够与宿主pMHC复合物相互作用的外周T细胞库。然而,为了限制自身反应性T细胞的发育和激活,那些表现出高亲和力/亲和度的TCR与自身pMHC结合的T细胞会通过中枢耐受机制(即负选择)和/或外周耐受机制被删除或失活。因此,现在的普遍观点是,针对自身和非自身抗原的外周T细胞库在TCR-pMHC结合亲和力/亲和度方面存在巨大差异(见Fig 40.2)。
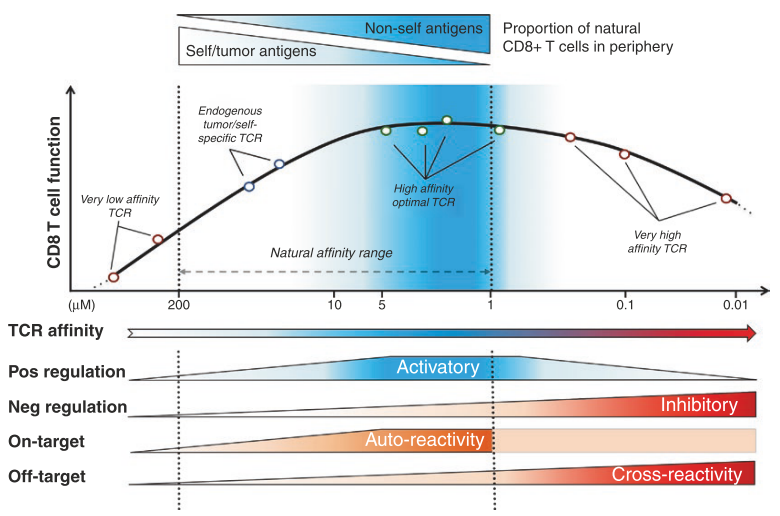
Fig. 40.2 整合T细胞功能、TCR亲和力及调节细胞反应的正/负调节因子的关系模型
我们评估了一组通过基因工程改造的CD8 T淋巴细胞的功能能力(y轴),这些细胞表达了对HLA-A2/NY-ESO-1表位具有递增亲和力的抗肿瘤TCR。结果表明,TCR-pMHC亲和力的最佳窗口位于自然范围的上限(KD为5~1 μM),这一范围与大多数外周非自身/病毒特异性T细胞的亲和力相对应。我们最近发现,T细胞功能的正调节因子(如CD28和TNFR辅因子)在具有最佳亲和力的T细胞中富集,而抑制性受体PD-1及其下游的SHP-1磷酸酶则参与限制超生理亲和力的TCR工程化CD8 T细胞的激活和反应。
研究还表明,靶向毒性遵循CD8 T细胞的功能和激活特征,而随着TCR-pMHC亲和力的增加,特别是在超自然亲和力范围内,会出现脱靶反应和毒性。
许多在癌症患者中常见的肿瘤相关抗原,如过表达抗原(例如Her2/neu、WT1或端粒酶)、分化抗原(如Melan-A/MART-1、gp100或酪氨酸酶)、癌胚抗原(如AFP或CEA)以及肿瘤特异性抗原(如NY-ESO-1或MAGEs),并不是真正意义上的癌症特异性抗原,因为它们也会在健康组织中表达。因此,针对自身/肿瘤抗原的天然T细胞库,通常表达的是具有相对低亲和力/亲和度的TCR,而高亲和力的T细胞极为罕见,因为这些细胞会通过中枢耐受机制和/或外周耐受机制被消除。
Aleksic等人的研究表明,这些TCR-pMHC相互作用的KD值通常在200μM到10μM之间(平均约为100μM),而病毒特异性TCR的KD相互作用范围为1μM(平均约为10μM)。尽管如此,这些耐受机制依然保留了对自身/肿瘤抗原产生相对较低的TCR-pMHC结合亲和力/亲和度的T细胞。因此,尽管癌症患者体内可能存在大量的自身/肿瘤特异性T细胞,但它们的TCR亲和力/亲和度往往过低,不足以介导有效的抗肿瘤免疫反应。
因此,在癌症免疫治疗的背景下,提升肿瘤特异性T细胞的TCR-pMHC亲和力和/或亲和度显得尤为重要。
40.4 优化TCR-pMHC与癌细胞的结合亲和力/亲和度
TCR工程化T细胞的过继性转移是一种近年来发展的免疫治疗手段,旨在增强针对免疫原性较差肿瘤的免疫反应。该策略依赖于优化TCR序列,以提高其与同源肿瘤抗原的亲和力/亲和度,并将这些工程化T细胞通过过继性细胞转移回输给患者。实际上,工程化T细胞的过继转移显著增强了肿瘤抗原反应性CD8 T细胞的功能和保护能力。
近年来,我们通过基于结构的合理设计,开发了一组独特的人类CD8 T细胞,这些T细胞经过工程化处理,表达逐渐增加亲和力的TCR,针对HLA-A2背景下呈现的肿瘤抗原NY-ESO-1。研究结果表明,表达上限自然范围内亲和力(KD为5到1μM)的TCR的T细胞,与表达中等亲和力的野生型TCR(KD为21.4μM)或极低亲和力TCR(KD>100μM)的T细胞相比,展现出更强的生物学反应性(见Fig 40.2)。
首先,我们观察到,在表达高亲和力TCR的T细胞中,抑制性受体PD-1的表达更为显著,且在阻断PD-1配体PD-L1后,这些T细胞的功能得以恢复。其次,随着TCR亲和力的增加,我们还发现SHP-1磷酸酶在CD8 T细胞中逐渐上调。因此,药理学抑制SHP-1能够进一步提高这些工程化T细胞的功能,具体效果取决于它们的TCR结合亲和力。
我们的观察结果与其他研究(基于小鼠和人类模型)非常一致,并提供了有力的证据,表明T细胞的激活与信号传导在TCR-pMHC相互作用达到某一亲和力阈值时增强,但如果超过此阈值,T细胞的功能可能会受到抑制,无法继续发挥有效作用。
一些临床试验已经证实了TCR-pMHC结合参数对治疗效果的重要性(见Table 40.1)。早期研究表明,与低亲和力的T细胞相比,高亲和力的肿瘤特异性T细胞反应通常与自身免疫反应相关。在一项针对黑色素瘤的临床试验中,患者接受了亲和性优化TCR转导的自体血液单核细胞治疗,靶向分化肿瘤抗原Melan-A/MART-1(见Table 40.1)。与天然的低TCR亲和力(DMF4)相比,具有更高结合亲和力的DMF5 TCR在临床上表现出更好的疗效。
然而,值得注意的是,表达更多自身/肿瘤特异性TCR的T细胞也可能会靶向正常组织中表达同源抗原的细胞(如皮肤、眼睛和耳朵中的黑色素细胞,它们表达Melan-A和gp100),从而在患者体内引发有害的细胞毒性免疫反应。类似的靶向反应也在使用针对癌胚抗原(CEA)的TCR治疗难治性转移性结肠癌患者中观察到,虽然这些患者的血清CEA水平有所下降,但也伴随出现了严重的短暂性炎性结肠炎。
有趣的是,基于A*0201/NY-ESO-1癌睾丸抗原模型的研究表明,基因优化T细胞能够产生显著的功能反应,导致客观的临床反应,且未观察到明显的体内交叉反应性或严重不良事件。这些看似矛盾的结果可以通过抗原分布的差异来解释:NY-ESO-1抗原仅在睾丸细胞中表达,而Melan-A或CEA抗原广泛存在于正常黑色素细胞或胃肠道上皮细胞中。因此,在过继细胞转移中优化T细胞的抗原特异性选择对于提升疗效、避免副作用至关重要。
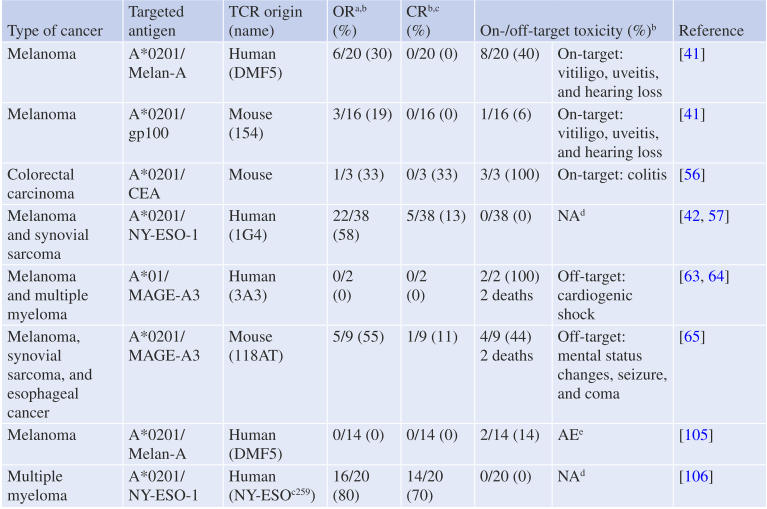
Table 40.1 使用TCR结合亲和力/亲合力优化的T细胞进行的临床试验
a. 根据实体瘤疗效评价标准(RECIST)或骨髓瘤评估的国际统一疗效标准得出的客观缓解(OR),包括部分或完全缓解。
b. 应答患者数/总患者数(应答百分比)。
c. 根据实体瘤疗效评价标准(RECIST)或国际骨髓瘤工作组(IMWG)的标准,CR表示完全缓解或接近完全缓解。
d. NA:不适用。
e. 与输入T细胞的开/脱靶毒性无关的不良事件。
另一个重要的参数是自肽交叉反应性增加的风险,这可能导致脱靶毒性。实验模型已经证明,TCR与pMHC复合物结合的T细胞在活性极高的情况下,可能会失去抗原特异性,并产生交叉反应。同样,近期的临床试验显示,亲和力增强的TCR如果超过某个阈值,可能导致患者出现严重的脱靶副作用。
例如,接受TCR治疗的患者对睾丸癌HLA-A1/MAGE-A3肿瘤抗原的增强亲和力,导致T细胞对心肌特异性蛋白Titin产生脱靶识别,进而引发严重不良反应(SAE)和对心脏组织的致命毒性。此外,两名输注了自体抗HLA-A2/MAGE-A3 TCR工程T细胞的患者出现了神经毒性,伴随精神变化,最终导致死亡。这被认为是由于TCR对人脑中表达的MAGE-A12自身抗原的交叉反应所致。
这些结果不仅证明了亲和改良TCR在体内具有强大的抗肿瘤效应,也强调了其潜在的安全性问题(见Table 40.1)。因此,我们和其他研究者提出,改良的自身特异性TCR的设计不应超过天然TCR亲和力的范围,以确保最佳T细胞功能,并避免不可预测的交叉反应性风险(见Fig 40.2)。为此,更好的临床前评估是迫切需要的,以评估工程化TCR的精确抗原特异性,并确定与亲和力改良TCR过继细胞转移最合适的肿瘤抗原。
重要的是,优化TCR亲和力的过程中,必须评估T细胞的最佳反应性,并确保不会因为自身反应性而引发靶向和脱靶副作用,从而保证TCR工程T细胞在未来临床试验中的安全性。在这方面,需要开发新的策略,以识别和选择那些自然发生但罕见的自身/肿瘤抗原特异性T淋巴细胞。这些细胞在生理TCR亲和力范围内表现出最高的TCR结合活性和功能,将在后续进一步描述。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 何丽娜
图文排版 | 赵栩 麦思淋
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab