40.5 TCR-pMHC的结合及动力学测量
为了详细表征TCR-pMHC结合的亲和力/亲合力,并解析这种分子相互作用的结合速率和解离速率的动力学贡献,已经采用了几种技术。在本节中,我们将总结目前使用的不同方法,并重点介绍它们各自的优缺点。
早期的晶体学分析表明,TCR-pMHC结构与T细胞功能之间缺乏显著相关性,这提示T细胞的激活依赖于动态过程。因此,主要使用表面等离子体共振(SPR)生物传感器对TCR-pMHC相互作用的动力学和结合参数进行定量测量。这种技术允许同时检测结合速率和解离速率,以及分子亲和度(1/KD),从而提供所谓的“3D亲和度”参数。具体来说,SPR测量中一个分子在溶液中流过传感器芯片,而另一个潜在的相互作用目标则固定在芯片上(见Fig 40.1b)。
从SPR研究收集的数据表明,与其他生物分子相互作用相比,天然人类TCR-pMHC相互作用的亲和力较弱(KD范围为500 μM至1 μM),表现为解离速率快、结合速率慢。然而,SPR技术的一个固有缺点是,它需要耗时费力地生产可溶性TCR和pMHC分子,并且忽略了CD8共受体及其他膜分子对TCR-pMHC相互作用的结合贡献。
最近,新一代技术如耦合显微镜的SPR亲和测量,以及石英晶体微平衡(QCM)生物传感器,已经被设计用于直接在活细胞表面检测膜蛋白之间的实时相互作用和动力学。这些新技术有望用于研究活体自身/肿瘤抗原特异性T细胞表面低亲和力的TCR-pMHC相互作用。
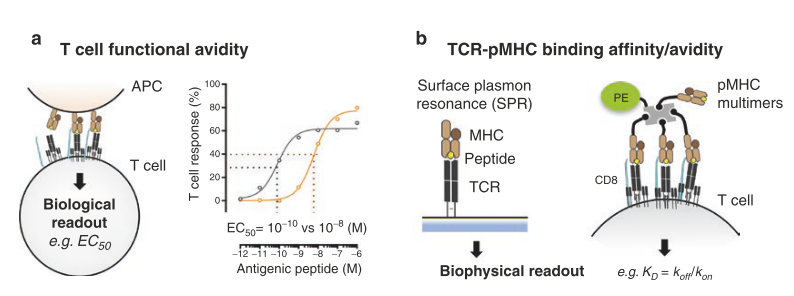
Fig. 40.1定义和评估T细胞功能亲和力与TCR-pMHC结合亲和力/亲合力
(a) T细胞功能亲和力反映T细胞对抗原特异性刺激的反应性,评估方式为T细胞在暴露于滴定剂量抗原肽时的功能反应(如细胞毒性活性、IFN-γ产生或增殖)。EC50定义为产生半最大反应的肽浓度。
(b) TCR-pMHC结合亲和力和亲合力描述的是TCR与其抗原之间单体/多聚体结合相互作用强度的生物物理读数,通常使用SPR和pMHC多价结合试剂来测量。
除了SPR技术之外,近年来还开发了其他基于机械或荧光分析的技术,这些技术可以直接在活T细胞与替代抗原呈递细胞(APC)之间,或T细胞与支撑的平面脂质双分子层之间,推断出kon和koff动力学。因此,这些基于表面的膜相互作用被称为“二维相互作用”。2D分析显示出与T细胞活化和功能有很好的相关性,但其kon和koff动力学要比3D SPR技术更快。尽管2D方法允许以更接近生理条件的方式测量TCR-pMHC结合参数,但两种方法应被视为高度互补。
事实上,2D分析需要专门设备且较为耗时,这妨碍了对活抗原特异性T细胞的快速和高通量筛选,而这种筛选可能对过继细胞免疫治疗具有重要意义。值得注意的是,最近的一项研究成功测量了单细胞2D TCR亲和力,并直接从人原代CD8 T细胞中进行TCR测序,为快速选择个体治疗性TCR以用于过继细胞转移免疫治疗铺平了道路。
随着可逆多聚体的开发,技术上实现了显著的进步。可逆多聚体在结构上类似于传统多聚体,但它们的设计特点是,当加入刺激物时,pMHC单体可以从多聚体支架上释放出来。可逆链体由荧光支架分子(StrepTactin)与多个携带链标签(streptag)的pMHC单体偶联组成。由于D-生物素与StrepTactin的结合亲和力高于streptag,它能够竞争结合位点,破坏多聚体复合物并在细胞表面释放pMHC单体。由于pMHC单体不能稳定结合TCR,它们可以迅速与TCR分离,从而识别并分离真正“未接触”的抗原特异性CD8 T细胞,同时保留其表型和功能状态。
基于类似原理的另一种可逆多聚体被称为NTAmers,它由带有his标签的pMHC与携带工程化硝基三乙酸(NTA)连接子的荧光亲和素连接(见Fig 40.3a)。在加入低浓度且无毒的咪唑后,NTA复合物迅速解体为pMHC单体,从而允许通过FACS分选抗原特异性CD8 T细胞,而不会对细胞完整性造成不良影响,如活化诱导的细胞死亡。
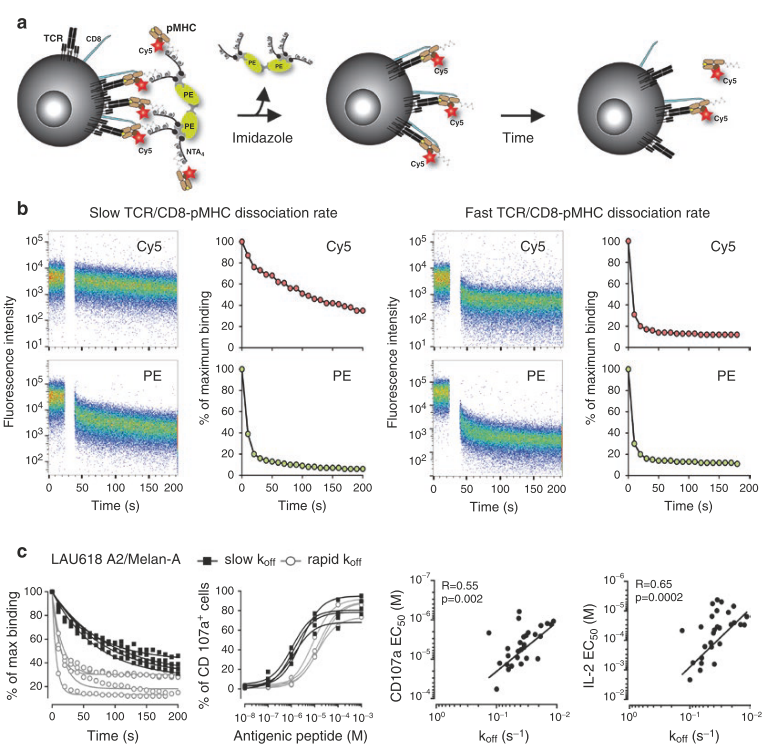
Fig. 40.3 基于NTAmers的单体解离分析用于鉴定具有更高TCR-pMHC亲和力和功能效力的抗肿瘤T细胞
(a) 基于NTAmers的单体解离分析示意图。CD8 T细胞通过NTAmers进行稳定染色,NTAmers由链霉亲和素-PE(绿色)-NTA4(灰色)和含有Cy5标记的β2m(红色)的肽-MHC(棕色)单体组成。加入咪唑后,NTAmers迅速在Cy5标记的pMHC单体中解体(中间图)。根据固有的TCR/CD8-pMHC解离速率(koff)(右图),Cy5标记的pMHC单体随后从与细胞相关的TCR(黑色)和CD8(蓝色)解离。
(b) 代表性NTAmers解离染色及其相应的拟合曲线。从CD8 T细胞克隆获得的染色数据在左图中展示,而右图为相应的拟合曲线,定义为TCR-pMHC解离速率(koff)的快或慢。在1分钟基线记录(白色间隙)后,加入咪唑,通过流式细胞术观察随时间推移的Cy5(pMHC单体)和PE(NTA4支架)信号的解离曲线。相应的单体解离速率(koff)通过Prism(GraphPad软件)进行分析。
(c) TCR-pMHC结合亲和力与T细胞功能亲和力的关系。从一名黑色素瘤患者(LAU618)中分离出的HLA-A2/Melan-A特异性CD8 T细胞克隆,根据解离速率(koff)分为快(白色圆圈)和慢(黑色方块)两类。在左图中展示了基于NTAmers的单体解离曲线,第二图展示了基于CD107a的滴定曲线。第三、四图分别展示了TCR-pMHC亲合力(单体TCR-pMHC koff)与功能亲合力(CD107a脱颗粒EC50和IL-2产生EC50)之间的相关性(以Spearman系数r和P值表示)。
由于荧光标记了可逆多聚体复合物中的单个pMHC单体,最近的技术可以直接监测并定量分析抗原特异性T细胞表面的pMHC单体与TCR的解离情况。通过基于实时显微镜的策略,可逆双色链体成功地用于测定人类和小鼠T细胞上非自身病毒特异性TCR的单体解离动力学。
具体而言,Nauerth及其同事报道,与半衰期较短(高koff)的T细胞相比,具有较长半衰期(低koff)的病毒特异性CD8 T细胞展现出更高的功能亲和力和更强的体内保护能力。此外,Streptamer技术的优势在于,它能够同时检测数百个抗原特异性CD8 T细胞上的koff值,不受限于克隆性T细胞群的产生。然而,Streptamer解体为单体pMHC分子所需的显著延迟时间(约60秒)以及与显微镜检测相关的光漂白效应,限制了快速TCR-pMHC脱靶率的检测,而脱靶率通常在低亲和力的自身/肿瘤特异性CD8 T细胞中发现。
最近,基于Streptamer的实验进一步优化,使得通过常规流式细胞仪测量体外未分选的多克隆抗原特异性CD8 T细胞的koff值成为可能,这为高通量应用打开了大门。
同时,作者的团队使用了可逆NTAmer的双色版本,通过流式细胞仪直接评估活体CD8 T细胞上的TCR-pMHC解离动力学(见Fig 40.3a, b)。NTAmer方法的准确性得到了验证,研究发现基于NTAmer的单体解离率与SPR测量结果之间具有高度相关性。与Streptamer技术相比,NTAmer支架的降解速度更快(2-3秒),这使得对广谱TCR亲和力解离动力学的精确分析成为可能,尤其是针对自身/肿瘤特异性CD8 T细胞的解离动力学,它们通常表现出低亲和力和快速koff(见Fig 40.3c)。
总而言之,双色可逆多聚体技术(即Streptamer和NTAmer)能够在大量非自身/病毒和自身/肿瘤抗原特异性CD8 T细胞克隆内,直接在活体原代CD8 T细胞表面实时定量单体TCR-pMHC解离动力学。然而,当前仍未出现基于单体pMHC的检测方法,能够直接对活体T细胞上的kon关联动力学或KD亲和力进行精确测量。
40.6 TCR-pMHC结合参数与CD8 T细胞效力之间的关系
TCR与抗原之间的有效相互作用是成功启动和发展适应性免疫应答的关键。然而,目前对内源性TCR-pMHC结合参数的大规模评估仍然具有技术挑战性,这限制了我们对TCR-pMHC亲和力/亲合力在天然自身/肿瘤特异性CD8 T细胞应答中的影响和临床相关性的了解。特别是,尚不清楚高TCR-pMHC亲和力/亲合力的T细胞是否存在于癌症患者的内源性肿瘤特异性库中,以及TCR-pMHC亲和力/亲合力参数是否是强大抗肿瘤T细胞反应的决定性因素,仍然是一个开放的问题。
在过去的20年中,许多研究通过使用实验性改变的肽配体或亲和力优化的TCR变异体,来阐明TCR-pMHC结合参数与CD8 T细胞功能之间的关联机制。这些研究表明,在生理相互作用范围内(KD 200 μM – 1 μM),TCR-pMHC亲和力(由SPR确定)与T细胞功能亲和力密切相关。功能指标包括T细胞与靶细胞结合的潜能、TCR信号复合体下游分子的磷酸化、细胞内Ca²⁺动员、裂解颗粒极化、靶细胞杀伤、细胞因子产生、细胞增殖、多功能性,以及体内肿瘤浸润和保护/生存能力。
总之,这些研究为根据TCR-pMHC结合参数调控肿瘤特异性T细胞功能效力提供了有力证据。然而,这些人工模型可能绕过了许多其他分子和细胞参数,这些参数可能会削弱TCR-pMHC亲和力对总体T细胞功能的影响。因此,TCR-pMHC亲和力/亲合力是否是天然抗肿瘤CD8 T细胞应答的决定性因素,仍有待进一步验证。
通过使用新型NTAmer技术,我们团队最近分析了TCR-pMHC结合参数(即koff或解离速率)在癌症患者自发或治疗诱导的肿瘤特异性T细胞应答中的作用。我们从黑色素瘤患者中分离出大量Melan-A和NY-ESO-1特异性CD8 T细胞克隆,发现TCR-pMHC解离速率与功能亲和力密切相关。具有较长半衰期(缓慢koff)的肿瘤特异性T细胞克隆表现出更强的靶细胞杀伤能力。更重要的是,这些相关性与所使用的功能性读数无关(如Th1/Th2相关细胞因子产生、多功能性或增殖),表明TCR配体解离速率是CD8 T细胞效能的可靠预测指标(见Fig 40.3c)。
此外,我们的结果表明,NTAmers是一种有效工具,能够从癌症患者的内源性库中分离出那些具有更高抗肿瘤效能的罕见CD8 T细胞,用于过继性细胞治疗。
最后,通过使用基于NTAmer的技术,我们还能够量化黑色素瘤患者在免疫治疗中的反应效果。事实上,我们发现,疫苗接种所用的肽类型对肿瘤特异性T细胞的TCR-pMHC结合亲和力有着显著影响,进而影响T细胞功能。与接种Melan-A26-35 A27L类似物肽相比,重复接种天然Melan-A26-35肽的患者产生了更高TCR-pMHC亲和力和更强杀伤效力的肿瘤特异性CD8 T细胞。尽管A27L肽与MHC的结合更强更稳定,但使用MHC结合较弱/天然肽进行疫苗接种,有助于富集高功能活性T细胞。
因此,评估TCR-pMHC结合活性能够帮助我们在比较实验中确定哪种治疗性疫苗方案能够触发最有效的肿瘤特异性T细胞反应,为未来癌症疫苗的肽选择提供宝贵的见解。
40.7 结论
近年来,随着抗CTLA-4抗体和抗PD-1抗体等新型治疗试剂的问世,肿瘤免疫治疗取得了显著进展。然而,我们仍然迫切需要一种可靠的技术,能够快速鉴定和分离癌症患者体内自身/肿瘤抗原特异性CD8 T细胞,这些细胞在自然库中具有最高的TCR-pMHC亲和力。
目前,科学界正在努力设计新的技术,以实现对TCR-pMHC结合亲和力及其在单细胞水平上的动力学速率进行快速且高通量的评估。理想情况下,这种技术能够保留活细胞,以便进一步进行扩增、功能表征,并平行克隆其TCRα链和β链,从而为过继性T细胞转移治疗提供基础。
优化的流式细胞术方法将使基于动力学或亲和力参数的单细胞分选成为可能。同时,新的显微成像技术、微平衡技术和等离子共振装置也有望在不久的将来实现这些目标。
通过更好地理解免疫保护的相关性,并开发出能够选择出最佳肿瘤特异性CD8 T细胞(即高亲和力和高功能)的新技术,我们有望推动基于T细胞的抗癌疗法的进一步发展。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 何丽娜
图文排版 | 赵栩 麦思淋
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab