41.1 简介
癌症患者的免疫反应涉及免疫细胞和可溶性因子,这些反应可以通过越来越多的实验室技术来进行测量,通常与生物信息学数据处理和解释相结合。这种过程被称为免疫监测。相比传统的临床评估工具和结果衡量标准,免疫监测能够更直接、更快速地跟踪疾病的演变及其对治疗的反应。为了为癌症患者提供最优的临床护理,这些工具和标准被充分利用。
免疫监测方法依赖于基于前沿技术和工程的各种手段,如细胞和分子生物学、生物化学和显微成像技术,从而大幅提高了分析的分辨率和精确度。然而,目前大多数方法尚未广泛应用于常规患者分析中,而是作为研究中的主题,不断进行优化和改进,在一定程度上也应用于临床试验。一些方法正在进行扩展验证,特别是那些有望在未来用于常规临床实践的技术。
免疫监测的主要目标是确立能够预测疾病进展或治疗反应的生物标记物,这些标记物将为未来的精准医学提供有力支持。Fig. 41.1展示了用于分析患者血液和组织标本的各种技术,而本章后续内容也将围绕这些技术展开。通过追踪癌症患者的诊断、治疗和随访过程,研究人员深入探讨了肿瘤的动态特性,从而为人类癌症的生物学提供了重要见解。
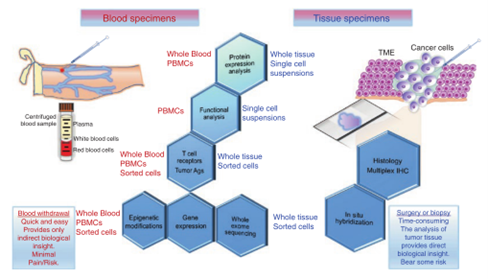
Fig. 41.1 患者血液和组织样本分析示意图:使用多种方法对血液、其他体液,以及通过手术或活组织检查获取的固体样本进行分析。
41.2 流式细胞术与蛋白质表达分析
在过去的二十年里,免疫细胞的特性逐渐成为研究和临床领域的核心内容,提供了大量关键信息。多种技术被应用于研究病人的T细胞(Fig.41.2)。近年来,这一领域的技术取得了巨大进展,帮助建立了可靠的仪器、标准化技术和方法,用于分析来自不同来源的细胞和体液,例如血液、其他体液以及包括肿瘤和淋巴组织在内的多种组织样本。由于人类样本的种类多样、细胞类型繁多,以及各种细胞因子和趋化因子的复杂性,研究人员需要采用多种不同的技术和专门程序,才能从有限的生物材料中获取最大信息量。
对免疫反应的描述和监测是开发抗癌新疗法以及评估其疗效的关键。为了有效监测和量化针对肿瘤的免疫反应,必须使用能够可靠检测和表征肿瘤抗原特异性T细胞的技术。这些技术能够提供有关T细胞表型、特异性和增殖的详细信息,甚至可以直接测量T细胞的多种功能。
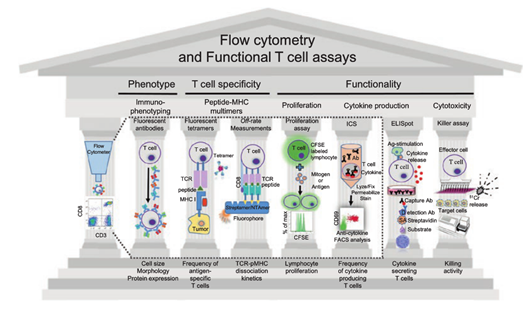
Fig. 41.2 T细胞检测概述。
该图展示了用于描述和监测T细胞反应的各种技术,能够提供有关肿瘤特异性T细胞的表型、特异性、增殖及其功能的信息。从左至右,流式细胞术可快速分析从患者血液或肿瘤微环境(TME)中分离出的单个细胞的物理特性(例如,大小)和多种分子特征。结合荧光染料的抗体被用来标记细胞膜上或细胞内的特定蛋白质。
抗原特异性T细胞可以通过荧光标记的四聚体-MHC(pMHC)与T细胞受体(TCR)的复合体来检测。除了确定T细胞的频率外,当四聚体与各种抗体结合时,也可以进一步确定T细胞的表型特征。新的技术还允许通过实时流式细胞术(使用NTAmers)和/或显微镜(使用StrepTamers)直接、精确地定量活的CD8T细胞上的TCR:pMHC解离率(KOFF)。
荧光CSFE标记常用于评估T细胞体外增殖,而细胞内细胞因子染色(ICS)是一种广泛应用的基于流式细胞术的技术,能够检测细胞在刺激后产生和积累的细胞因子,并量化产生细胞因子的T细胞的频率。在免疫监测领域,还存在一些重要的基于非细胞学的分析,例如:干扰素-γELISpot试验,这是一种高度敏感的免疫分析方法,通过检测抗原刺激后每个细胞产生的斑点,揭示肿瘤特异性淋巴细胞的频率。此外,杀伤试验用于测定淋巴细胞的细胞毒性和裂解能力,即通过标记靶细胞的裂解来测量细胞毒性T细胞的杀伤效应(如使用释放的放射性~(51)Cr测定)。
41.2.1 流式细胞术
流式细胞术是目前应用最广泛的技术之一,主要用于分析血液细胞和肿瘤微环境(TME)。自从30年前开始使用以来,这项技术已经被广泛采用。通过结合高特异性、荧光标记抗体,流式细胞术能够从几微升的血液中识别出多种不同的细胞类型,例如T细胞、B细胞、NK细胞、树突状细胞(DC)以及单核细胞。
这项技术不仅可以列举不同细胞类型的频率,还可以进一步确定细胞的激活状态和分化阶段,甚至通过高度特定的细胞亚群来识别它们所表达的受体类型。例如,研究发现,T细胞中CCR7和CD45RA的表面受体表达模式能够区分幼稚T细胞(CD45RA+CCR7+)、记忆T细胞(CD45RA−CCR7+)和效应T细胞(CD45RA−/+CCR7−)。同时,CD27和CD28等共刺激受体的荧光标记,能够将T细胞进一步分类为不同的分化阶段(Fig. 41.3)。
现代流式细胞仪配备多个(通常为12-18个)荧光通道,使得可以同时检测许多参数,包括激活和抑制受体、细胞因子、趋化因子,以及细胞毒性的蛋白水解酶表达(Fig. 41.3)。
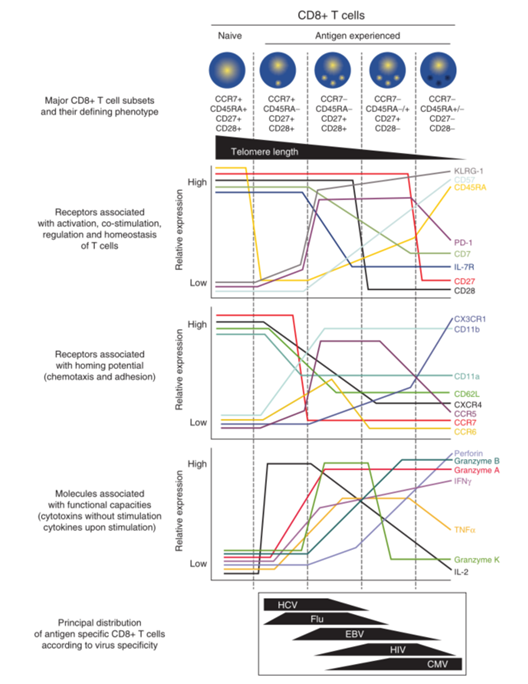
Fig. 41.3 人类CD8 T细胞亚群的表型相关性及其与功能属性的关系:根据CD27、CD28、CCR7和CD45RA的表达,定义了5种不同的循环CD8 T细胞亚群。根据文献数据,这些亚群中的细胞表面受体和细胞内分子的相对端粒长度和表达,与T细胞激活、共刺激、调节、内稳态、归巢潜力和功能能力有关。此外,还描绘了病毒感染后(如流感)或潜伏期感染阶段(如丙型肝炎病毒、EB病毒、艾滋病毒和巨细胞病毒)的病毒特异性CD8 T细胞的常见表型分布。
最常用的技术是分析外周血单个核细胞(PBMC),这些细胞通过对新鲜静脉血进行梯度离心获得。该技术的优势在于消除了红细胞和粒细胞,从而能够分析纯化的细胞群体,并且这些细胞可以等份冷冻保存,供后续进一步研究使用。然而,研究人员逐渐意识到,这种策略可能导致一些关键细胞类型的丢失,并且可能引入伪迹,导致某些细胞群体的特征发生变化,从而产生误导性的结果。因此,许多细胞类型,特别是髓系来源的抑制性细胞(MDSCs),应该通过新鲜全血进行分析。
为了在样本量小或稀有样本的情况下获得更多信息,研究人员付出了巨大的努力。一种策略是使用重金属离子标记抗体代替荧光标记,并通过质谱仪和流式细胞术结合的方法进行分析,读数由飞行时间质谱仪(CyTOF/Fluidigm)完成。另一种策略是将流式细胞术与显微镜结合使用,例如图像流机(AMNIS),这类仪器能够通过荧光标记对细胞进行分析,并同时拍摄细胞的显微照片。这种方法不仅可以显示荧光分子是否均匀分布在细胞表面,还可以确定它们是否极化在细胞的不同区域或特定隔室。事实上,由于细胞在仪器中通过的速度较慢,我们可以观察到细胞之间的相互接触,并分析其接触区域发生的分子交换。
此外,像IncuCyte(Essen BioScience)、CytoSMART(Lonza)和Operetta(Perkin Elmer)这样的实时成像系统,可以在培养条件下连续观察细胞及其体外活动。这些系统中的相机会被放置在培养箱中,在最优条件下进行数天的定时拍摄。例如,我们可以在肿瘤细胞存在的情况下,观察免疫细胞的运动或由于外部刺激导致的细胞趋化运动。
最新的技术之一是芯片细胞仪(ZellkraftWerk),它允许对悬浮细胞和固定在显微镜设备上的组织样本进行荧光显微镜分析。这项技术可以对不同细胞或同一细胞进行多次重新染色,从而获取更多信息。尽管这项技术仍在优化中,但它有望最终取代耗时的免疫组织化学(IHC)和流式细胞术。
该技术的优势在于能够对稀有的细胞表面标记物以及流式细胞仪中荧光检测的细胞内分子进行更深入的分析。
41.2.2 蛋白质阵列
另一种获取细胞不同状态信息的方式,是通过蛋白质阵列技术。这项技术允许将健康捐赠者的样本与患者在不同时间点的样本进行对比分析,通常可以通过大量材料或通过流式细胞仪或磁珠分选的不同细胞类型来实现。蛋白质阵列能够提供定性的蛋白质图谱,并且可以表征蛋白质的磷酸化状态,从而揭示细胞内的信号活动。这种技术有助于筛选出关键因素,并最终确定候选生物标记物。
41.2.3 细胞因子分析
T细胞能够分泌一种或多种细胞因子。通过酶联免疫吸附试验(ELISA),可以检测来自体外实验中不同类型细胞或直接从血液样本的血清中分泌的可溶性分子。虽然这种技术简单高效,但其灵敏度相对较低,且一次只能分析一种特定分子。近年来,开发了新的尖端技术,能够高灵敏度地检测多种细胞因子、趋化因子或其他分子。这些技术包括基于液体系统的珠粒捕获分析(如FCM、Luminex)或基于成像系统的技术,例如MSD(介观尺度发现),其中分泌的分子被捕获在特定涂层的膜上。这些技术的优势在于,它们能够从少量样本中同时检测多个分子。
41.2.4 为数据分析提供生物信息学支持
对来自多种分析方法的海量数据集进行结论性分析是一项挑战。即使严格遵守普遍确立的分析规则,流式细胞术的数据分析仍可能受到一些主观因素的影响。例如,主观的门控决策可能会显著影响结果的准确性及其解释。为了解决这一问题,使用新的专用软件程序来分析数据变得越来越重要。数学算法能够以更加公正的方式分析和比较数据集,通过结合所有不同参数,进行深入的分析。这不仅能够快速识别细胞群体,还可以发现传统门控方法可能忽略的非常规细胞。
41.3 进一步检测T细胞功能
除了流式细胞术,还有其他多种技术可以用来分析T细胞的功能。如Fig. 41.2所示,几种标准的功能性T细胞分析方法用于确定细胞毒性、细胞因子产生和增殖。
此外,能够同时检测T细胞频率和功能的分析方法,如干扰素-γ(IFN-γ)酶联免疫斑点法(ELISpot),在临床试验和基础研究中用于监测T细胞反应越来越受欢迎。
41.3.1 分析细胞介导的细胞毒作用
T细胞介导的细胞毒作用是肿瘤免疫应答的关键机制。因此,评估细胞毒性免疫反应的监测方法至关重要。评估细胞毒性T淋巴细胞(CTL)和自然杀伤细胞(NK细胞)介导的细胞毒性,最经典且常用的方法是铬(51Cr)释放试验,也称为细胞毒性试验,如Fig. 41.2所示。该方法最早由Brunner等人于1968年开发,并广泛用于检测免疫监测实验室中的杀伤活性。
该技术基于靶细胞被动内化放射性铬(51Cr),随后通过添加效应淋巴细胞裂解靶细胞,导致51Cr释放到培养上清液中,然后由伽马计数器检测。尽管已经出现了几种改进的替代方法,铬释放试验仍然被认为是测量细胞介导细胞毒性的“金标准”。
然而,这种方法存在一些缺点,促使需要开发更准确的方法:
-
灵敏度相对较低,通常需要多次刺激细胞毒性淋巴细胞才能达到可检测的裂解活性水平,这可能改变了原始T细胞群体的组成和功能。
-
该方法无法提供关于体内功能和单个效应细胞行为的直接信息。
-
单个T细胞的杀伤活性可能差异很大,在细胞毒性分析中,可能有“超级杀手”细胞占主导地位,而其他T细胞对靶细胞的杀伤贡献甚微。
-
部分靶细胞难以标记放射性铬,或表现出较高的自发释放,影响试验结果的准确性。
-
自体肿瘤细胞难以获得,替代靶细胞可能无法真实反映淋巴细胞在体内对自体肿瘤细胞的溶解能力。
-
最后,该方法的结果变异性较大,并且与放射性同位素的生物危害及其处置相关联,增加了操作复杂性。
41.3.2 检测细胞因子和干扰素产生细胞的ELISpot技术
干扰素-γ ELISpot试验是一种高度敏感的免疫分析方法,用于检测肿瘤特异性淋巴细胞的功能。它通过每个细胞形成一个斑点,揭示出能分泌干扰素-γ并对抗原刺激产生反应的细胞。这种方法特别适合于确定功能性T细胞的频率。Versteegen等人的研究首次使用ELISpot技术检测人类细胞分泌干扰素-γ。此后,通过使用硝酸纤维素膜和特异性单克隆抗体,对ELISpot技术进行了重要改进,提升了其灵敏度和重复性。自2000年第13届国际艾滋病大会推荐使用ELISpot进行免疫监测以来,它已成为细胞免疫学中最重要的直接体外检测方法之一。
在临床试验和免疫监测中,确保结果的可比性和可重复性至关重要。ELISpot分析凭借其简单的操作流程,能够准确检测从患者体内提取的T细胞,因此最能反映细胞的体内功能状态。这使得ELISpot检测成为一种标准化且经过验证的检测方法。为了减少试验间和试验内的可变性,并提高精确度和重现性,该技术的第一步是对方案、材料和试剂进行标准化,例如使用预涂覆的96孔板。
Fig. 41.2展示了ELISpot分析原理的示意图,每个斑点代表一个分泌细胞因子的单个细胞。通过ELISpot生物阅读器对这些斑点进行计数,从而计算出功能性T细胞的频率。与其他方法相比,ELISpot能够在细胞分泌后立即捕捉到细胞因子的存在,避免了因受体结合或蛋白酶降解而导致的测量误差。
ELISpot被认为是目前最灵敏的T细胞功能检测方法之一。标准的ELISpot检测方法能够检测到100,000个细胞中的1个功能T细胞,而经过改良的ELISpot技术,检测灵敏度可以达到每200,000个PBMC中的1个。这使得ELISpot在细胞数量有限的情况下尤为有用。
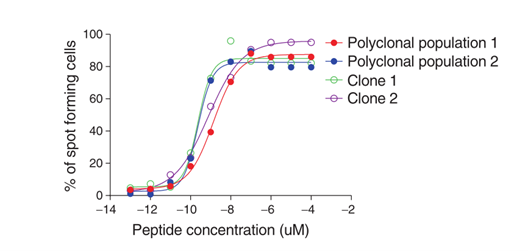
Fig. 41.4 展示了两个单克隆CD8 T细胞和两个患者的多克隆T细胞群体的ELISpot滴定曲线示例。每个微培养中包含300个抗原(Melan-A)特异性的单克隆T细胞或由300个抗原特异性细胞组成的多克隆T细胞群体。多克隆群体中抗原特异性T细胞的百分比先前通过流式细胞术使用荧光四聚体进行测定,因此能够计算出每个微培养中所需的细胞数量以获得300个抗原特异性T细胞。为了进行刺激,每个微培养都加入了20,000个T2细胞和指定浓度的抗原肽(Melan-A)。测试了10个不同浓度的多肽,每个浓度三次重复,因此共需30个微培养(使用96孔板)。每个孔中的斑点数量由ELISpot BioReader 5000计算,并使用Prism软件绘制曲线。
传统上,这种分析是通过使用单一的高浓度多肽(通常为1微摩尔)进行的。然而,使用多肽滴定可以生成S形剂量反应曲线(如Fig. 41.4),用于确定T细胞的功能亲和力。功能性活动对应于产生50%最大活性所需的多肽浓度(EC50),即达到半最大干扰素-γ ELISpot活性所需的抗原肽量。由于抗原在体内通常是限速因素,功能亲和力成为评估抗肿瘤T细胞功能效力的重要参数。
功能亲和力主要取决于T细胞表面TCR-肽-MHC的相互作用。多个因素影响这一相互作用的强度,例如TCR的聚集、CD8共受体的参与、局部黏附分子的浓度以及共激活和共抑制受体的作用,所有这些都会调节细胞间的相互作用强度,进而调节T细胞活性。功能亲和力指的是个体非共价相互作用的累积“动态强度”。
另一个重要的参数是功能亲和力的异质性,这可以通过曲线的斜率来表示,揭示T细胞对抗原反应的多样性。
41.3.3 细胞内细胞因子染色
细胞内细胞因子染色(ICS) 是流式细胞术中最受免疫学家欢迎的分析方法之一,专门用于评估复杂的T细胞反应。ICS 的一个独特优势在于,它能够同时评估多种表型、分化和功能参数,包括多种细胞因子的表达。ICS 与其他流式细胞术联合使用,如通过荧光抗体标记的细胞表面标志物或荧光MHC多聚体,从而对抗原特异性T细胞进行免疫表型鉴定,成为一种极其灵活且通用的方法。
ICS 的主要实验步骤包括:首先,使用特定的多肽或通过抗CD3抗体或有丝分裂原等非抗原特异性激活方法,来激活目标细胞。接着,加入蛋白质运输抑制剂(例如灯盏花素A),以将细胞因子保留在细胞内。随后,进行细胞的洗涤,并加入针对细胞标志物的抗体。然后,细胞会被固定(如使用多聚甲醛)并渗透,接着加入抗细胞因子抗体。最后,通过流式细胞仪对细胞进行分析(如Fig. 41.2所示)。
近年来,技术进步显著,例如多色分析,能够同时检测T细胞的五种或更多独立功能(如产生多种细胞因子和趋化因子,或检测脱颗粒作为细胞毒性的替代指标),同时还能识别多个表面标记。这些技术使ICS成为评估T细胞多功能性和免疫反应的关键工具。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 刘玉娇
图文排版 | 蔡倩薇 郑家怡
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab