19世纪90年代,纽约纪念斯隆·凯特琳癌症中心 (Memorial Sloan Kettering Cancer Center) 的一位外科医生作出了重大发现。他在一位丹毒患者身上观察到,复发性肉瘤的消退可能是由于人体感染防御系统的激活,引发了一种肿瘤排斥反应,这种反应是手术并发症导致的。
外科医生 W. Coley 决定验证这一理论。他通过将实验室培养的细菌(当时最先进的微生物学技术)直接注射到肿瘤中进行实验。令人惊讶的是,他在部分病人中观察到了完全的肿瘤反应。这些发现开启了肿瘤免疫学这一全新领域。作为免疫学的一个分支,它与癌症生物学和临床肿瘤学一起,经过了120年的发展才趋于成熟。
在过去的十年里,科学界和肿瘤学界重新激活了这一领域,尤其是在免疫检查点阻断方面取得的巨大成功,推动了这一领域的复兴。免疫治疗目前正逐渐成为继手术、化疗和放疗之后的第四大癌症治疗支柱。特别是,PD-1/PD-L1轴阻断的单克隆抗体已经成为多种肿瘤(如黑色素瘤、肺癌、肾癌、膀胱癌和霍奇金淋巴瘤)治疗的核心手段。
那么,我们从中学到了什么?我们现在知道,免疫系统通常在癌变早期能够识别肿瘤,甚至在某些情况下,直到转移阶段。研究表明,Th1定向免疫和细胞毒性T细胞浸润对预后有积极影响,而且在肿瘤微环境中发现了对突变肿瘤抗原特异性T细胞,进一步支持了这一观点。
肿瘤的进化与免疫系统的相互作用是动态的,两者之间相互影响,导致肿瘤在免疫压力下逐渐进化,形成抵抗抗肿瘤免疫的主要机制,如对IFNγ或细胞溶解淋巴细胞的耐受性。另一方面,肿瘤也可能利用先天免疫和适应性免疫的某些成分,来为其生长、迁移、侵袭和远处播散创造有利条件。
在临床表现的肿瘤中,相当一部分属于T细胞炎症型肿瘤。不同肿瘤类型之间,以及具有相似组织学的癌症患者之间,T细胞浸润的比例存在差异。多种因素可以解释这种差异,其中一个重要因素是肿瘤的固有免疫原性,尤其是那些具有高体细胞突变负荷的肿瘤,例如黑色素瘤或肺癌,这些肿瘤更可能向T细胞呈现高密度的新抗原。
然而,即便树突状细胞系统完整,尤其是在疫苗接种后进行靶向时,它们未必总能有效引发强效的肿瘤排斥反应。此外,T细胞库对肿瘤相关抗原的亲和力较低,且大多无效。用于疫苗的佐剂效力也可能不足。随着对先天免疫激活信号理解的深入,应该开发出更有效的化合物,用于下一代疫苗。
有效的疫苗不仅需要产生大量T细胞,还需选择性促进高亲和力的肿瘤抗原特异性T细胞的扩增,具备强大的多功能分化能力,同时还要诱导持久的记忆T细胞反应。这些要求构成了重大挑战。
为了解决这些问题,一方面需要基础免疫学的进一步研究,另一方面需要创新的早期临床试验。这些试验应采用适应性设计,以便能够快速测试较多变量,并结合精准的免疫监测来评估疫苗特异性免疫细胞反应。
开发有效免疫疗法面临的下一组挑战是应对免疫机制耐药性的发展。最近已经报道了首例黑色素瘤适应性耐药性的案例。除了现已获批的免疫检查点阻断剂,如抗PD-1和抗CTLA-4,肿瘤免疫学界正在积极努力,挖掘肿瘤微环境中复杂的免疫抑制机制。其中包括额外的免疫检查点,如效应T细胞上的LAG-3、VISTA和TIGIT。
此外,另一类新的免疫检查点通过外切酶降解核苷酸/核苷,生成腺苷,这是一种抑制T细胞免疫功能的分子。值得关注的是,在调节性T细胞(Treg)上表达的CD39,以及在多种免疫细胞(包括T细胞和肿瘤细胞)中表达的CD73。CD73是将AMP不可逆转地转化为腺苷的关键酶。目前,针对CD73的两种阻断单克隆抗体正在进行早期临床试验,以评估其剂量和安全性。
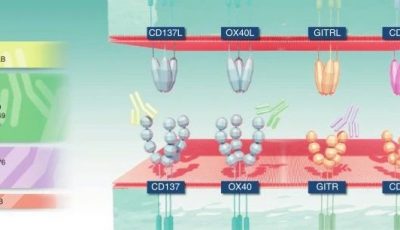
另一种补充的免疫治疗策略是通过使用激动性单克隆抗体来靶向共刺激受体。尽管CD28由于几年前Tegenero试验中的严重毒性而被排除在外,但其他一些有前景的靶标包括CD137、OX40、GITR和CD40。这些受体的早期临床试验已开展,且开发进展各有不同。
另一类潜在靶标是肿瘤微环境中多种细胞类型过度表达的酶。例如,精氨酸酶和诱导型一氧化氮合酶(iNOS)是抑制未成熟骨髓细胞浸润肿瘤的主要介质;吲哚胺氧化酶(IDO)1和2则在抗原呈递细胞中由IFNγ诱导,并在多种肿瘤中过度表达,类似的还有环氧化酶-2(COX2)。在IDO方面,其色氨酸消耗会抑制T细胞效应功能,而色氨酸降解产物犬尿氨酸则是Th17细胞AH受体的激动剂,会引发炎症细胞因子,促进肿瘤的生长和扩散。使用这些酶的特异性抑制剂在临床前模型中表现出显著的抗肿瘤作用,其中一些IDO抑制剂已经在临床开发中取得了良好进展。在不久的将来,IDO抑制剂联合免疫检查点阻断可能会成为新的联合免疫疗法。
最后,肿瘤相关巨噬细胞(TAM)和/或髓源性抑制细胞(MDSC)的重编程是另一个增强抗肿瘤免疫反应的策略。研究表明,阻断CSF-1R的单克隆抗体能够在体内产生抗肿瘤作用,这是由于TAM功能从原本支持肿瘤的M2型转变为具有肿瘤免疫保护功能的M1型,而不是像最初设想的那样耗尽TAM。
该领域现已达到高度复杂性。正如书中所述,我们现在对肿瘤微环境中不同细胞类型之间的相互作用(包括炎症细胞和间质细胞)有了更深入的理解,这对于未来肿瘤免疫治疗的进一步发展至关重要。
肿瘤与抗肿瘤炎症和免疫反应的分子基础已经揭示出大量可操作的靶点,这些靶点目前正处于不同阶段的临床开发中。迄今为止,越来越多的研究认为,抗PD-1/PD-L1药物已成为免疫治疗的核心支柱,未来的治疗策略将通过与其他靶向特定免疫抑制机制的化合物组合,进一步提升临床疗效。
目前,该领域的关注点正从传统的信号通路转向两个前景广阔的方向。首先是理解肿瘤进化与抗肿瘤免疫反应背后的代谢状态。这一研究推动了对Warburg效应的重新认识,表明炎症细胞与肿瘤细胞在营养物质,尤其是葡萄糖方面展开激烈竞争,它们根据氧气和营养供应调整各自的代谢速率以适应微环境的变化。
系统生物学现已采用代谢组学方法,这些方法能够提供多细胞水平上代谢状态的全局概况,并正致力于提高对肿瘤内特定位置更细胞分辨率的检测能力。第二个关注点是基因表达领域。除了单细胞转录组学的惊人成就,研究者们现在对在系统层面理解基因表达调控的表观遗传机制产生了浓厚兴趣。未来的进展将为我们提供单细胞水平的肿瘤微环境图谱,使我们达到前所未有的理解深度,并借助计算生物学将这些知识整合进动态数学模型中。
未来的转化科学家将越来越依赖于精确模型,以确定合适的免疫治疗策略,并开发出更具预测性的免疫生物标志物来指导治疗决策。尽管复杂性在增加,这些模型有望在临床日常决策中提供简化。在未来几年中,组合免疫疗法以及免疫疗法与标准治疗的联合应用将稳步增长。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 罗荷
图文排版 | 王坤
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab