42.6 临床安全考虑
在基因工程T细胞疗法的临床应用中,最常见且最重要的毒性反应包括靶外肿瘤T细胞介导的正常组织破坏、细胞因子释放综合征(CRS)和神经毒性事件。
B细胞发育不全:由于CAR-T细胞识别正常B细胞表面的CD19,导致了B细胞发育不全,这是CD19特异性CAR修饰T细胞所引发的预期且不可避免的靶外肿瘤毒性。B细胞发育不全被用作CAR-T细胞功能和持久性的药效学标志。在临床试验中,B细胞发育不全通常通过静脉注射免疫球蛋白(IVIg)补充来治疗,以降低因B细胞耗竭引发的感染并发症风险。然而,目前的数据显示不足,尚无法确定这种风险增加是否具有临床意义,或者IVIg替代疗法是否能有效预防感染并发症。
细胞因子释放综合征(CRS):CRS是CAR和TCR T细胞治疗中的常见并发症。CRS患者通常表现为高热、低血压和缺氧,严重时可能导致终末器官衰竭。CRS的发作时间从T细胞输注后几小时至几天不等,通常是由于CAR-T细胞与抗原结合后,继发性促炎细胞因子(如IL-6、TNFα、IFNγ)的大量分泌引发。重症CRS可发展为巨噬细胞激活综合征,表现为噬血细胞增多、高铁蛋白血症、全血细胞减少、肝功能不全、凝血障碍和神经系统症状。
大多数CRS病例可以通过支持性治疗控制。在严重CRS情况下,使用抗IL-6R单克隆抗体tocilizumab可以迅速缓解症状。由于皮质类固醇具有淋巴细胞抑制作用,因此在阻断细胞因子后,常采用皮质类固醇治疗严重CRS。在ALL患者中,CRS的发生频率和严重程度与CAR-T细胞输注时的肿瘤负荷呈正相关。此关联表明,提前对患者进行有效减容,尤其是在MRD患者中,可能显著降低严重CRS的风险。
神经毒性:在一些使用CD19靶向CAR-T细胞治疗的研究中,约29%的患者出现了神经毒性,包括癫痫发作、昏厥、谵妄和吞咽障碍。尽管CAR-T细胞浸润脑脊液的机制尚不完全清楚,且没有证据表明CD19在脑组织中表达,但神经系统症状通常是短暂且在支持性治疗下可逆。部分ALL患者在CRS症状缓解后,仍出现了自限性脑病,且托珠单抗对此无效。最近,Juno Therapeutics停止了其JCAR015项目的开发,该项目在成人B细胞ALL患者的II期试验中,因5名患者死于与治疗相关的脑水肿而终止。在最初的两例死亡后,试验组尝试通过移除氟达拉滨以改善输注后早期毒性,但另外三名患者在仅使用环磷酰胺的情况下仍死于同样的并发症。值得注意的是,有证据表明,加入氟达拉滨可提高CAR-T细胞的扩增、持久性和长期临床效果。
这些严重的毒性事件突显了选择高度专业化的中心进行过继性T细胞治疗研究的重要性,同时也强调了具有细胞治疗经验的医务人员密切监测的重要性,以及在CRS和/或神经毒性发生时早期使用皮质类固醇和/或IL-6阻断治疗的重要性。尽管在TCR T细胞治疗中的毒性与CD19导向CAR-T细胞类似,但CRS和神经毒性的发生率和严重程度相对较低。
一项针对53例接受NY-ESO-1c259 SPEAR®治疗的滑膜肉瘤、黑色素瘤、卵巢癌和多发性骨髓瘤患者的研究显示,最常见的不良反应包括皮疹(49%)、腹泻(40%)、疲劳和发热(各36%)、恶心(26%)、贫血和淋巴细胞减少(各25%)以及粒细胞减少(23%)。大多数这些毒性可能与氟达拉滨/环磷酰胺的淋巴细胞消耗方案有关。与治疗相关的严重(3-4级)不良事件相对较少,CRS、中性粒细胞减少症和发热各仅发生在8%的患者中,而移植物抗宿主病(GvHD)的发生率为6%,仅见于移植后的多发性骨髓瘤患者。迄今为止,未观察到3-4级神经毒性事件。值得注意的是,CRS的发生率因适应症而异,尽管IL-6水平较高,但在接受NY-ESO-1c259 SPEAR®T细胞治疗的自体SCT患者中,未出现严重CRS病例。
基因工程T细胞疗法在缺乏有效治疗的癌症患者中展现了惊人的疗效。然而,为了充分发挥这些疗法的潜力,医生需要深入了解相关的风险及其管理。我们对CRS病理生理学的理解取得了重大进展,使得有效的治疗策略得以发展。然而,仍需进一步研究以更好地理解CAR-T细胞输注后神经毒性事件的病理生理学,这似乎与CRS不同。未来的研究将评估细胞因子阻断在CRS预防中的作用,以及分子安全开关在减少接受CAR或TCR T细胞治疗患者的CRS相关毒性中的应用潜力。
42.7 最大化CAR-T细胞和TCR-T细胞药物安全性和有效性的挑战
鉴于T细胞的强大效力,控制其活性至关重要,以防止产生靶上毒性、非肿瘤毒性,包括那些可能由内源性TCR或与引入的TCR错配引起的毒性,以及由过度激活和细胞因子产生导致的毒性。
如前所述,已有多项技术处于概念或开发阶段,旨在提高CAR-T细胞或TCR-T细胞疗法的安全窗口:
-
免疫受体可以根据其特异性和亲和力进行微调,以区分健康组织和肿瘤组织。
-
可以将活性开关或自杀开关引入治疗细胞,使用小分子药物或单克隆抗体激活或消除治疗细胞。
-
免疫受体可以引入内源性TCR位点,或通过RNA干扰关闭内源性TCR,将T细胞特异性限制为肿瘤特异性免疫受体。
-
免疫受体可以在肿瘤微环境中,利用例如蛋白水解活性等条件,提供一个可激活的灭活状态。
-
逻辑门控受体通过整合多种信号(包括负面信号),帮助区分健康组织和肿瘤组织。
-
基于缺口的技术可用于精确控制目标抗原识别后的基因表达程序,使治疗性T细胞在识别一种肿瘤相关抗原后,诱导表达第二种肿瘤相关抗原的受体,从而将CAR或TCR的表达限制在肿瘤微环境内的T细胞中。这可以确保只表达特定细胞因子、趋化因子和其他效应器。
优化疗效同样至关重要,以便CAR-T细胞和TCR-T细胞疗法实现其作为单次输注疗法的潜力,从而提供长期疾病控制甚至治愈。尽管CAR-T细胞疗法在血液系统恶性肿瘤中显示出良好的治疗前景,但在实体肿瘤中的反应率较为令人失望。来自TCR-T细胞疗法和TILs的证据表明,高效疗法是可以实现的,但细胞产品仍需通过设计改进或与合适的免疫疗法结合,克服肿瘤微环境的抑制性。
目前,有大量增强CAR-T细胞和TCR-T细胞疗法疗效的方法正在临床前或临床试验中进行测试(见图42.2)。如此多的研究反映了该领域的新颖性以及在尝试CAR-T或TCR-T细胞疗法时所面临的多种背景和挑战。
然而,预计最终的最佳方法可能比最初设想的要少,且只有这些方法会被广泛采用。由于PD-1/PD-L1轴已经在几种恶性肿瘤中得到临床验证,并且肿瘤常常通过上调PD-L1来应对来自T细胞的IFN-γ,因此靶向PD-1/PD-L1轴的策略很可能对CAR-T细胞和TCR-T细胞疗法产生积极影响。此外,TGF-β在正常组织的稳态中发挥重要作用,也可能涉及某些免疫抑制途径。由于目前尚无针对TGF-β的系统性抑制疗法获批,未来可以通过基因工程高度定位的治疗性T细胞来实现特异性抑制,从而提供潜在的治疗方案。
总的来说,技术进步已经带来了许多创新,以提高CAR-T细胞和TCR-T细胞疗法的安全性和有效性。然而,这些技术尚未达到足够成熟的水平,无法在短期内提供解决方案,安全地为CD19+血液恶性肿瘤以外的广泛癌症患者群体实现长期疾病控制。不可避免的是,该领域将继续学习如何充分利用现有新技术,并在未来为更多患者带来更多的治疗益处。
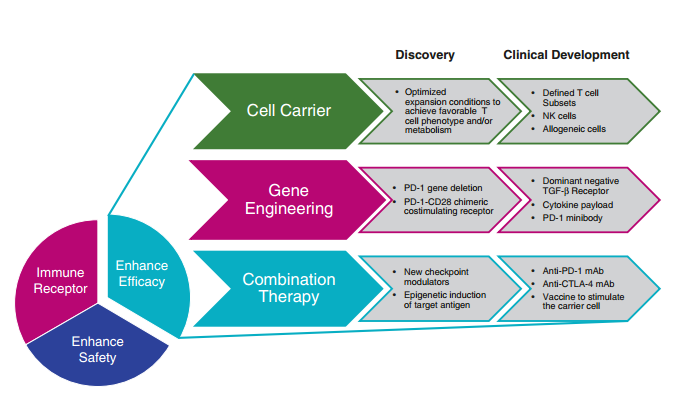
Fig.42.2 增强CAR-T细胞和TCR-T细胞疗法的疗效策略。通过三类途径增强疗效:提高细胞载体的质量或性质,增加基因工程步骤以“武装”治疗性T细胞对抗肿瘤微环境,或使用联合疗法。
42.8 最大化CAR-T细胞和TCR-T细胞药物可及性的挑战
虽然本章主要聚焦于工程T细胞的生物学,但值得注意的是,病毒载体和自体细胞产品的供应链也是影响这些疗法广泛可及性的关键因素。为患者提供工程化T细胞的成本依然高昂,这仍然是限制更多患者获得此类疗法的主要障碍。
载体生产成本和制造工程细胞的成本是两大主要成本驱动因素。目前,能够生产GMP级载体和细胞产品的设施数量有限,现有的设施难以适应大批量生产和市场需求。大多数临床试验使用的慢病毒载体生产困难,因为它们依赖于表达多种基因产物的包装细胞系来生成具有转导能力且复制缺陷的病毒载体。一些专业的合同生产组织(CMO)和制药公司已经开始开发更具可扩展性的生产工艺,这有望在未来3-5年内提高产量并降低成本。此外,基于DNA转座子的无病毒基因转移系统正在崛起,可能进一步减少生产成本。然而,目前判断质粒系统能否完全取代慢病毒基因转移还为时过早。
细胞转导过程是最大的成本驱动因素,这一过程通常需要7-12天,期间进行T细胞的激活、基因转导和扩增。目前,最先进的技术需要B级洁净室和A级层流,以生产针对单个患者的产品。为了降低这些成本,多家技术供应商正在开发替代方案,包括使用封闭袋系统引入部分或全自动化的细胞制造流程。目前已经启动的临床试验中,患者将首次使用完全自动化的桌面细胞处理设备接受治疗。未来的机会在于开发“盒子里的基因治疗”设备,将多个设备放入洁净级别较低的环境中运行,这将有望大幅降低制造成本。A. Kaiser最近的一份报告强调了自动化的优势,并提出了一种新的概念,可能进一步推动制造业从中央工业设施向护理点靠近,从而进一步降低成本。
新兴的核酸酶技术使得对CAR和TCR T细胞进行多基因编辑成为可能,或者结合同源定向重组(HDR),可以将治疗性基因盒与基因组修饰结合。这种技术或许将改变游戏规则,因为它允许从单个供体生成现成的产品,这些产品可以用于多名患者,而不依赖内源性细胞,从而减少同种异体反应的风险。目前,已有多种核酸酶技术,如锌指核酸酶、TALEN核酸酶、巨核酶和CRISPR/Cas9。最近,通过慢病毒转导非人白细胞抗原匹配的供体细胞,并使用TALEN对TCRα链和CD52基因位点进行基因编辑,成功生成了通用CAR19 T细胞,并用于治疗ALL儿童。这些基因编辑的通用CAR-T细胞在约4周内诱导了分子缓解,并持续至异基因干细胞移植前。然而,虽然这种桥接移植策略展示了基因编辑技术的潜力,但仍需长期数据来确定通用CAR-T细胞是否能够替代自体细胞产品,并在体内表现出更长的持久性。
一种更具颠覆性的方法可能是未来使用表面工程的病毒载体,该载体能够高效靶向静息T细胞的特定亚群。通过缩短工艺时间,这种方法可以显著降低制造成本,甚至可能直接在体内对T细胞进行基因修饰。然而,目前尚不清楚这种体内方法何时能够进入临床测试阶段。
总之,我们相信CAR和TCR T细胞疗法的商品化成本将在未来显著下降。这将得益于对GMP级工艺的大量投资,尤其是扩大基因传递病毒载体的生产能力,或者由更便宜的替代基因传递平台取代。此外,自动化技术的出现也将使供应链创新解决方案成为可能。多个行业参与者正在这一领域投入大量资源,这将逐步降低工程细胞产品的成本。然而,成熟的技术解决方案可能还需要4-5年才能广泛用于临床试验,并最终为更广泛的患者群体提供未来的市场供应。
展望未来,该领域有可能转向体内CAR/TCR基因递送方法,至少适用于部分产品,这将引发产品成本的又一次显著下降。
42.9 结论与未来展望
我们得出结论,表达CAR或TCR的改造淋巴细胞在癌症患者中展现出巨大的临床潜力。本文讨论了阻碍工程细胞临床和商业潜力充分发挥的三个关键障碍,并提出了相应的解决方案。如今,已经涌现出一系列新型使能技术,这些技术有望开发出更安全、更有效的药物,为那些非CD19靶点的患者提供变革性益处。此外,未来将会有创新的供应链解决方案,以应对自体细胞产品的主要成本驱动因素,并使更多医疗需求未被满足的患者获得这些新型疗法。
一旦通过开发这些关键技术实现患者获益最大化、成本最小化,该领域将能够将价值转移至更大规模的CAR和TCR T细胞药物管线中,靶向肿瘤中表达的多种共享和个性化抗原。早期的CAR-T细胞产品使用的是缺乏共刺激结构域的简单CAR构造,在1998年至2008年期间进行了初步临床评估。这些开创性临床试验并未为患者带来显著的抗肿瘤活性。然而,随着第二代CAR结构的出现,尤其是在ALL、DLBCL和CLL患者中,产生了前所未有的临床反应。这一突破点燃了一个围绕细胞疗法的新兴产业,预计首批CAR-T细胞产品可能在2017年获得上市许可。
尽管B细胞恶性肿瘤在肿瘤学中仅占据相对较小的市场份额,且工程淋巴细胞的生产成本依然较高,但我们期望持续的技术进步将推动细胞疗法取得进一步成功。虽然未来的发展路径难以完全预测,但以目前的技术进步速度,似乎不可避免的是,CAR-T细胞和TCR-T细胞疗法将为越来越多的患者带来成功和希望。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 曾世纪
图文排版 | 林子畅 邓越华
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号:OncoLab